- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Решение задач
Содержание
- 1. Презентация по химии Решение задач
- 2. Слайд 2
- 3. Массовая доля кислорода в одноосновной аминокислоте равна
- 4. Массовая доля кислорода в одноосновной аминокислоте равна
- 5. Домашнее задание:Определить химическую формулу соединения, имеющего состав:
- 6. Относительная плотность углеводорода по водороду, имеющего состав:
- 7. Относительная плотность углеводорода по водороду, имеющего состав:
- 8. Домашнее задание:Относительная плотность паров органического кислородсодержащего соединения
- 9. Определите молекулярную формулу алкана, если известно, что
- 10. Определите молекулярную формулу алкана, если известно, что
- 11. Домашнее задание:Относительная плотность паров предельного альдегида по кислороду равна 1,8125. Выведите молекулярную формулу альдегида. Ответ: C3Н6О
- 12. Массовая доля углерода в соединении равна 39,97
- 13. Массовая доля углерода в соединении равна 39,97
- 14. Массовая доля углерода в соединении равна 39,97
- 15. Массовая доля углерода в соединении равна 39,97
- 16. Массовая доля углерода в соединении равна 39,97
- 17. Дано: w (С) = 39,97 % w
- 18. Домашнее задание:Углеводород содержит 81,82 % углерода. Масса
- 19. Какова молекулярная формула углеводорода, имеющего плотность
- 20. Какова молекулярная формула углеводорода, имеющего плотность 1,97
- 21. Какова молекулярная формула углеводорода, имеющего плотность 1,97
- 22. Какова молекулярная формула углеводорода, имеющего плотность 1,97
- 23. Домашнее задание:Относительная плотность паров кислородсодержащего органического соединения
- 24. Соединение содержит 62,8% S и 37,2%
- 25. Соединение содержит 62,8% S и 37,2% F.
- 26. Домашнее задание:Все 5 задач письменно!!!
Слайд 1 Решение задач на вывод химической формулы
Габриэлян О.С. «Химия»
В каждой естественной
И.Кант
Слайд 3Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу
M
где n - число атомов
Слайд 4Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу
Дано:
w (О) = 42,67%
Вывести формулу
соединения
CnН2n (N Н2) CОOH
Решение:
Рассчитать молярную массу кислоты CnН2n (N Н2) CОOH
w (О)
M кислоты = 75 (г/моль)
Найти число атомов углерода в молекуле кислоты и установить её формулу
М = 12 n + 2 n + 16 + 45 =75
14 n = 14, n = 1
Ответ: формула кислоты NН2CН2CОOH
М (NН2CН2 CОOH) = 75 г/моль
Слайд 5Домашнее задание:
Определить химическую формулу соединения, имеющего состав:
натрий – 27,06%; азот
Ответ: NaNO3
Слайд 6Относительная плотность углеводорода по водороду, имеющего состав: w(С) = 85,7 %;
М (CхНу) = D(Н2) ·М (Н2)
Слайд 7Относительная плотность углеводорода по водороду, имеющего состав: w(С) = 85,7 %;
Дано:
w (С) = 85,7 %
w (Н) = 14,3 %
D Н2 (CхНу) = 21
Вывести формулу соединения
CхНу- ?
Решение:
Находим относительную молярную массу углеводорода, исходя из величины его относительной плотности: М (CхНу)= D (Н2) ·М (Н2)
М (CхНу)= 21 · 2 = 42
m(С) = 42г.*85.7% /100% = 36 г.
m (Н) = 42г.*14.3% /100% = 6 г.
Находим количество вещества атомов углерода и водорода
n (С) = 36г :12 г/моль = 3 моль
n (Н) = 6г.: 1 г/моль = 6 моль
Ответ: истинная формула вещества C3Н6.
Слайд 8Домашнее задание:
Относительная плотность паров органического кислородсодержащего соединения по кислороду равна 3,
Слайд 9Определите молекулярную формулу алкана, если известно, что его пары в 2,5
М (в-ва) = ρ · М (газообр. в-ва)
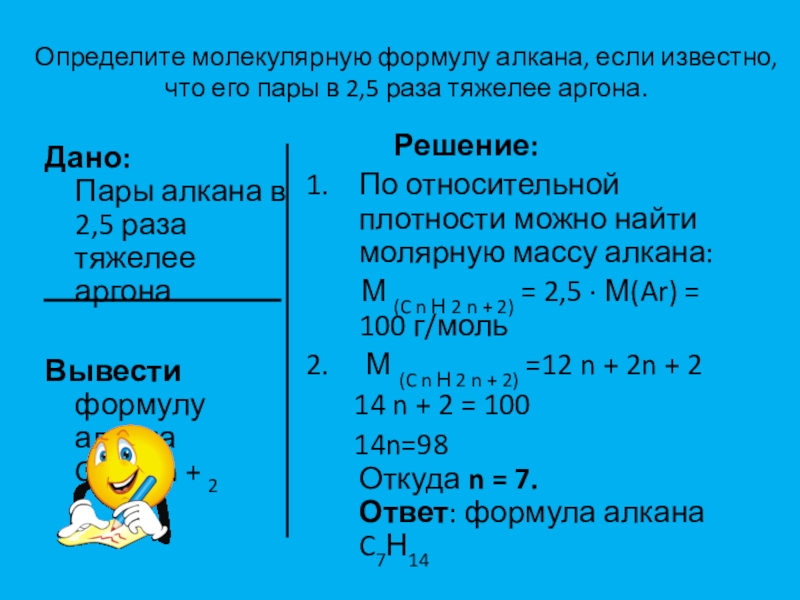
Слайд 10Определите молекулярную формулу алкана, если известно, что его пары в 2,5
Дано:
Пары алкана в 2,5 раза тяжелее аргона
Вывести формулу алкана
C n Н2 n + 2
Решение:
По относительной плотности можно найти молярную массу алкана:
М (C n Н 2 n + 2) = 2,5 · М(Ar) = 100 г/моль
М (C n Н 2 n + 2) =12 n + 2n + 2
14 n + 2 = 100
14n=98
Откуда n = 7.
Ответ: формула алкана C7Н14
Слайд 11Домашнее задание:
Относительная плотность паров предельного альдегида по кислороду равна 1,8125. Выведите
Слайд 12 Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73
М находится по соотношению,
или
М
Слайд 13Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73
Дано:
w (С) = 39,97 %
w (Н) = 6,73 %
w (0) = 53,30 %
Vн.у. (CхHуОz) = 300 мл.
m (CхHуОz) = 2,41 г.
Вывести формулу соединения
CхНуОz- ?
Слайд 14Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73
Дано:
w (С) = 39,97 %
w (Н) = 6,73 %
w (0) = 53,30 %
Vн.у. (CхHуОz) = 300 мл.
m (CхHуОz) = 2,41 г.
Вывести формулу
соединения
CхНуОz- ?
Решение:
Для расчёта выбираем 100г. соединения.
Тогда масса углерода равна 39,97 г; водорода 6,73 г; кислорода 53,30 г.
Определяем количество вещества:
n (С) = 39,97г :12 г/моль = 3,33 моль
n (Н) = 6,73г.: 1,008 г/моль = 6,66 моль
n (0) = 53,3г.: 16 г/моль = 3,33 моль
Слайд 15Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73
Дано:
w (С) = 39,97 %
w (Н) = 6,73 %
w (0) = 53,30 %
Vн.у. (CхHуОz) = 300 мл.
m (CхHуОz) = 2,41 г.
Вывести формулу
соединения
CхНуОz- ?
Решение:
Определяем наименьшее общее кратное – 3,33.
n (С) : n (Н) : n (0) = 1 : 2 : 1
Простейшая формула соединения – CH2О
М (CH2О) = 30 г/моль
Определяем молярную массу соединения по соотношению:
0,3 л. – 2,41 г.
22,4 л. – х г.
х = (22,4 · 2,41)/0,3 = 180
Слайд 16Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73
Дано:
w (С) = 39,97 %
w (Н) = 6,73 %
w (0) = 53,30 %
Vн.у. (CхHуОz) = 300 мл.
m (CхHуОz) = 2,41 г.
Вывести формулу
соединения
CхНуОz- ?
Решение:
К = 180 : 30 = 6
Определяем молекулярную формулу соединения, умножая стехиометрические коэффициенты в простейшей формуле на 6.
Ответ: искомая формула - C6H12О6
Слайд 17Дано: w (С) = 39,97 % w (Н) = 6,73 % w (0)
300 мл. m (CхHуОz) =
2,41 г.
Вывести
формулу
соединения CхНуОz- ?
Решение:
Для расчёта выбираем 100г. соединения.
Тогда масса углерода равна 39,97 г; водорода 6,73 г; кислорода 53,30 г.
Определяем количество вещества:
n (С) = 39,97г :12 г/моль = 3,33 моль
n (Н) = 6,73г.: 1,008 г/моль = 6,66 моль
n (0) = 53,3г.: 16 г/моль = 3,33 моль
Определяем наименьшее общее кратное – 3,33.
n (С) : n (Н) : n (0) = 1 : 2 : 1
Простейшая формула соединения – CH2О
М (CH2О) = 30 г/моль
Определяем молярную массу соединения по соотношению:
0,3 л. – 2,41 г.
22,4 л. – х г.
х = (22,4 · 2,41)/0,3 = 180 Или по формуле М= Vm · m/ V
К = 180 : 30 = 6
Определяем молекулярную формулу соединения, умножая стехиометрические коэффициенты в простейшей формуле на 6.
Ответ: искомая формула - C6H12О6
Слайд 18Домашнее задание:
Углеводород содержит 81,82 % углерода. Масса 1 л. этого углеводорода
Слайд 19 Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при
М (в-ва)=Vm·ρ
Слайд 20Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании
Дано:
M (CхHу) = 4,4 г.
ρ (н.у.) = 1,97 г/л
V (СО2) = 6,72 л.
m (Н2О) = 7,2 г.
Вывести формулу
CхHу - ?
Решение:
1. Находим относительную молярную массу углеводорода, исходя из величины его относительной плотности:
М (CхHу) = Vm · ρ
М (CхHу) = 22,4л/моль · 1,97г/л = 44г/моль
Слайд 21Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании
Дано:
M (CхHу) = 4,4 г.
ρ (н.у.) = 1,97 г/л
V (СО2) = 6,72 л.
m (Н2О) = 7,2 г.
Вывести формулу
CхHу - ?
Решение:
2. Записываем в алгебраическом виде уравнение реакции горения газа, выразив коэффициенты через х и у.
Слайд 22Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании
Дано:
M (CхHу) = 4,4 г.
ρ (н.у.) = 1,97 г/л
V (СО2) = 6,72 л.
m (Н2О) = 7,2 г.
Вывести формулу
CхHу - ?
Решение:
Составляем пропорции:
4,4 / 44 = 6, 72/ х · 22,4
х = 44 · 6, 72/ 4,4 · 22,4 = 3
4,4 / 44 = 7,2/ y · 9
у = 44 · 7,2/ 4,4 · 9 = 8
Формула соединения C3H8; М (C3H8) = 44 г/моль
Ответ: молекулярная формула соединения C3H8
Слайд 23Домашнее задание:
Относительная плотность паров кислородсодержащего органического соединения по гелию равна 25,5.
Ответ: C6H14О
Слайд 24 Соединение содержит 62,8% S и 37,2% F. Масса 118 мл
М
Слайд 25Соединение содержит 62,8% S и 37,2% F. Масса 118 мл данного
Дано:
w (S) = 62,8 %
w (F) = 37,2 %
m (CхHу) = 0,51 г
V (CхHу) = 118 мл.
Т = 70
Р = 98,64 кПа
Вывести формулу соединения
SхFу - ?
Решение:
Определяем простейшую формулу соединения:
n(S) : n(F) = 62,80/32 : 37,2/19 = 1,96 : 1,96 = 1 : 1
Простейшая формула S F
Находим молярную массу соединения:
M =(0, 51 · 8,31 · 280)/(98,64 ·103·118 ·10-6) =101,95 г/моль.
М (S F) = 101,95: 51 = 2
Следовательно, формула соединения S2 F2 Ответ: S2F2