- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
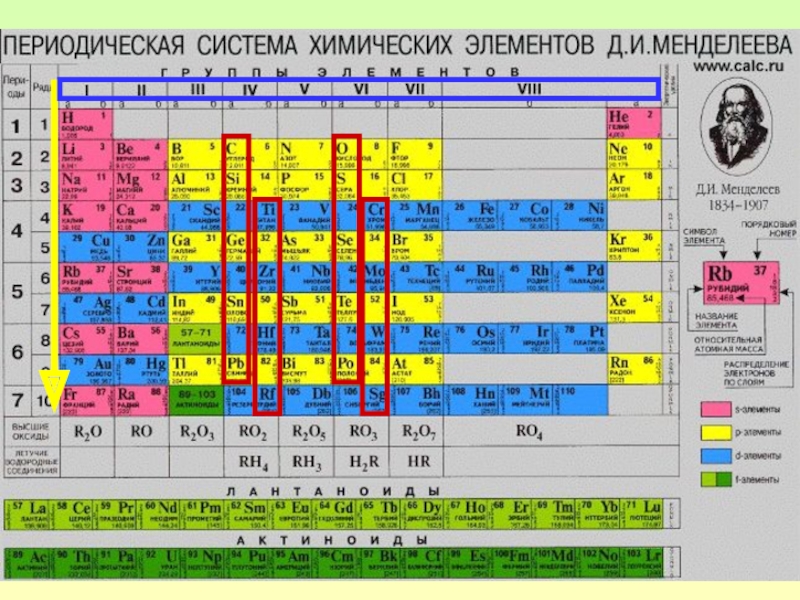
Презентация, доклад по химии Периодический закон Д.И.Менделеева
Содержание
- 1. Презентация по химии Периодический закон Д.И.Менделеева
- 2. Первые системы элементов 1. Деление элементов на
- 3. Октавы Ньюлендса 4. Английский химик Ньюлендс расположил
- 4. 5. Немецкий химик Мейер расположил 28 химических
- 5. 1 марта 1869 года русский
- 6. Для этого ему пришлось исправить
- 7. Свойства химических элементов, а так же свойства
- 8. Слайд 8
- 9. Слайд 9
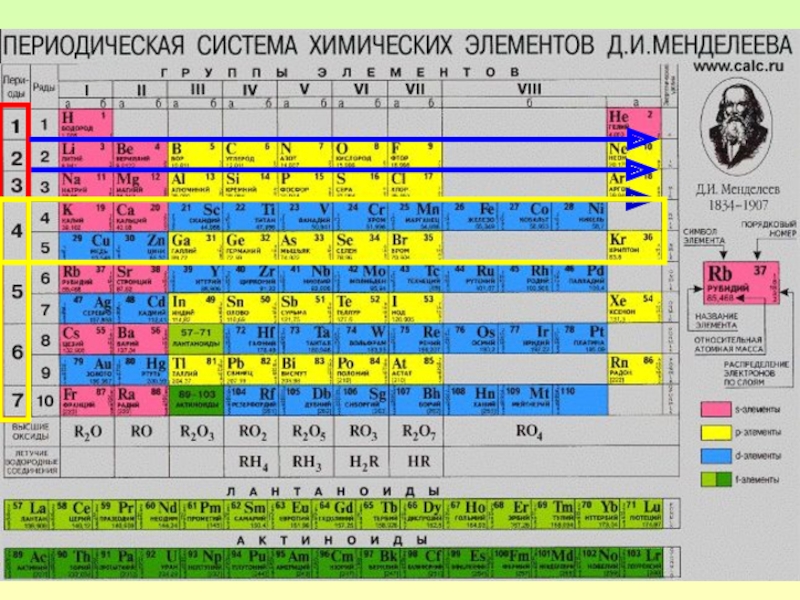
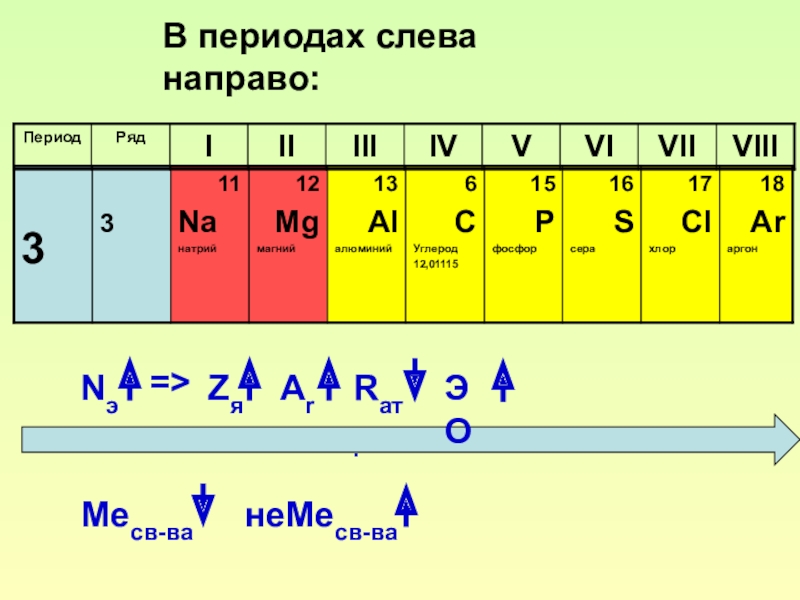
- 10. NэZя=>ArRат.ЭОМесв-ванеМесв-ваВ периодах слева направо:
- 11. Слайд 11
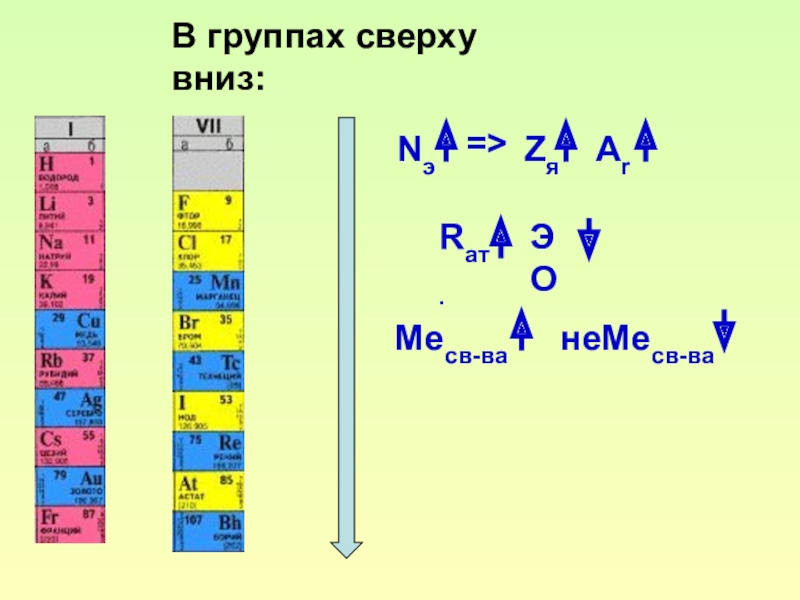
- 12. NэZя=>ArRат.ЭОМесв-ванеМесв-ваВ группах сверху вниз:
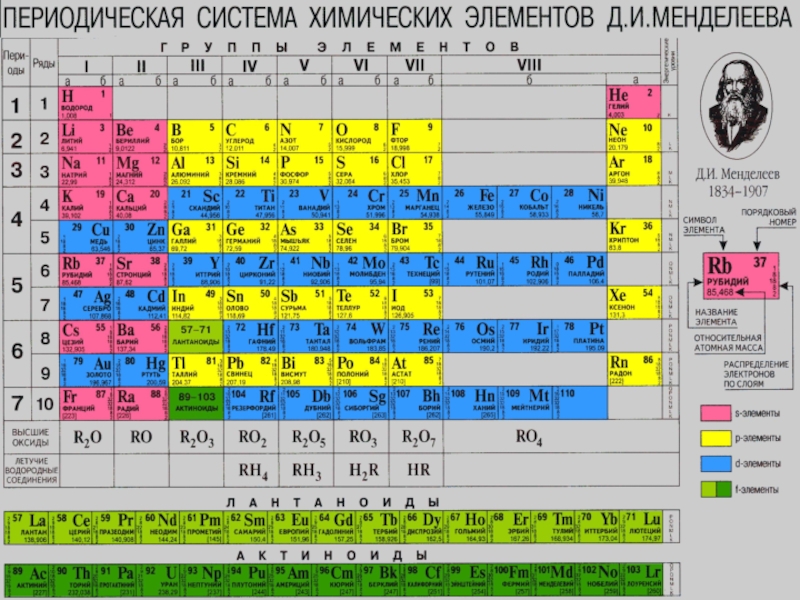
- 13. s-, p-, d-, f-элементы.s-элементы:элементы I, II (A)
- 14. s-, p-, d-, f-элементы.d-элементы:Элементы побочных (В) подгруппУ
- 15. Слайд 15
- 16. Памятник Д. И. Менделееву в Санкт-Петербурге.
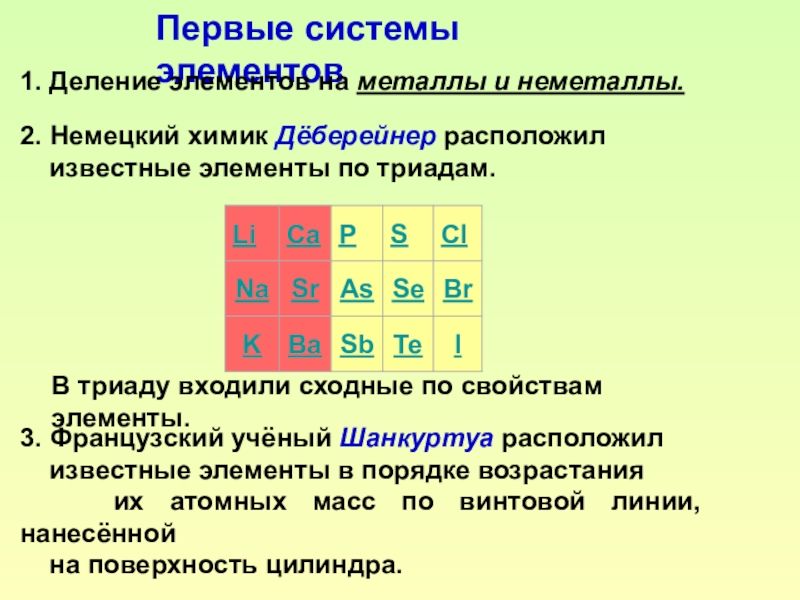
Слайд 2Первые системы элементов
1. Деление элементов на металлы и неметаллы.
2.
известные элементы по триадам.
В триаду входили сходные по свойствам элементы.
3. Французский учёный Шанкуртуа расположил
известные элементы в порядке возрастания
их атомных масс по винтовой линии, нанесённой
на поверхность цилиндра.
Слайд 3Октавы Ньюлендса
4. Английский химик Ньюлендс расположил элементы
в
что их свойства повторяются от седьмого элемента
к восьмому.
Слайд 45. Немецкий химик Мейер расположил 28 химических
элементов в
В группу входили сходные по свойствам элементы.
Основным недостатком этих классификаций являлось то,
что учёные рассматривали только известные элементы.
Слайд 5 1 марта 1869 года русский учёный
Д. И. Менделеев
изложил
отображение в периодическую систему элементов.
Слайд 6 Для этого ему пришлось исправить
атомные массы у двадцати
химических элементов.
За основу классификации Д. И. Менделеев взял атомную массу элементов и расположил их
в порядке возрастания атомных масс
с учётом их свойств.
Некоторые элементы он переставил
местами, например, Co и Ni , Te и I.
Менделеев так же оставил свободные
клетки для неизвестных в то время элементов
с № 21, 31,32, описав подробно их свойства.
Слайд 7Свойства химических элементов,
а так же свойства их соединений
находятся в
от их атомных масс.
Свойства химических элементов,
а так же свойства их соединений
находятся в периодической зависимости
от заряда их атомных ядер.
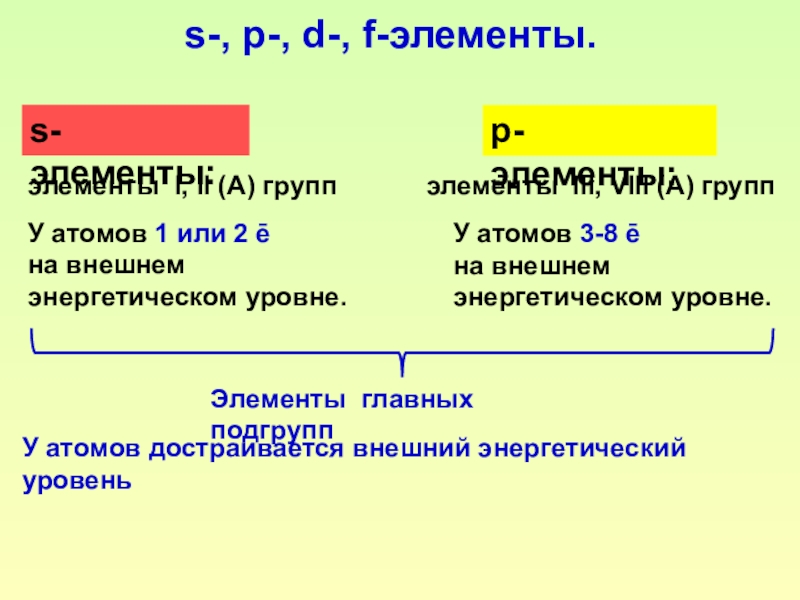
Слайд 13s-, p-, d-, f-элементы.
s-элементы:
элементы I, II (A) групп
У атомов 1 или
на внешнем
энергетическом уровне.
р-элементы:
элементы III, VIII (A) групп
У атомов 3-8 ē
на внешнем
энергетическом уровне.
Элементы главных подгрупп
У атомов достраивается внешний энергетический уровень
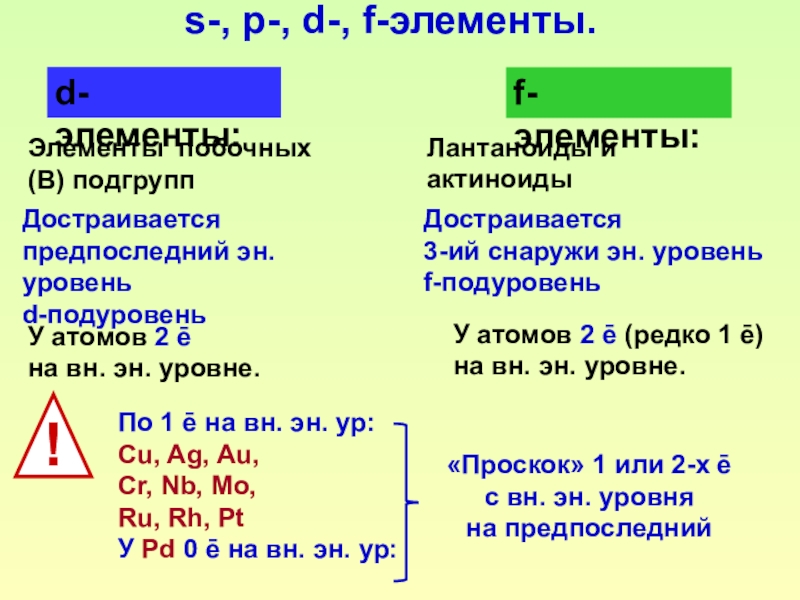
Слайд 14s-, p-, d-, f-элементы.
d-элементы:
Элементы побочных
(В) подгрупп
У атомов 2 ē
на
f-элементы:
Лантаноиды и актиноиды
У атомов 2 ē (редко 1 ē)
на вн. эн. уровне.
Достраивается
предпоследний эн. уровень
d-подуровень
Достраивается
3-ий снаружи эн. уровень
f-подуровень
По 1 ē на вн. эн. ур:
Cu, Ag, Au,
Cr, Nb, Mo,
Ru, Rh, Pt
У Pd 0 ē на вн. эн. ур:
«Проскок» 1 или 2-х ē
с вн. эн. уровня
на предпоследний