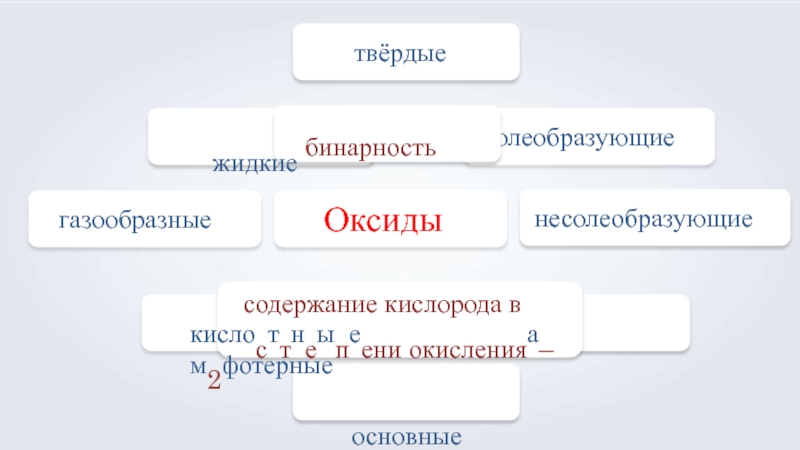
Классификация оксидов основывается на их
агрегатном состоянии и химических свойствах.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Оксиды, их классификация и свойства
Содержание
- 1. Презентация по химии Оксиды, их классификация и свойства
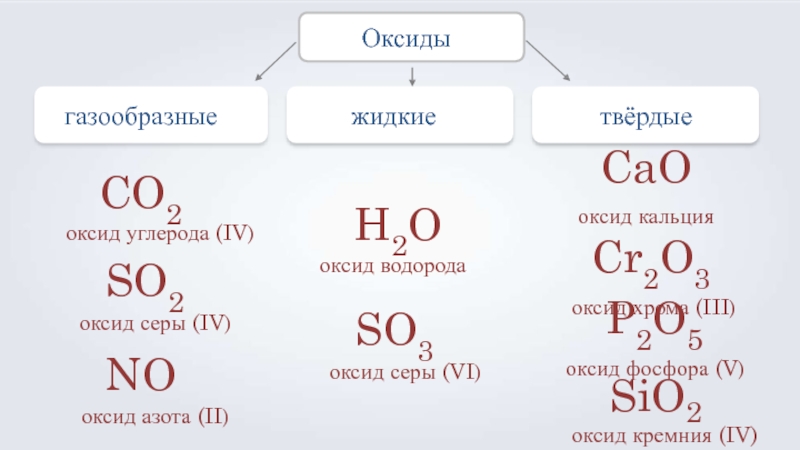
- 2. газообразныежидкиеОксидыCO2оксид углерода (IV)SO2оксид серы (IV)NOоксид азота (II)H2Oоксид
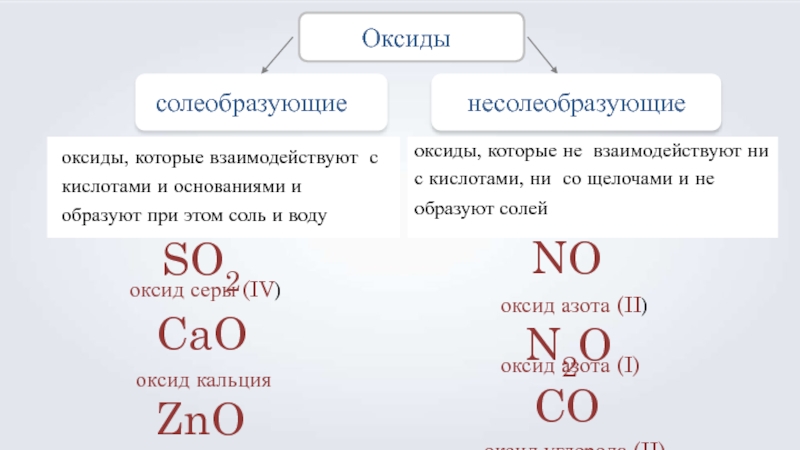
- 3. Оксидысолеобразующиеоксиды, которые взаимодействуют с кислотами и основаниями
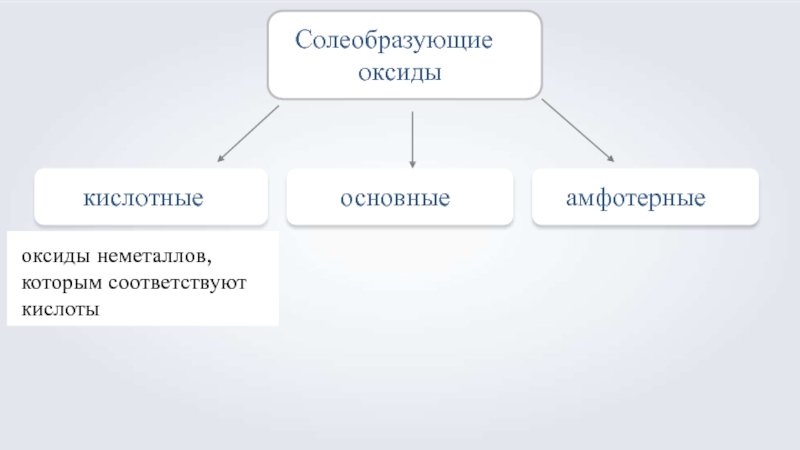
- 4. кислотныеосновныеСолеобразующие оксидыамфотерныеоксиды неметаллов, которым соответствуют кислоты
- 5. Кислотные оксидыSO2 оксид серы (IV) — H2SO3
- 6. CrO3 оксид хрома (VI)H2CrO4хромовая кислотамарганцевая кислотаMn2O7 оксид
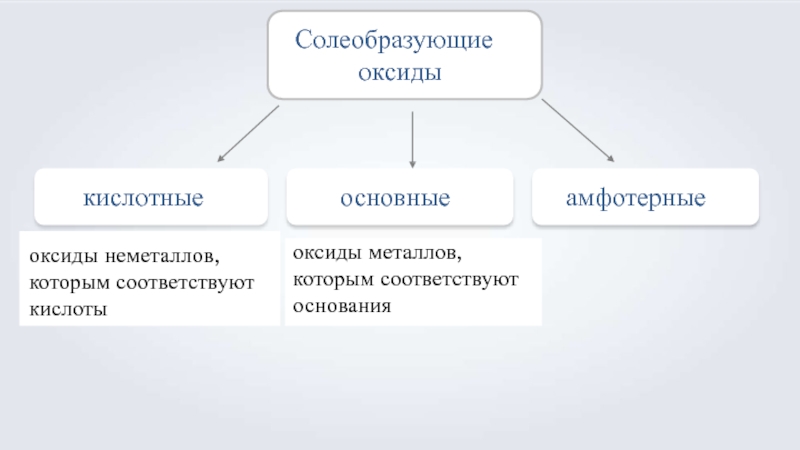
- 7. кислотныеосновныеСолеобразующие оксидыамфотерныеоксиды неметаллов, которым соответствуют кислотыоксиды металлов, которым соответствуют основания
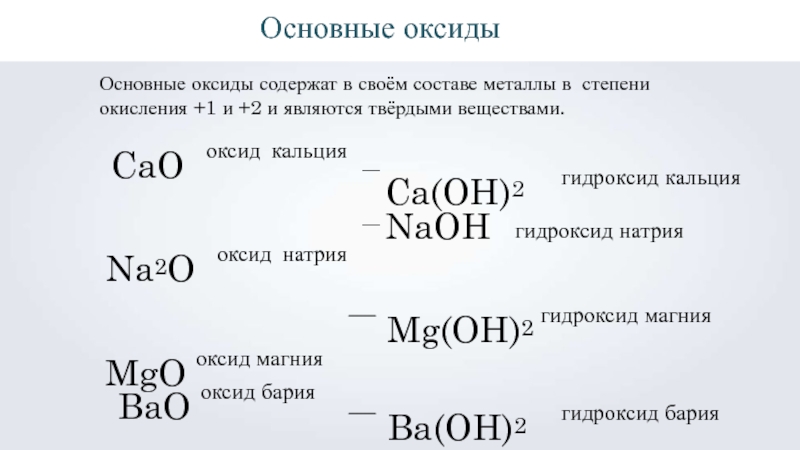
- 8. Основные оксидыОсновные оксиды содержат в своём составе
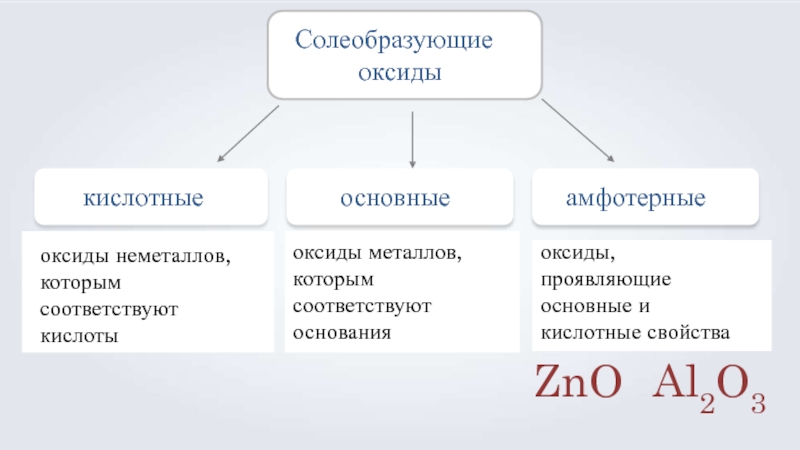
- 9. кислотныеосновныеСолеобразующие оксидыамфотерныеоксиды неметаллов, которым соответствуют кислотыоксиды металлов, которым соответствуют основанияоксиды, проявляющие основные и кислотные свойстваZnO Al2O3
- 10. Оксидыгазообразныетвёрдыесолеобразующиенесолеобразующиежидкие бинарностьсодержание кислорода вкислосттнеыпеени окисленияа–м2фотерныеосновные
Слайд 1Оксиды — это сложные вещества, состоящие из двух химических элементов, один из
Слайд 2газообразные
жидкие
Оксиды
CO2
оксид углерода (IV)
SO2
оксид серы (IV)
NO
оксид азота (II)
H2O
оксид водорода
SO3
оксид серы (VI)
твёрдые
CaO
оксид кальция
Cr2O3
оксид
P2O5
оксид фосфора (V)
SiO
2
оксид кремния (IV)
Слайд 3Оксиды
солеобразующие
оксиды, которые взаимодействуют с кислотами и основаниями и образуют при этом
SO2
оксид серы (IV)
CaO
оксид кальция
ZnO
оксид цинка
несолеобразующие
оксиды, которые не взаимодействуют ни с кислотами, ни со щелочами и не образуют солей
NO
оксид азота (II)
N2O
оксид азота (I)
CO
оксид углерода (II)
Слайд 4кислотные
основные
Солеобразующие оксиды
амфотерные
оксиды неметаллов, которым соответствуют кислоты
Слайд 5Кислотные оксиды
SO2 оксид серы (IV) — H2SO3 сернистая кислота P2O5 оксид
азотистая кислота
азотная кислота
N2O3 оксид азота (III) — HNO2 N2O5 оксид азота (V) — HNO3
Слайд 6CrO3 оксид хрома (VI)
H2CrO4
хромовая кислота
марганцевая кислота
Mn2O7 оксид марганца (VII) — HMnO4
H2Cr2O7 дихромовая
SO3 оксид серы (VI)— H2SO4 серная кислота
CO2 оксид углерода (IV) — H2CO3 угольная кислота
Кислотные оксиды
Слайд 7кислотные
основные
Солеобразующие оксиды
амфотерные
оксиды неметаллов, которым соответствуют кислоты
оксиды металлов, которым соответствуют основания
Слайд 8Основные оксиды
Основные оксиды содержат в своём составе металлы в степени окисления
— Ca(OH)2 гидроксид кальция
гидроксид натрия
— NaOH
CaO оксид кальция Na2O оксид натрия MgO оксид магния
BaO оксид бария
Mg(OH)2 гидроксид магния
Ba(OH)2 гидроксид бария
Слайд 9кислотные
основные
Солеобразующие оксиды
амфотерные
оксиды неметаллов, которым соответствуют кислоты
оксиды металлов, которым соответствуют основания
оксиды, проявляющие
ZnO Al2O3