- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Окислительно-восстановительные реакции (11 класс)
Содержание
- 1. Презентация по химии Окислительно-восстановительные реакции (11 класс)
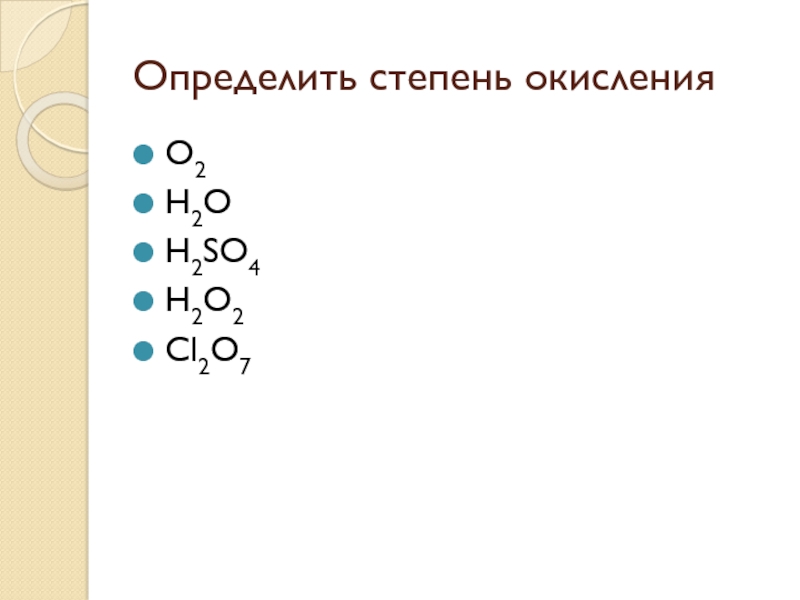
- 2. Определить степень окисленияO2H2OH2SO4H2O2Cl2O7
- 3. Выбрать ОВРHNO3 ⇨ NO2 + H2O + O2 HNO3 + NaOH ⇨ NaNO3 + H2O
- 4. Определение окислителя и восстановителяОкислитель: понижает степень окисления, принимает электроны, восстанавливается.Восстановитель: повышает степень окисления, отдает электроны, окисляется.
- 5. Алгоритм расстановки коэффициентов методом электронного баланса.Определяем степени
Определить степень окисленияO2H2OH2SO4H2O2Cl2O7
Слайд 4Определение окислителя и восстановителя
Окислитель: понижает степень окисления, принимает электроны, восстанавливается.
Восстановитель: повышает
степень окисления, отдает электроны, окисляется.
Слайд 5Алгоритм расстановки коэффициентов методом электронного баланса.
Определяем степени окисления в каждом веществе.
Подчеркиваем
элементы, изменившие степень окисления.
Выписываем окислитель, показываем переход электронов. Подписываем окислитель.
Выписываем восстановитель, показываем переход электронов. Подписываем восстановитель.
Находим НОК чисел электронов.
Делим НОК на каждое число электронов, получаем коэффициенты.
Ставим полученные коэффициенты в уравнение.
Доставляем необходимые коэффициенты для веществ, элементы в которых не изменили степень окисления.
Выписываем окислитель, показываем переход электронов. Подписываем окислитель.
Выписываем восстановитель, показываем переход электронов. Подписываем восстановитель.
Находим НОК чисел электронов.
Делим НОК на каждое число электронов, получаем коэффициенты.
Ставим полученные коэффициенты в уравнение.
Доставляем необходимые коэффициенты для веществ, элементы в которых не изменили степень окисления.