- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Общие способы получения металлов
Содержание
- 1. Презентация по химии Общие способы получения металлов
- 2. В природе такие химические элементы как металлы
- 3. Слайд 3
- 4. Слайд 4
- 5. Если металл в природных условиях находится в
- 6. В соединениях металлы находятся в окисленном виде
- 7. При этом в зависимости от применяемого способа восстановления металлов из соединений различают: пирометаллургию, гидрометаллургию, электрометаллургию.
- 8. Пирометаллургия охватывает способы получения металлов из руд
- 9. В качестве восстановителя применяют уголь или СО
- 10. Углерод, применяемый в виде кокса, при соответствующих
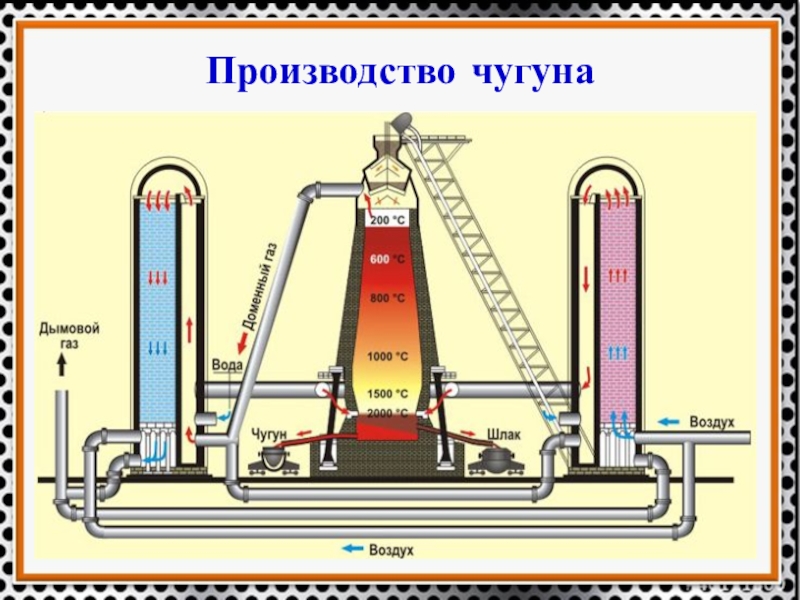
- 11. Производство чугуна
- 12. Выплавка стали проводится в специальных печах (конвертерных, мартеновских,
- 13. С помощью карботермии обычно получают такие металлы,
- 14. С помощью водородотермии получают следующие металлы - молибден,
- 15. В металлотермии одним из наиболее активных восстановителей
- 16. Его можно использовать даже для получения щелочных
- 17. Если в руде находится сульфид металла, то
- 18. Карбонатные руды с этой же целью также предварительно подвергают прокаливанию:
- 19. Гидрометаллургия охватывает способы получения металлов из растворов их
- 20. Так, например, при обработке разбавленной серной кислотой
- 21. Аналогичным методом получают Au, Ag, Zn, Cd,
- 22. Электрометаллургия охватывает способы получения металлов путем электролиза растворов
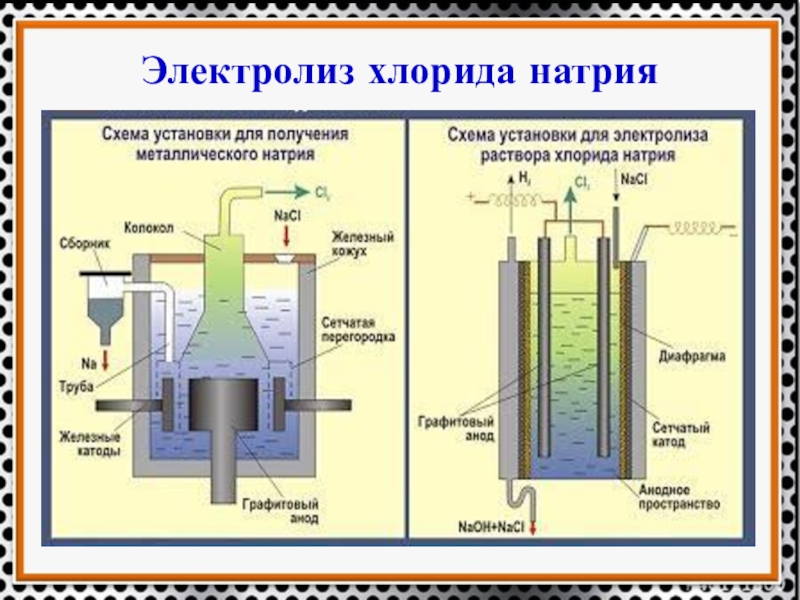
- 23. Электролиз хлорида натрия
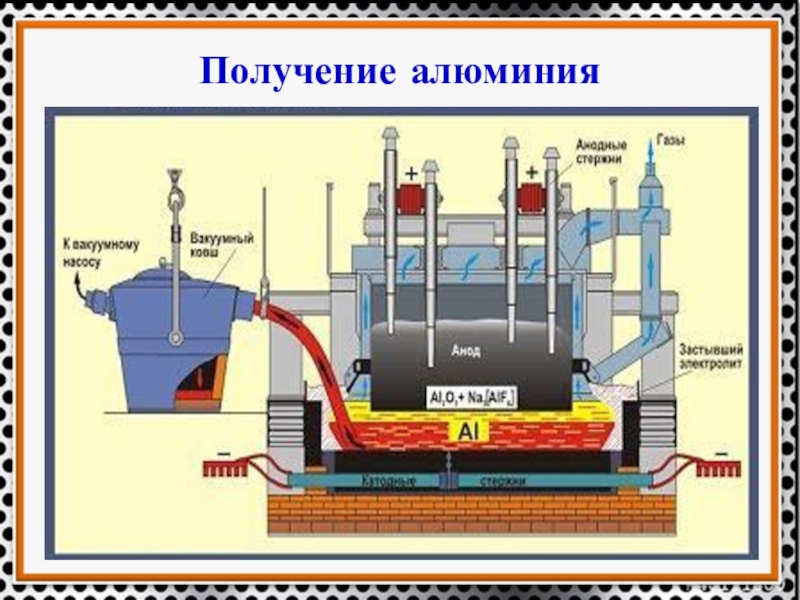
- 24. Получение алюминия
- 25. Таким образом, чтобы реализовать металлургический процесс, надо
- 26. Слайд 26
Слайд 2В природе такие химические элементы как металлы могут находиться как в
Слайд 5Если металл в природных условиях находится в свободном виде, то его
Слайд 6В соединениях металлы находятся в окисленном виде и поэтому для выделения
Слайд 7При этом в зависимости от применяемого способа восстановления металлов из соединений
пирометаллургию,
гидрометаллургию,
электрометаллургию.
Слайд 8Пирометаллургия охватывает способы получения металлов из руд с помощью реакций восстановления,
Сырьем для получения металлов главным образом служат руды, содержащие их оксиды.
Слайд 9В качестве восстановителя применяют уголь или СО (карботермия), активные металлы (металлотермия),
ZnO + C = Zn + CO
Fe2O3 + 3CO = 2Fe + 3CO2
Cr2O3 + 2Al = 2Cr + Al2O3
Ca + 2CsCl = CaCl2 + 2Cs
TiCl4 + 2Mg = Ti + 2MgCl2
MoO3 + 3H2 = Mo + 3H2O
WO3 + 3H2 = W + 3H2O
Слайд 10Углерод, применяемый в виде кокса, при соответствующих высоких температурах может восстановить
Слайд 12Выплавка стали проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева.
Слайд 13С помощью карботермии обычно получают такие металлы, как Fe, Cu, Zn,
Углерод(II)-оксид как восстановитель более эффективен, чем кокс, поскольку находится в газообразном состоянии и способен обеспечивать большую площадь соприкосновения реагирующих веществ.
Слайд 14С помощью водородотермии получают следующие металлы - молибден, вольфрам, рений. Достоинством этого
Слайд 15В металлотермии одним из наиболее активных восстановителей является алюминий, что объясняется
Н(Al2O3) = –1700 кДж/моль.
Алюминий применяют для получения таких металлов, как хром, железо, кобальт, никель.
Слайд 16Его можно использовать даже для получения щелочных и щелочноземельных металлов, так
3CaO + 2Al = Al2O3 +3Ca
CaO + Al2O3 = Ca(AlO2)2
Слайд 17Если в руде находится сульфид металла, то его переводят в оксид
2ZnS + 3O2 = 2ZnO + 2SO2
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
Слайд 19Гидрометаллургия охватывает способы получения металлов из растворов их солей. При этом соединение
Слайд 20Так, например, при обработке разбавленной серной кислотой медной руды, содержащей медь(II)-оксид,
CuO + H2SO4 = CuSO4 + H2O
Затем медь извлекают из раствора вытеснением с помощью порошка железа:
CuSO4 + Fe = Cu + FeSO4
Слайд 21Аналогичным методом получают Au, Ag, Zn, Cd, Mo и другие металлы.
4Au
2Na[Au(CN)2] + Zn = Na2[Zn(CN)4] + 2Au
Слайд 22Электрометаллургия охватывает способы получения металлов путем электролиза растворов или расплавов их соединений:
2Al2O3 =
2NaCl = 2Na + Cl2
2KCl = 2K + Cl2
Таким способом получают наиболее активные металлы, которые при восстановлении водородом, углем, алюминием образуют с этими веществами химические соединения.