- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Водород
Содержание
- 1. Презентация по химии на тему Водород
- 2. Общая характеристикаХимический знак –HПорядковый номер -1Относительная атомная масса Ar(H)=1.008Химическая формула-H2Относительная молекулярная масса Mr(H2)=2.016Валентность-1
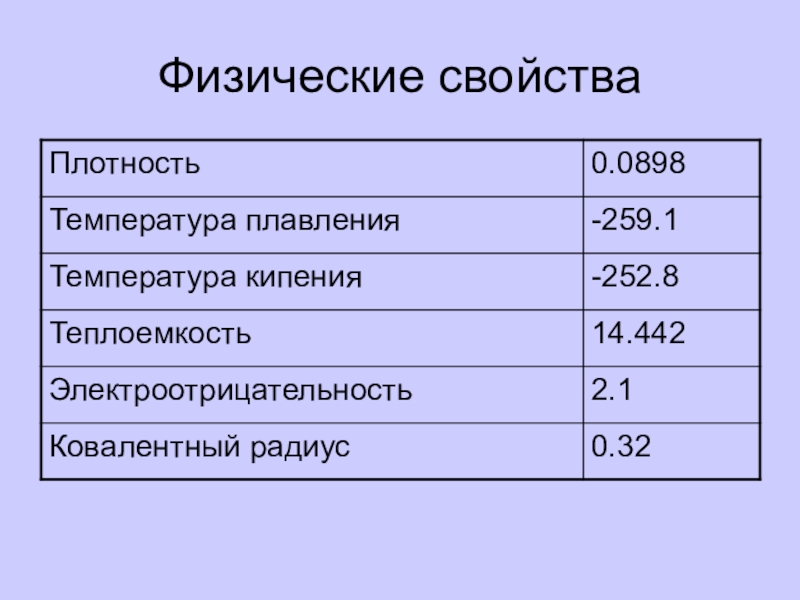
- 3. Физические свойства
- 4. ХИМИЧЕСКИЕ СВОЙСТВАN2 + 3H2 = 2NH3 F2 +
- 5. Получение в лаборатории1. Дейтвие разбавленных кислот на металлы. Zn +
- 6. Получение в промышленности1. Электролиз водных растворов солей:2NaCl +
- 7. Спасибо за просмотр!!! КОНЕЦ
Общая характеристикаХимический знак –HПорядковый номер -1Относительная атомная масса Ar(H)=1.008Химическая формула-H2Относительная молекулярная масса Mr(H2)=2.016Валентность-1
Слайд 2Общая характеристика
Химический знак –H
Порядковый номер -1
Относительная атомная масса Ar(H)=1.008
Химическая формула-H2
Относительная молекулярная
масса Mr(H2)=2.016
Валентность-1
Валентность-1
Слайд 4ХИМИЧЕСКИЕ СВОЙСТВА
N2 + 3H2 = 2NH3
F2 + H2 = 2HF
Cl2 +
H2 = 2HCl
C + 2H2 = CH4
Na + H2 = 2NaH
Ca + H2 = CaH2
CuO + H2 = Cu + H2O
Fe2O3 + 3H2 = 2Fe + 3H2O
WO3 + 3H2 = W + 3H2O
C + 2H2 = CH4
Na + H2 = 2NaH
Ca + H2 = CaH2
CuO + H2 = Cu + H2O
Fe2O3 + 3H2 = 2Fe + 3H2O
WO3 + 3H2 = W + 3H2O
Слайд 5Получение в лаборатории
1. Дейтвие разбавленных кислот на металлы.
Zn + 2HCl = ZnCl2 +
H2
2. Взаимодействие кальция с водой:
Ca + 2H2O = Ca(OH)2 + H2
3. Гидролиз гидридов:
NaH + H2O = NaOH + H2
4. Действие щелочей на цинк или алюминий:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
2. Взаимодействие кальция с водой:
Ca + 2H2O = Ca(OH)2 + H2
3. Гидролиз гидридов:
NaH + H2O = NaOH + H2
4. Действие щелочей на цинк или алюминий:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
Слайд 6Получение в промышленности
1. Электролиз водных растворов солей:
2NaCl + 2H2O → H2 +
2NaOH + Cl2
2. Пропускание паров воды над раскаленным коксом
при температуре около 1000°C:
H2O + C → H2 + CO
3. Из природного газа.
Конверсия с водяным паром:
CH4 + H2O → CO + 3H2 (1000°C)
Каталитическое окисление кислородом:
2CH4 + O2 → 2CO + 4H2
2. Пропускание паров воды над раскаленным коксом
при температуре около 1000°C:
H2O + C → H2 + CO
3. Из природного газа.
Конверсия с водяным паром:
CH4 + H2O → CO + 3H2 (1000°C)
Каталитическое окисление кислородом:
2CH4 + O2 → 2CO + 4H2