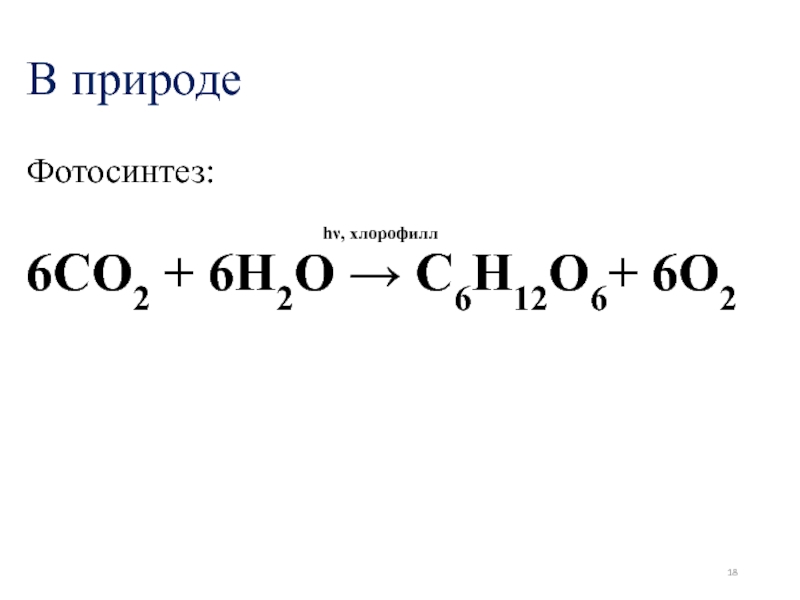- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Углеводы
Содержание
- 1. Презентация по химии на тему Углеводы
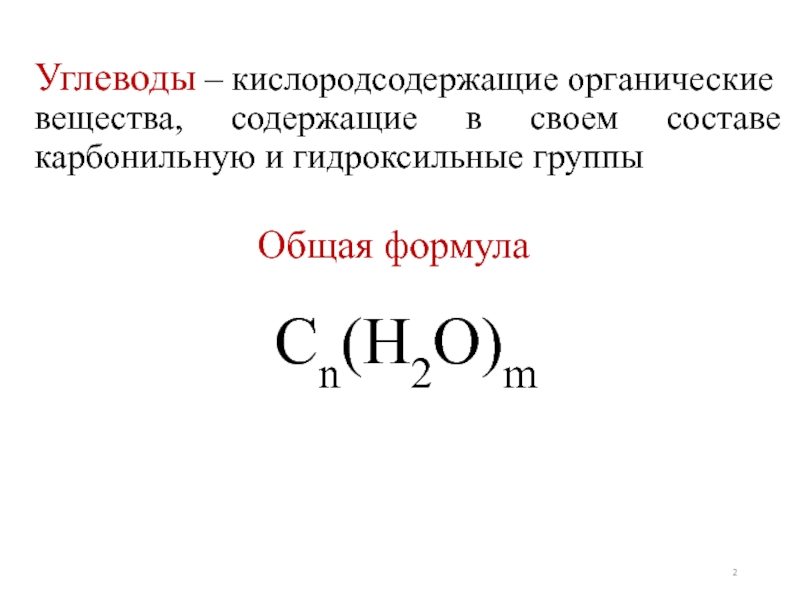
- 2. Углеводы – кислородсодержащие органические вещества, содержащие в своем составе карбонильную и гидроксильные группы Сn(Н2О)mОбщая формула
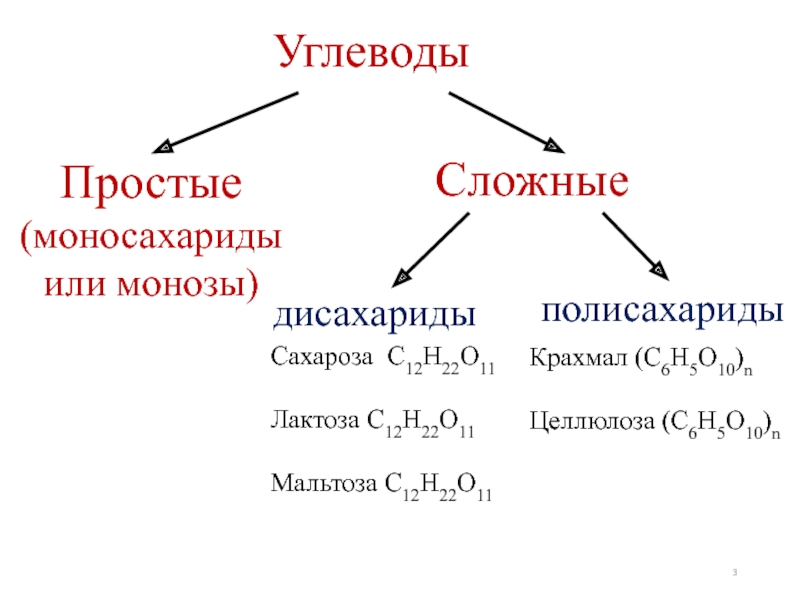
- 3. УглеводыПростые (моносахариды или монозы) Сложные дисахариды полисахариды Сахароза С12Н22О11Лактоза С12Н22О11Мальтоза С12Н22О11Крахмал (С6Н5О10)nЦеллюлоза (С6Н5О10)n
- 4. Моносахариды или монозы
- 5. КлассификацияПо числу атомов углерода в молекуле:Тетрозы (эритроза C4H8O4)Пентозы (рибоза С5Н10О5)Гексозы (глюкоза С6Н12О6)
- 6. 2. По типу наличию кето- или альдегидной
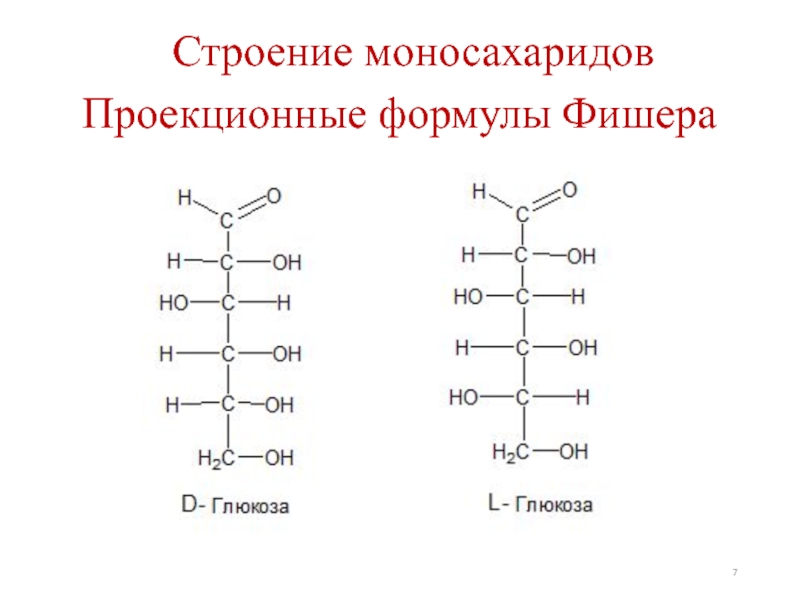
- 7. Строение моносахаридов Проекционные формулы Фишера
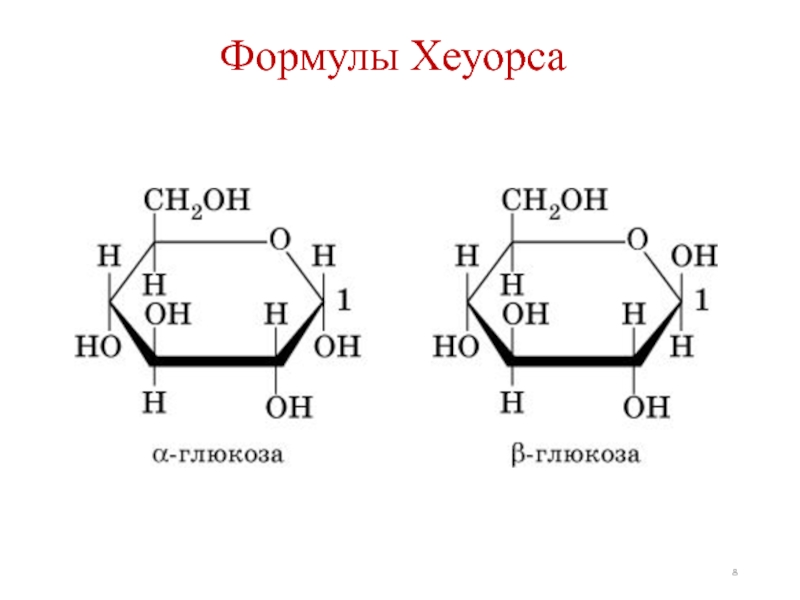
- 8. Формулы Хеуорса
- 9. Физические свойства Бесцветные кристаллические вещества,
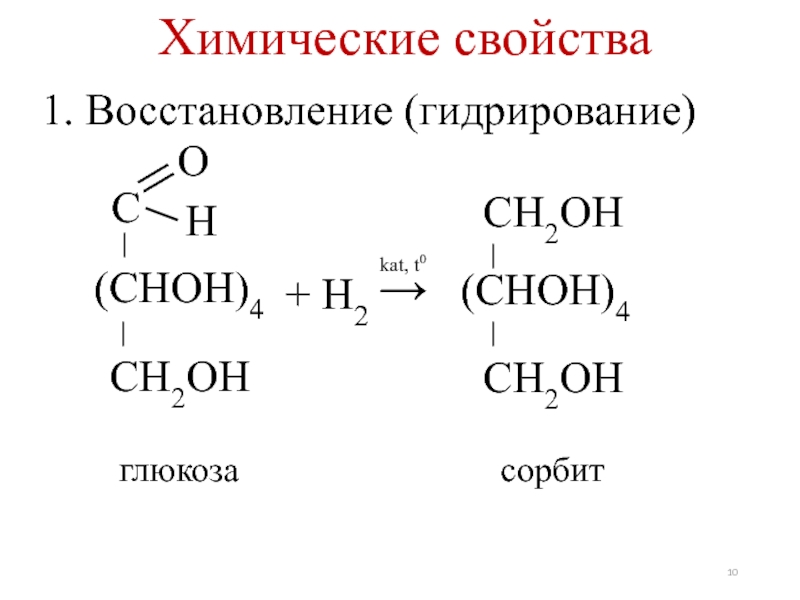
- 10. 1. Восстановление (гидрирование) Химические свойстваС│(СНОН)4 СН2ОН│+ Н2→kat, t0НО= СН2ОН СН2ОН(СНОН)4 ││глюкозасорбит
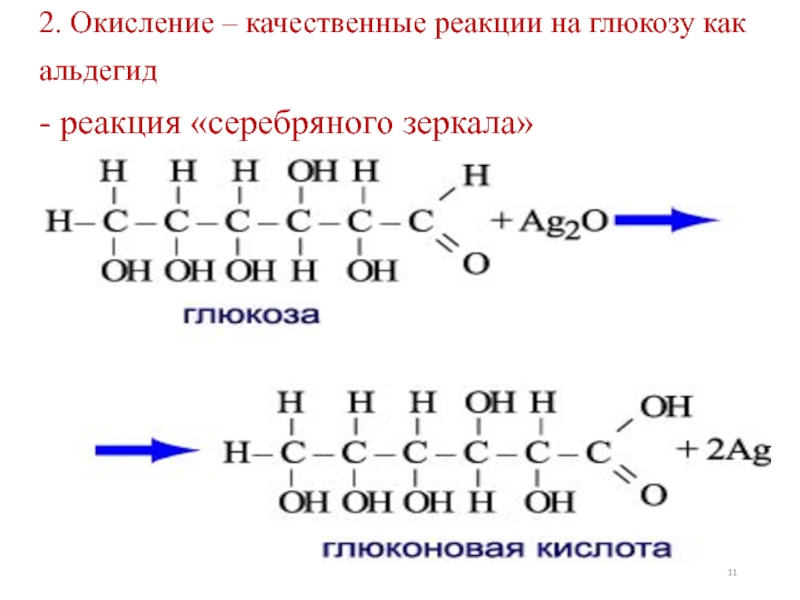
- 11. 2. Окисление – качественные реакции на глюкозу как альдегид - реакция «серебряного зеркала»
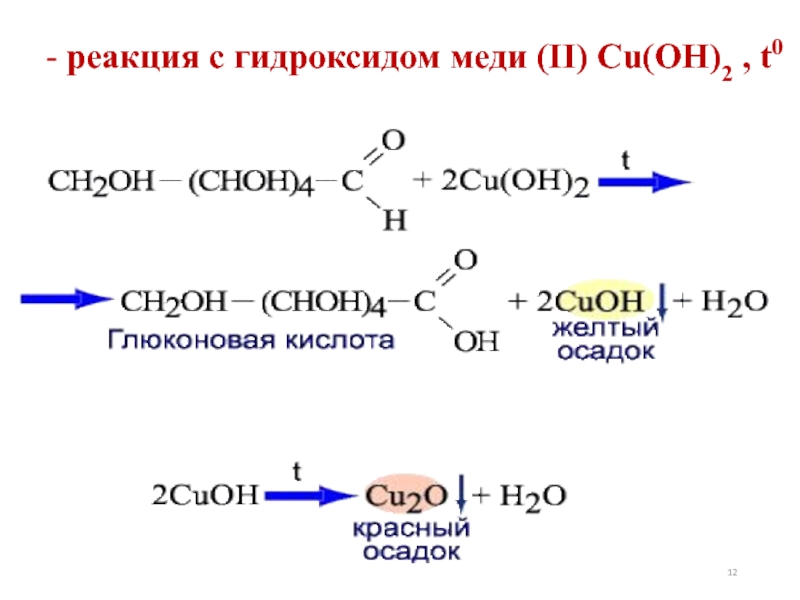
- 12. - реакция с гидроксидом меди (II) Cu(OH)2 , t0
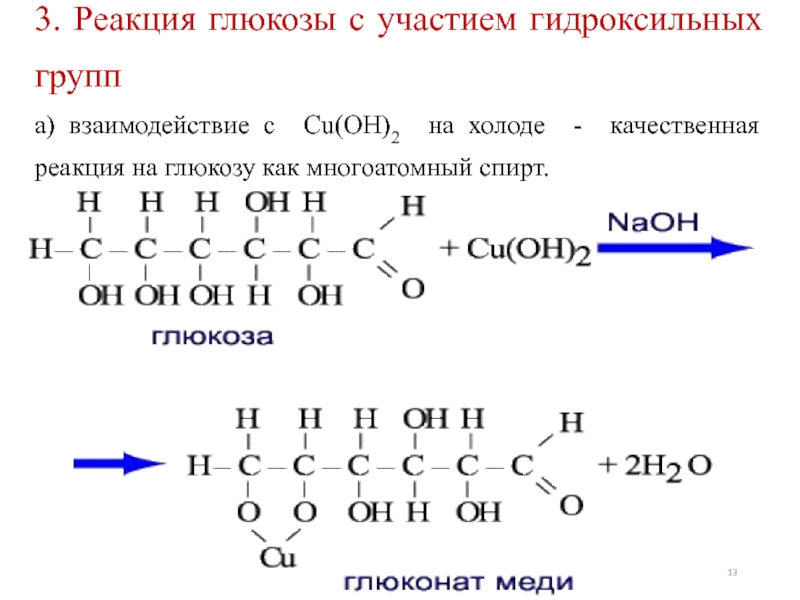
- 13. 3. Реакция глюкозы с участием гидроксильных групп
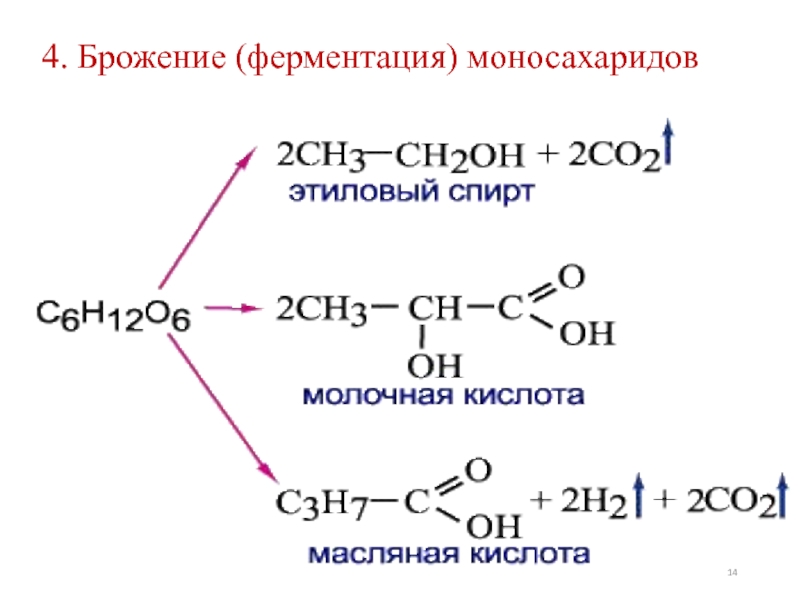
- 14. 4. Брожение (ферментация) моносахаридов
- 15. Глюкоза является ценным питательным продуктом. В организме
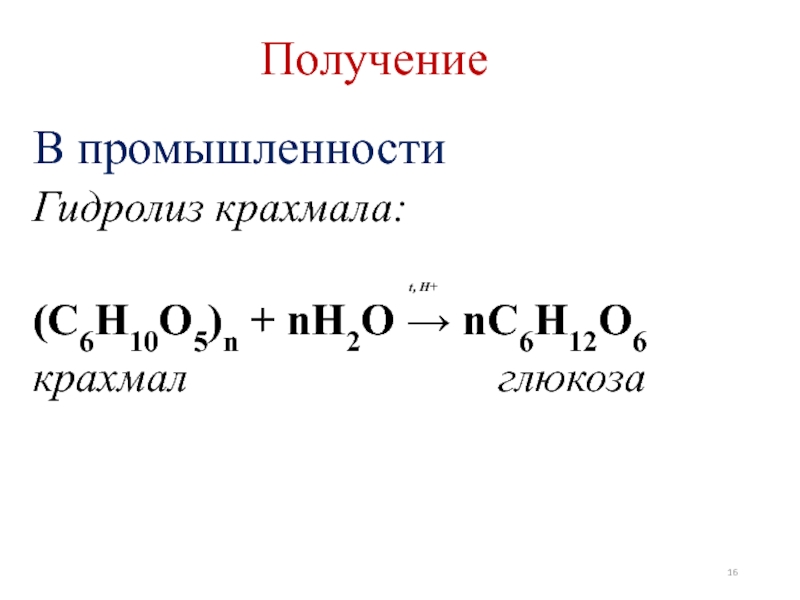
- 16. ПолучениеВ промышленностиГидролиз крахмала:
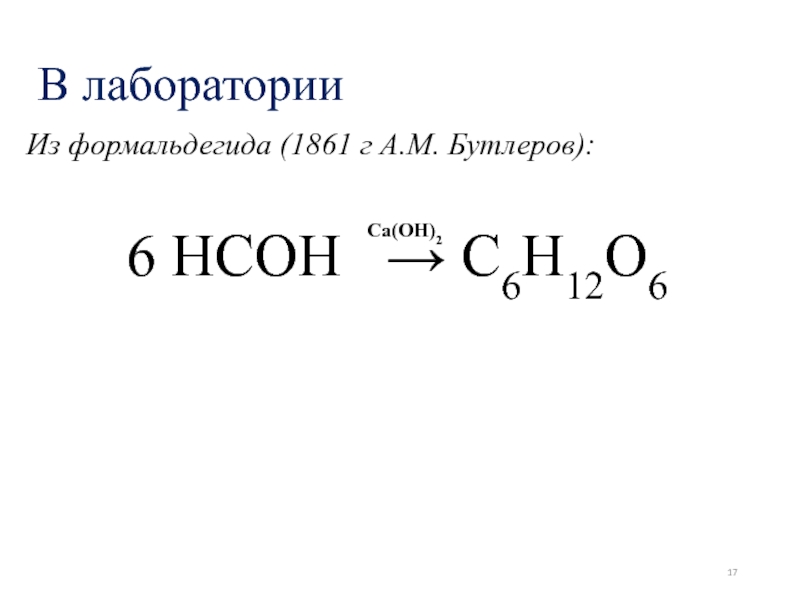
- 17. В лаборатории Из формальдегида (1861 г А.М. Бутлеров): 6 HCOH → C6H12O6 Ca(OH)2
- 18. В природе Фотосинтез: 6CO2 + 6H2O → C6H12O6+ 6O2 hν, хлорофилл
- 19. Дисахариды
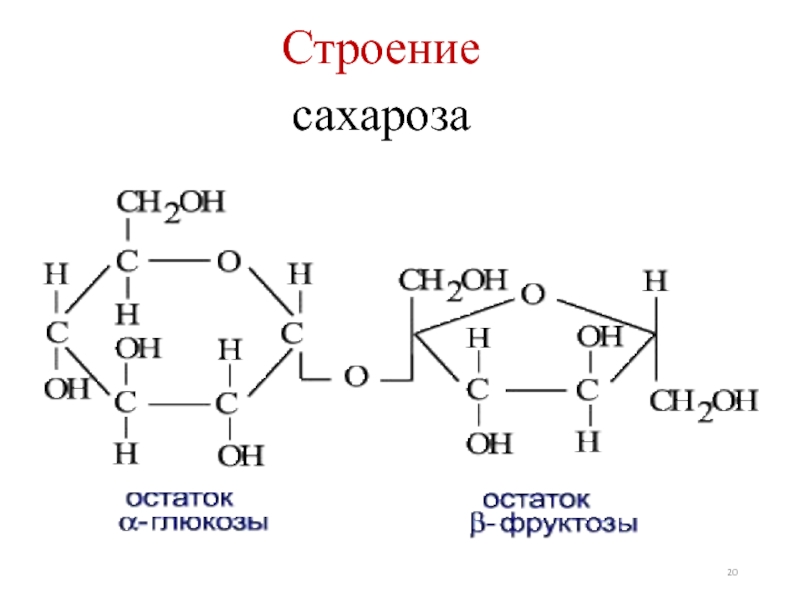
- 20. Строение сахароза
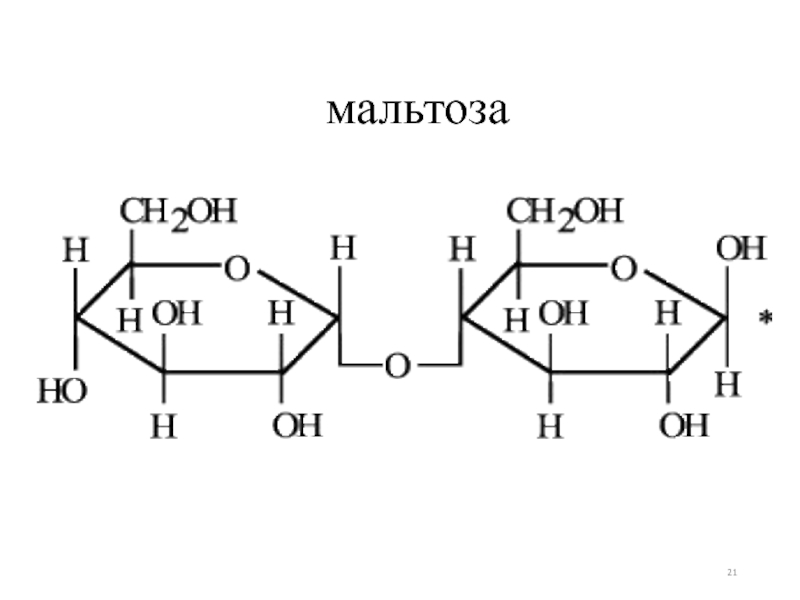
- 21. мальтоза
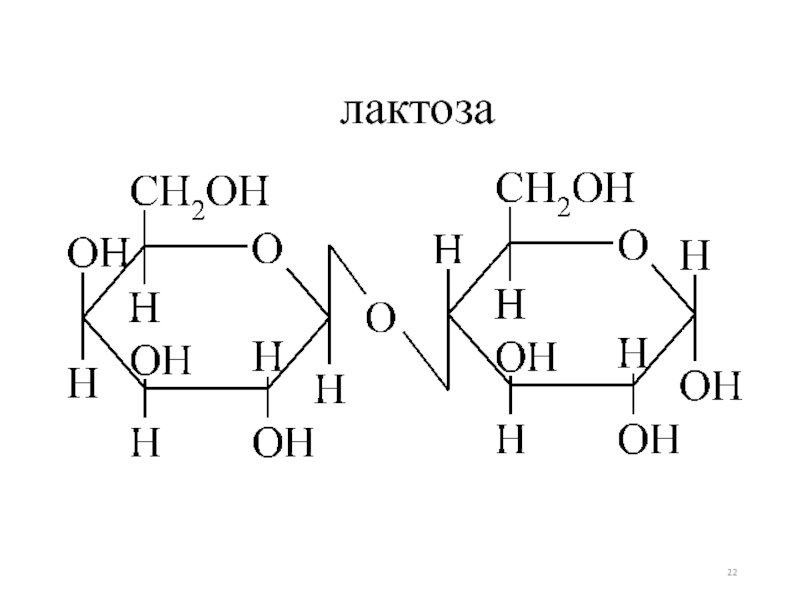
- 22. лактоза
- 23. Физические свойства и нахождение в природе1. Сахароза
- 24. Химические свойства дисахаридов1. Наличие гидроксильных групп в
- 25. 2. Альдегидной группы в сахарозе нет: при
- 26. 4. Реакция сахарозы с водойВажное химическое свойство
- 27. Полисахариды
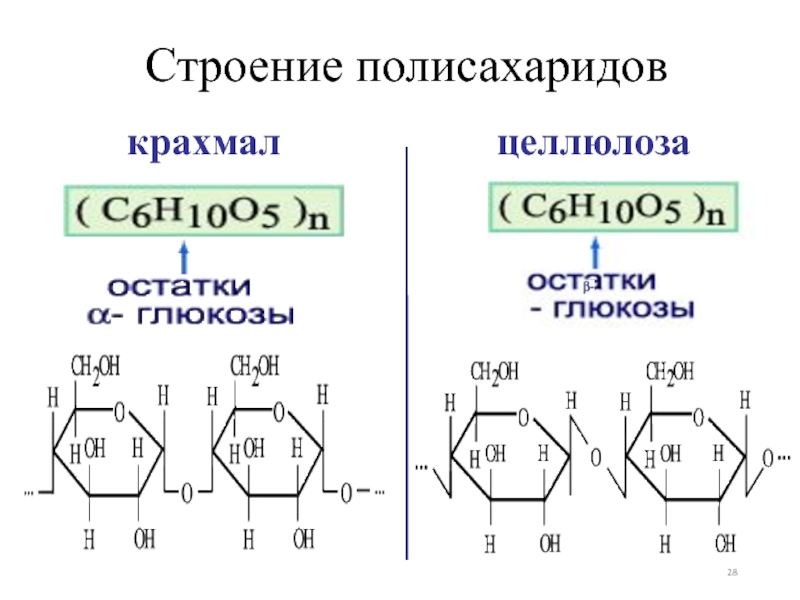
- 28. Строение полисахаридовкрахмалцеллюлоза
- 29. Физические свойстваКрахмал - белый аморфный порошок, не
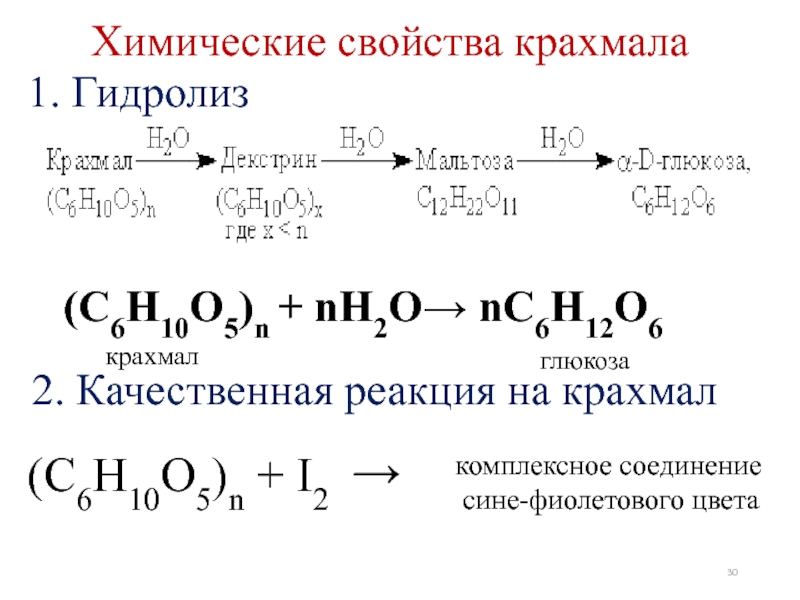
- 30. Химические свойства крахмала1. Гидролиз2. Качественная реакция на
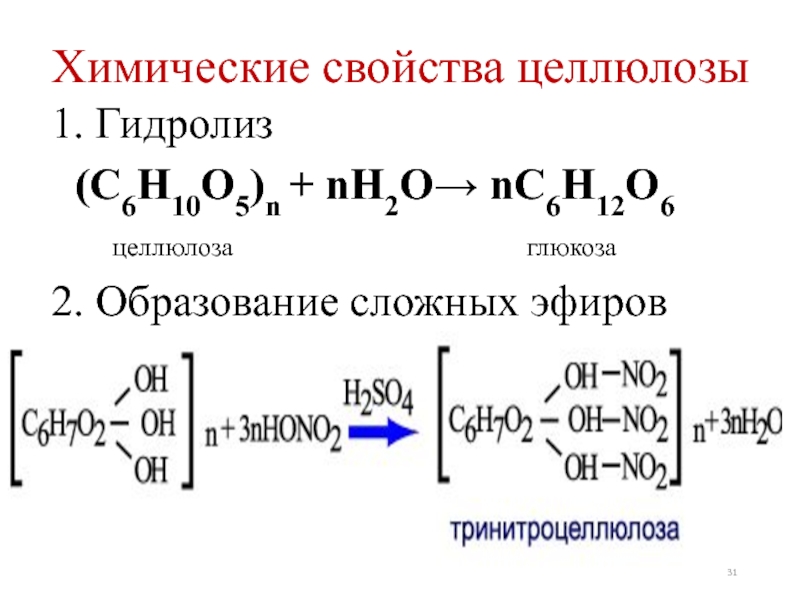
- 31. Химические свойства целлюлозы1. Гидролиз2. Образование сложных эфиров(С6Н10О5)n + nН2О→ nС6Н12О6целлюлозаглюкоза
- 32. 4. Термическое разложение без доступа воздуха:
Слайд 2Углеводы – кислородсодержащие органические вещества, содержащие в своем составе карбонильную и
Сn(Н2О)m
Общая формула
Слайд 3Углеводы
Простые (моносахариды или монозы)
Сложные
дисахариды
полисахариды
Сахароза С12Н22О11
Лактоза С12Н22О11
Мальтоза С12Н22О11
Крахмал
Целлюлоза (С6Н5О10)n
Слайд 5
Классификация
По числу атомов углерода в молекуле:
Тетрозы (эритроза C4H8O4)
Пентозы (рибоза С5Н10О5)
Гексозы (глюкоза
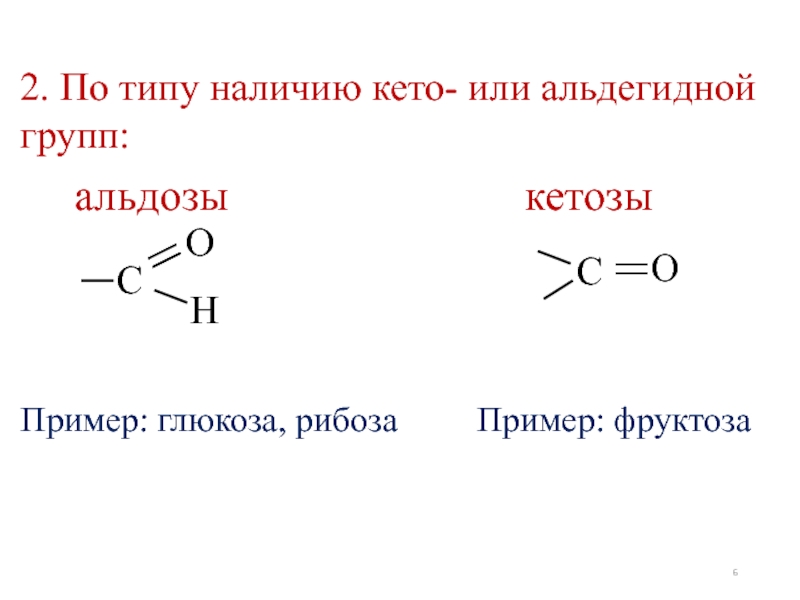
Слайд 62. По типу наличию кето- или альдегидной групп:
альдозы
С
=
О
кетозы
Пример: глюкоза, рибоза
С
=
О
Пример: фруктоза
Слайд 9Физические свойства
Бесцветные кристаллические вещества, сладкие на вкус, хорошо
Слайд 101. Восстановление (гидрирование)
Химические свойства
С
│
(СНОН)4
СН2ОН
│
+ Н2
→
kat, t0
Н
О
=
СН2ОН
СН2ОН
(СНОН)4
│
│
глюкоза
сорбит
Слайд 133. Реакция глюкозы с участием гидроксильных групп
а) взаимодействие с Cu(OH)2
Слайд 15Глюкоза является ценным питательным продуктом. В организме она подвергается сложным биохимическим
C6H12O6+6O2→6H2O+6CO2+2800 кДж
Слайд 16Получение
В промышленности
Гидролиз крахмала:
(C6H10O5)n + nH2O → nC6H12O6
крахмал глюкоза
t, H+
Слайд 23Физические свойства и нахождение в природе
1. Сахароза представляет собой бесцветные кристаллы
2. Температура плавления сахарозы 160 °C.
3. При застывании расплавленной сахарозы образуется аморфная прозрачная масса – карамель.
4. Содержится во многих растениях: в соке березы, клена, в моркови, дыне, а также в сахарной свекле и сахарном тростнике.
Слайд 24
Химические свойства дисахаридов
1. Наличие гидроксильных групп в молекуле сахарозы легко подтверждается
Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди (качественная реакция многоатомных спиртов).
Слайд 252. Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором
3. Сахароза, в отличие от глюкозы, не является альдегидом. Сахароза, находясь в растворе, не вступает в реакцию "серебряного зеркала", так как не способна превращаться в открытую форму, содержащую альдегидную группу. Подобные дисахариды не способны окисляться (т.е. быть восстановителями) и называются не восстанавливающими сахарами.
Слайд 264. Реакция сахарозы с водой
Важное химическое свойство сахарозы – способность подвергаться
С12Н22О11+Н2О →С6Н12O6 +С6Н12O6
t, Н2SО4
Слайд 29Физические свойства
Крахмал - белый аморфный порошок, не растворяется в холодной воде,
Целлюлоза - твердое волокнистое вещество, нерастворимое в воде
Слайд 30
Химические свойства крахмала
1. Гидролиз
2. Качественная реакция на крахмал
(С6Н10О5)n + I2
комплексное соединение
сине-фиолетового цвета
→
(С6Н10О5)n + nН2О→ nС6Н12О6
глюкоза
крахмал
Слайд 31
Химические свойства целлюлозы
1. Гидролиз
2. Образование сложных эфиров
(С6Н10О5)n + nН2О→ nС6Н12О6
целлюлоза
глюкоза
Слайд 32
4. Термическое разложение без доступа воздуха:
(С6Н10О5)n древесный уголь + Н2О + летучие органические вещества
t0
3. Горение
→
(С6Н10О5)n +6nО2→6nСО2 +5nН2О +Q