- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Типы химических реакций (8 класс)
Содержание
- 1. Презентация по химии на тему Типы химических реакций (8 класс)
- 2. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
- 3. Как классифицировать химические реакции?
- 4. Классификация реакцийпо тепловому эффекту экзотермическая реакция эндотермическая реакцияпо
- 5. Цель урокаИзучить классификацию химических реакций по числу и составу исходных веществ и продуктов реакции.
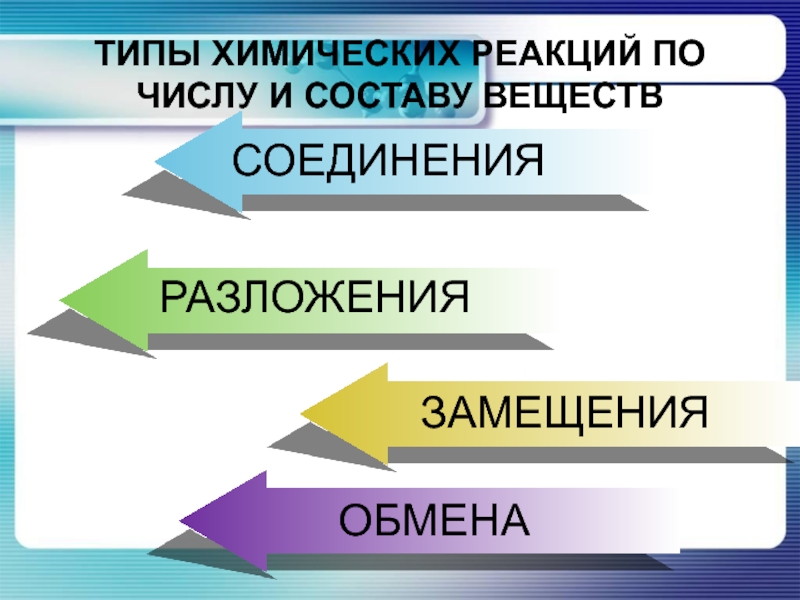
- 6. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ по числу и составу веществЗАМЕЩЕНИЯОБМЕНА
- 7. Перевёрнутый урок
- 8. Слайд 8
- 9. Взаимодействие железа с хлором
- 10. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
- 11. Реакции соединения:А + В = АВреакциями соединения
- 12. Оксид ртути (II)
- 13. Слайд 13
- 14. Реакции разложения: АВ = А
- 15. Реакция железа с сульфатом меди (II)
- 16. Цинк с соляной кислотой
- 17. Слайд 17
- 18. Реакции замещения:АВ + С = СВ + А
- 19. Фосфат натрия с нитратом серебра
- 20. Оксид меди (II) с серной кислотой
- 21. Слайд 21
- 22. Реакции обмена:АВ + СД = АД +
- 23. Типы реакций и их механизмы приведены в таблице:
- 24. Задания группам:
- 25. Проверьте свои знанияОпределите тип химической реакции. Распределите
- 26. Сравни и оцени2H2 + O2
- 27. РефлексияСделай выводПодумай, кого из одноклассников ты бы отметил за работу на уроке?
- 28. Домашнее задание §30 стр.111-113, вопросы №1,2,4 Шавандина Е.В.
- 29. Домашнее задание Задание на
- 30. Задание на «4». Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических реакций
- 31. Задание на «5». Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите типы химических реакций
- 32. Задание на «3» Расставьте коэффициенты в уравнениях химических реакций, укажите типы химических реакций.
- 33. Задание на «4» Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических реакций
- 34. Задание на «5» Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите типы химических реакций
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
Слайд 1урок по химии
Типы химических реакций
Автор: учитель химии МБОУ Зимовниковской СОШ №10
Сылка Алла Александровна
Слайд 4 Классификация реакций
по тепловому эффекту
экзотермическая реакция
эндотермическая реакция
по числу и составу исходных
веществ и продуктов реакции
реакция соединения
реакция разложения
реакция замещения
реакция обмена
реакция соединения
реакция разложения
реакция замещения
реакция обмена
Слайд 5Цель урока
Изучить классификацию химических реакций по числу и составу исходных веществ
и продуктов реакции.
Слайд 11Реакции соединения:
А + В = АВ
реакциями соединения называют реакции, в которых
из двух простых или сложных веществ образуется одно более сложное вещество.
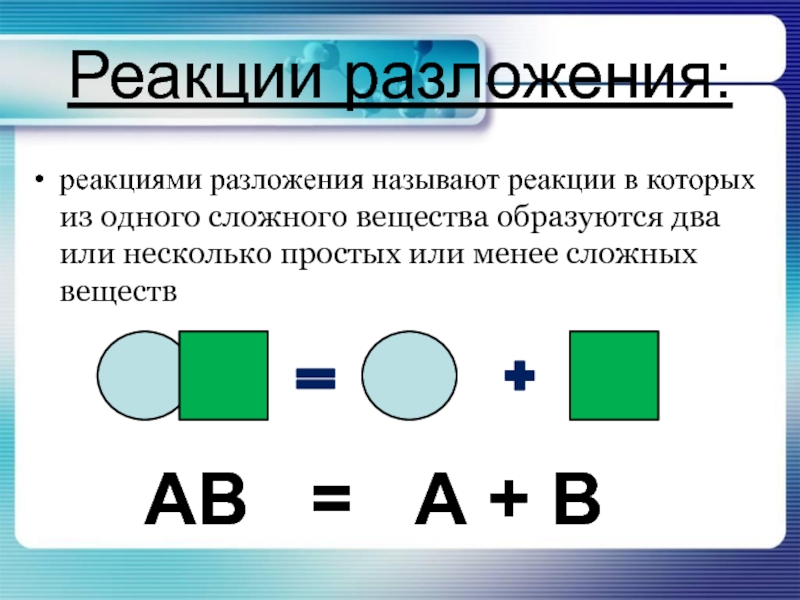
Слайд 14Реакции разложения:
АВ = А + В
реакциями разложения
называют реакции в которых из одного сложного вещества образуются два или несколько простых или менее сложных веществ
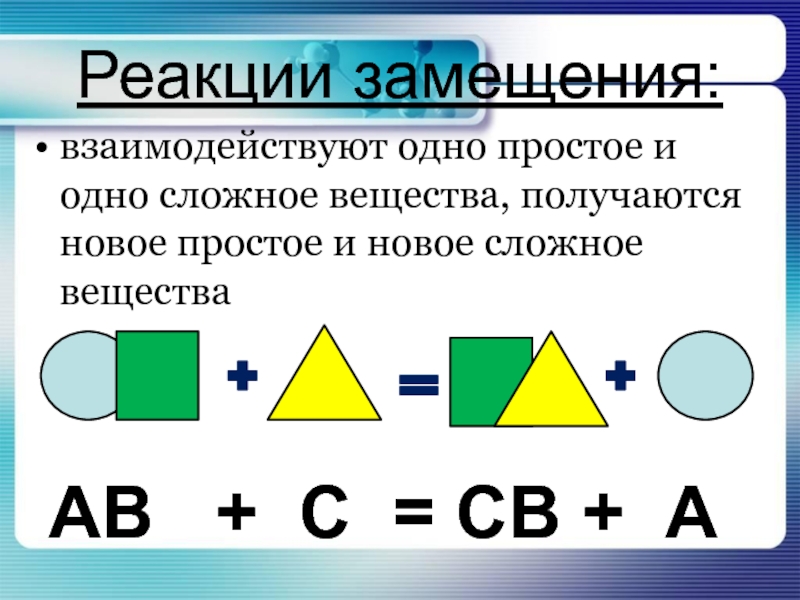
Слайд 18Реакции замещения:
АВ + С = СВ + А
взаимодействуют одно простое и
одно сложное вещества, получаются новое простое и новое сложное вещества
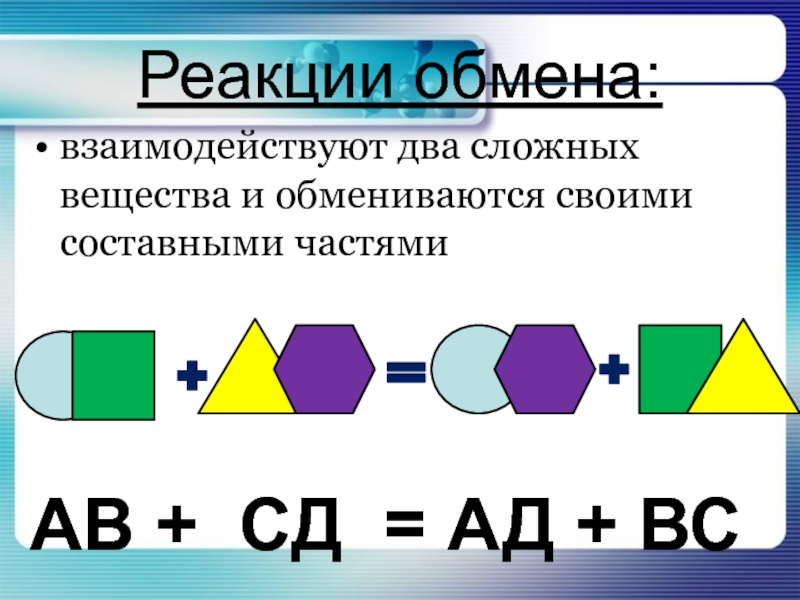
Слайд 22Реакции обмена:
АВ + СД = АД + ВС
взаимодействуют два сложных
вещества и обмениваются своими составными частями
Слайд 24 Задания группам:
Внимательно прочитайте
инструктивную карточку по проведению опыта.
Соблюдая технику безопасности проведите химическую реакцию.
Запишите ваши наблюдения, уравнение реакции, определите тип реакции.
Подготовьте отчет своей группы.
Соблюдая технику безопасности проведите химическую реакцию.
Запишите ваши наблюдения, уравнение реакции, определите тип реакции.
Подготовьте отчет своей группы.
Слайд 25Проверьте свои знания
Определите тип химической реакции.
Распределите предложенные вам уравнения, расставьте
коэффициенты в уравнениях реакций.
H2 + O2 = H2O
NaOH + H3PO4 = Na3PO4 + H2O
Fe(OH)3 = Fe2O3 + H2O
P2O5 + H2O = H3PO4
Mg(OH)2 + HNO3 = Mg(NO3)2 + H2O
Ca + H2O = Ca(OH)2 + H2
CaCO3 = CaO + CO2
Fe + HCl = FeCl2 + H2
H2 + O2 = H2O
NaOH + H3PO4 = Na3PO4 + H2O
Fe(OH)3 = Fe2O3 + H2O
P2O5 + H2O = H3PO4
Mg(OH)2 + HNO3 = Mg(NO3)2 + H2O
Ca + H2O = Ca(OH)2 + H2
CaCO3 = CaO + CO2
Fe + HCl = FeCl2 + H2
Слайд 26 Сравни и оцени
2H2 + O2 = 2H2O
3NaOH + H3PO4
= Na3PO4 + 3H2O
2Fe(OH)3 = Fe2O3 +3H2O
P2O5 + 3H2O = 2H3PO4
Mg(OH)2 + 2HNO3 = Mg(NO3)2 + 2H2O
Ca + 2H2O = Ca(OH)2 + H2
CaCO3 = CaO + CO2
Fe +2HCl = FeCl2 + H2
2Fe(OH)3 = Fe2O3 +3H2O
P2O5 + 3H2O = 2H3PO4
Mg(OH)2 + 2HNO3 = Mg(NO3)2 + 2H2O
Ca + 2H2O = Ca(OH)2 + H2
CaCO3 = CaO + CO2
Fe +2HCl = FeCl2 + H2
0 ошибок - «5» 1-2 ошибки – «4» 3-4 ошибки – «3» 5 и более – «2»
Слайд 29 Домашнее задание Задание на «3». Расставьте коэффициенты в уравнениях химических реакций, укажите
типы химических реакций.
Слайд 30Задание на «4». Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических
реакций
Слайд 31Задание на «5». Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите
типы химических реакций
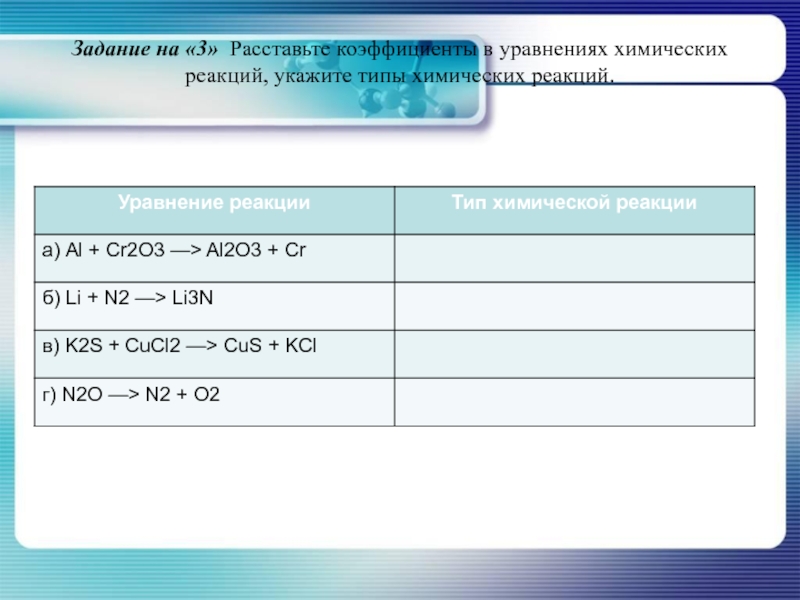
Слайд 32Задание на «3» Расставьте коэффициенты в уравнениях химических реакций, укажите типы
химических реакций.
Слайд 33Задание на «4» Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических
реакций
Слайд 34Задание на «5» Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите
типы химических реакций