- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Типы химических реакций
Содержание
- 1. Презентация по химии на тему: Типы химических реакций
- 2. Реакции соединения Реакции обмена Реакции разложения Химические реакции
- 3. Слайд 3
- 4. Запишите уравнения реакций разложения, схемы которых:Fe(OH)3 →
- 5. Слайд 5
- 6. Запишите уравнения реакций соединения, схемы которых:
- 7. Слайд 7
- 8. Запишите уравнения следующих реакций замещения:Cu + AgNO3
- 9. Запишите уравнения следующих реакций замещения:CuCl2 + Al →PbO2 + C →FeBr3 + Cl2 →
- 10. Запишите уравнения следующих реакций замещения:а) оксид железа(III)
- 11. Запишите уравнения следующих реакций замещенияг) оксид свинца(IV)
- 12. Слайд 12
- 13. Условия протекания реакций обмена в растворах до
- 14. Какие из реакций обмена, схемы которых даны,
- 15. Какие из реакций обмена, схемы которых даны,
Слайд 3
2HgO → 2Hg + O2 ↑
2H2O→ 2H2↑ + O2↑
Cu(OH)2 → CuO + Н2О
2KMnO4 → KMnO4 + MnO2 + O2 ↑
Реакции разложения-
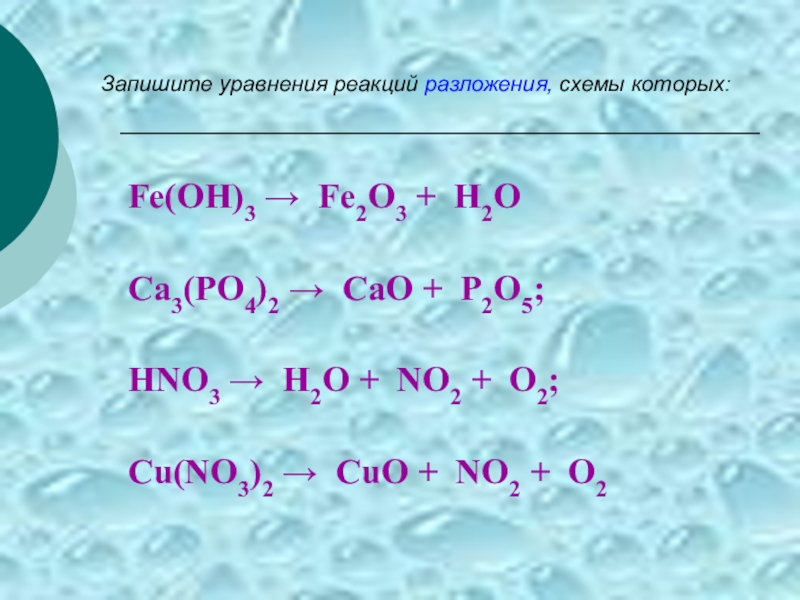
Слайд 4Запишите уравнения реакций разложения, схемы которых:
Fe(OH)3 → Fe2O3 + H2O
Ca3(PO4)2 →
HNO3 → H2O + NO2 + O2;
Cu(NO3)2 → CuO + NO2 + O2
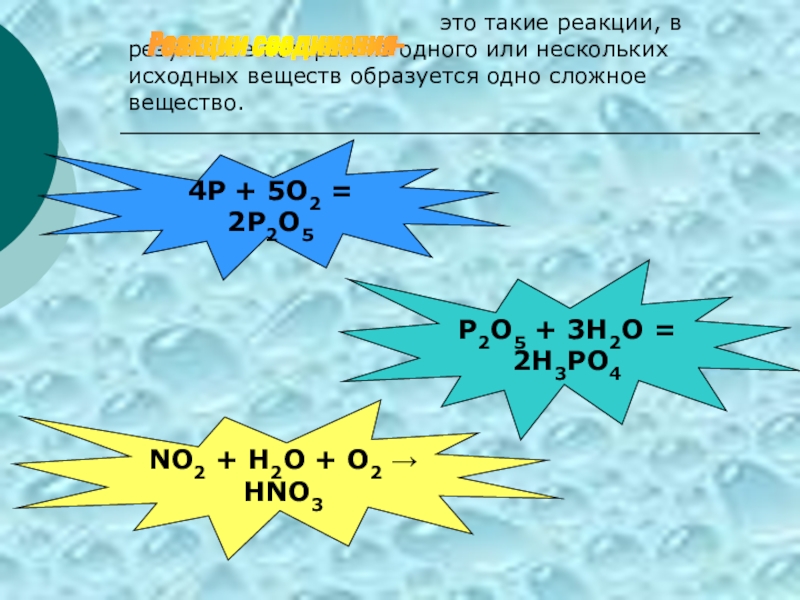
Слайд 5
4P + 5O2 = 2P2O5
P2O5 + 3H2O = 2H3PO4
NO2 + H2O + O2 → HNO3
Реакции соединения-
Слайд 7
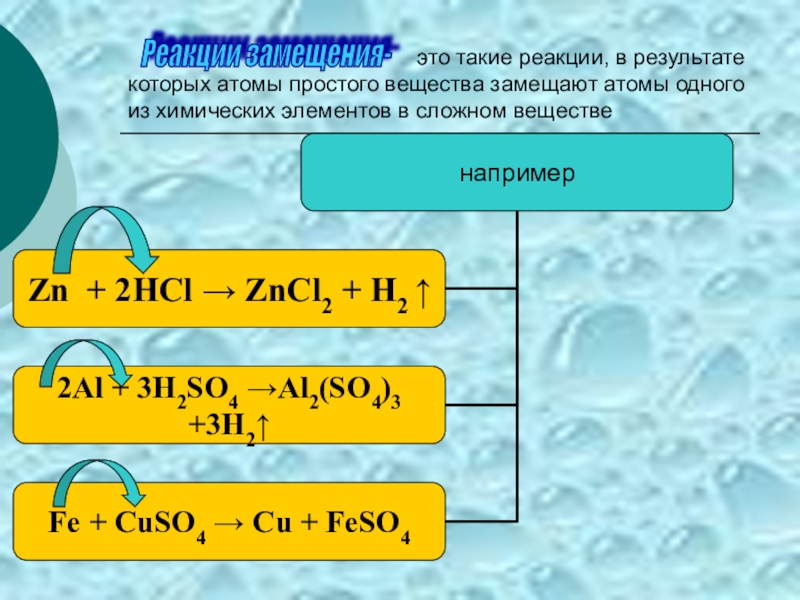
Реакции замещения-
Слайд 8Запишите уравнения следующих реакций замещения:
Cu + AgNO3 → Cu(NO3)2 + Ag
Fe2O3
Fe2O3 + H2 →
Слайд 10Запишите уравнения следующих реакций замещения:
а) оксид железа(III) + алюминий →
б) оксид
в) хлорид меди(II) + алюминий →
Слайд 11Запишите уравнения следующих реакций замещения
г) оксид свинца(IV) + углерод →
д) бромид
е)магний + хлорид меди(II) →
Слайд 12
Реакции обмена между кислотами и щелочами называют
NaOH + HCl →NaCl + H2O
Реакции обмена
реакциями нейтрализации
щелочь + кислота → соль + вода
Слайд 13Условия протекания реакций обмена в растворах до конца
Na2CO3 + 2HCl →
BaCl2 + K2SO4 → 2KCl + BaSO4↓
Реакции обмена, протекающие в растворах,
идут до конца только в том случае,
если в результате их образуется
осадок, газ или вода.
Слайд 14Какие из реакций обмена, схемы которых даны, будут протекать до конца?
а)
б) Cu(NO3)2 + NaCl →
в) Pb(NO3)2 + K2S →
Слайд 15Какие из реакций обмена, схемы которых даны, будут протекать до конца?
г)MgCl2
д)HNO3 + ZnSO4 →
е)Ca(NO3)2 + H3PO4 →
ж)Ba(NO3)2 + Na2SO4 →