- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Свойства кислорода
Содержание
- 1. Презентация по химии на тему Свойства кислорода
- 2. Цель урока
- 3. Умения:
- 4. Повторение материалаКакие физические свойства у Кислорода?Дать характеристику
- 5. Способность веществ
- 6. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОРОДАВзаимодействие веществ с кислородом
- 7. Реакции окисления реакции
- 8. Кислород – сильный окислитель.С кислородом реагируют все
- 9. ЗАДАНИЕ № 1Вставь вместо «?» необходимую формулу
- 10. ОТВЕТЫ К ЗАДАНИЮ № 1Вставь вместо «?»
- 11. НАХОЖДЕНИЕ КИСЛОРОДА В ПРИРОДЕОн всюду и везде:В
- 12. КРУГОВОРОТ КИСЛОРОДАРастения, поглощая атмосферный кислород в темное
- 13. Находит широкое применение в медицине и промышленности.При
- 14. Слайд 14
Слайд 4Повторение материала
Какие физические свойства у Кислорода?
Дать характеристику элемента по ПС (порядковый
Слайд 5 Способность веществ превращаться в другие под
Химические свойства
Определение
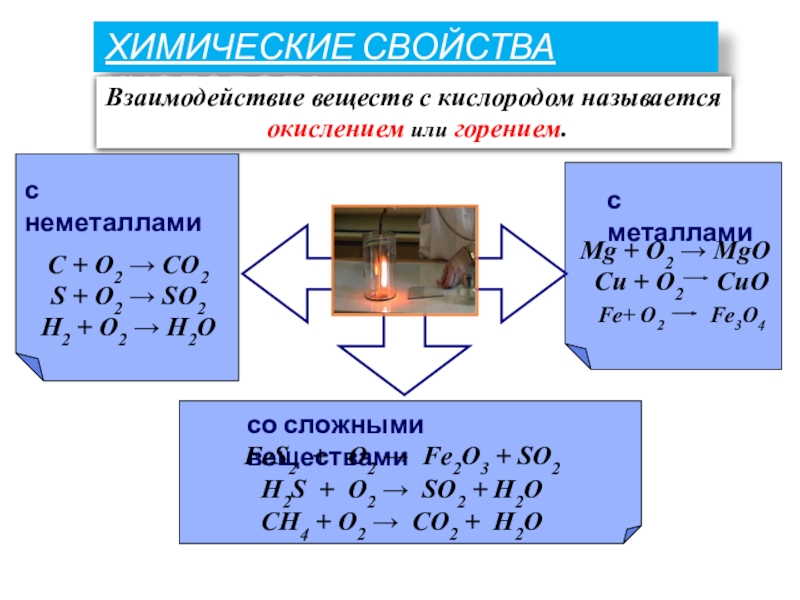
Слайд 6 ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОРОДА
Взаимодействие веществ с кислородом называется
окислением или горением.
с
с металлами
C + O2 CO2
S + O2 SO2
H2 + O2 H2O
Mg + O2 MgO
Cu + O2 CuO
Fe+ O2 Fe3O4
со сложными веществами
FeS2 + O2 Fe2O3 + SO2
H2S + O2 SO2 + H2O
CH4 + O2 CO2 + H2O
Слайд 7Реакции окисления
реакции взаимодействия веществ с кислородом
Определение
Горение фосфора
Горение серы
Горение угля
Горение железа
Горение метана
Слайд 8Кислород – сильный окислитель.
С кислородом реагируют все элементы, кроме Au, Pt,
В результате взаимодействия веществ с кислородом образуется оксиды.
Оксиды – сложные вещества, которые состоят из двух элементов, одним из которых является кислород.
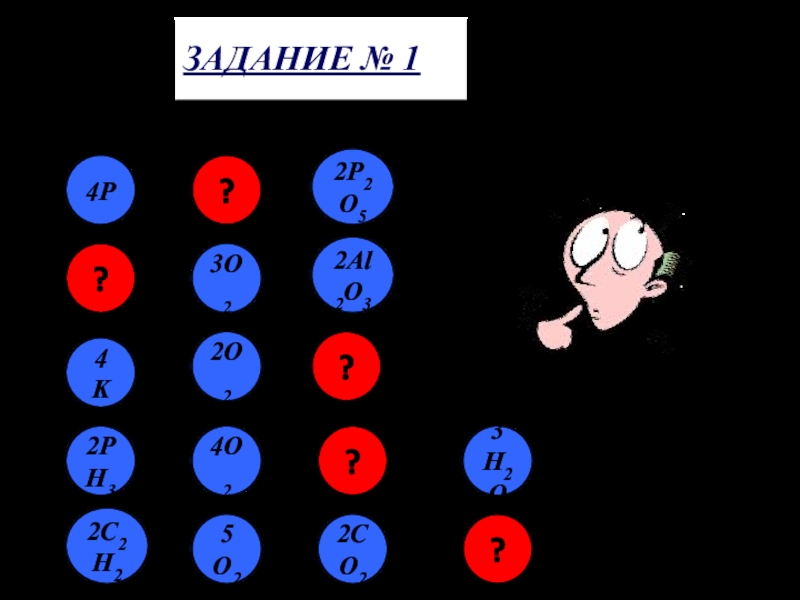
Слайд 9ЗАДАНИЕ № 1
Вставь вместо «?» необходимую формулу с коэффициентом.
?
2P2O5
?
4P
2Al2O3
3O2
2C2H2
2CO2
5 O2
3H2O
2PH3
4O2
2O2
?
4 K
А)
Б) + =
В) + =
Г) + = +
Д) + = +
?
?
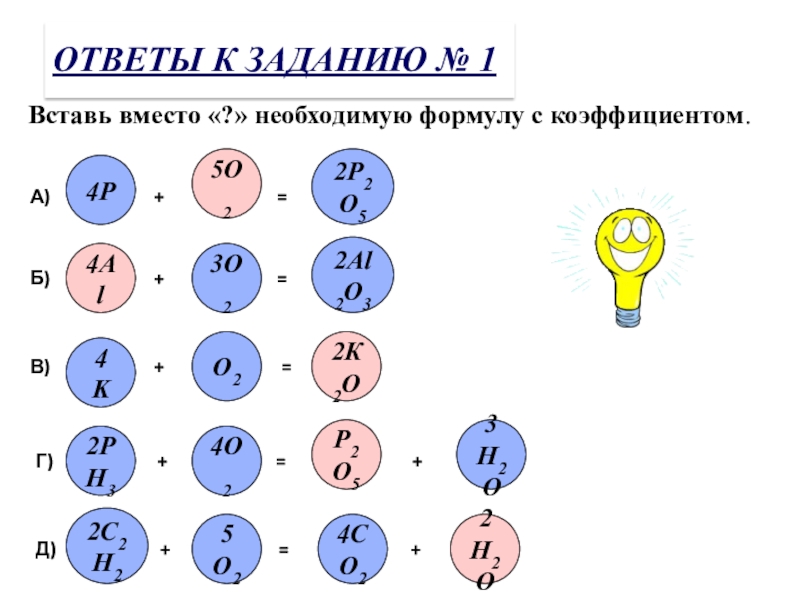
Слайд 10ОТВЕТЫ К ЗАДАНИЮ № 1
Вставь вместо «?» необходимую формулу с коэффициентом.
4Al
2P2O5
5O2
4P
2Al2O3
3O2
2C2H2
4CO2
5
3H2O
2PH3
4O2
O2
2К2О
4 K
А) + =
Б) + =
В) + =
Г) + = +
Д) + = +
2Н2О
Р2О5
Слайд 11НАХОЖДЕНИЕ КИСЛОРОДА В ПРИРОДЕ
Он всюду и везде:
В камне, в воздухе, в
Он и в утренней росе,
И в небес голубизне.
Литосфера - 47% по m (в составе оксидов, солей)
Гидросфера - 85,8% (в основном в составе воды)
Атмосфера - 23% по m, 21% по V
Растения - 40%
Животные - 20%
Тело человека - 65%
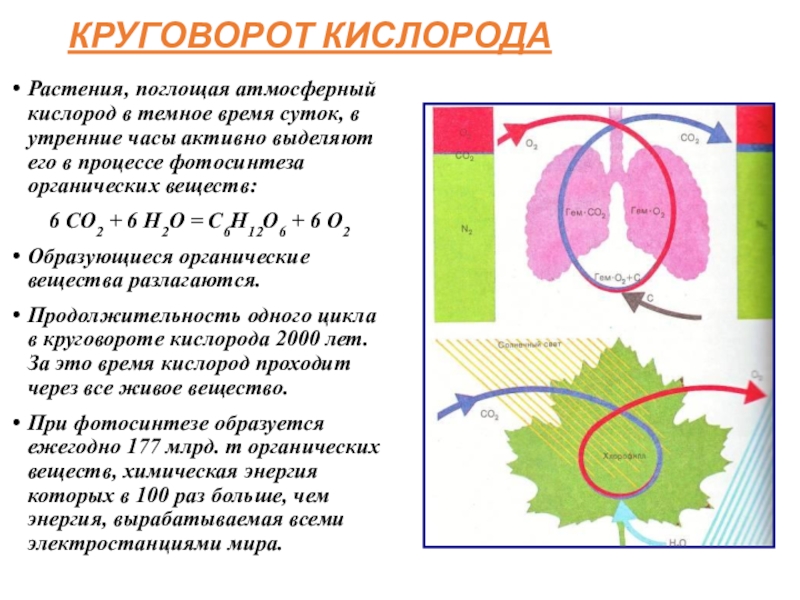
Слайд 12КРУГОВОРОТ КИСЛОРОДА
Растения, поглощая атмосферный кислород в темное время суток, в утренние
6 CO2 + 6 H2O = C6H12O6 + 6 O2
Образующиеся органические вещества разлагаются.
Продолжительность одного цикла в круговороте кислорода 2000 лет. За это время кислород проходит через все живое вещество.
При фотосинтезе образуется ежегодно 177 млрд. т органических веществ, химическая энергия которых в 100 раз больше, чем энергия, вырабатываемая всеми электростанциями мира.
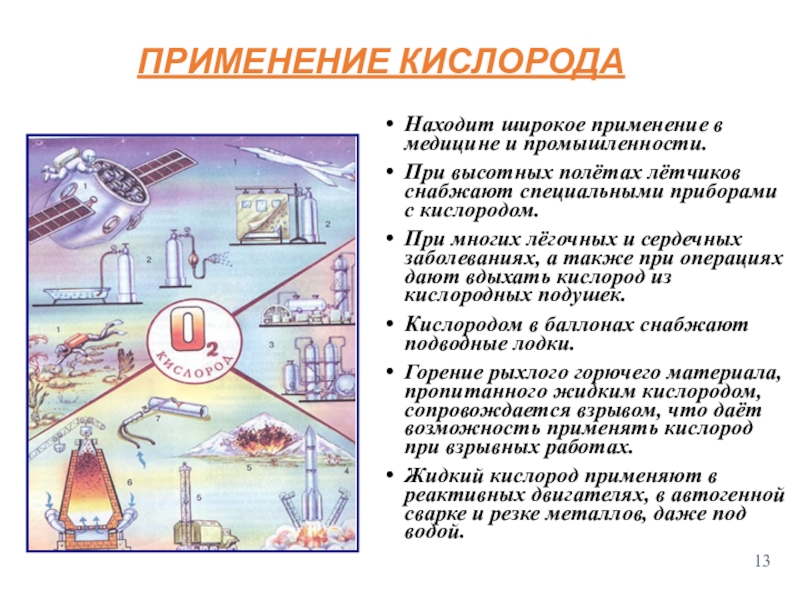
Слайд 13Находит широкое применение в медицине и промышленности.
При высотных полётах лётчиков снабжают
При многих лёгочных и сердечных заболеваниях, а также при операциях дают вдыхать кислород из кислородных подушек.
Кислородом в баллонах снабжают подводные лодки.
Горение рыхлого горючего материала, пропитанного жидким кислородом, сопровождается взрывом, что даёт возможность применять кислород при взрывных работах.
Жидкий кислород применяют в реактивных двигателях, в автогенной сварке и резке металлов, даже под водой.
ПРИМЕНЕНИЕ КИСЛОРОДА