- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Соли (8 класс)
Содержание
- 1. Презентация по химии на тему Соли (8 класс)
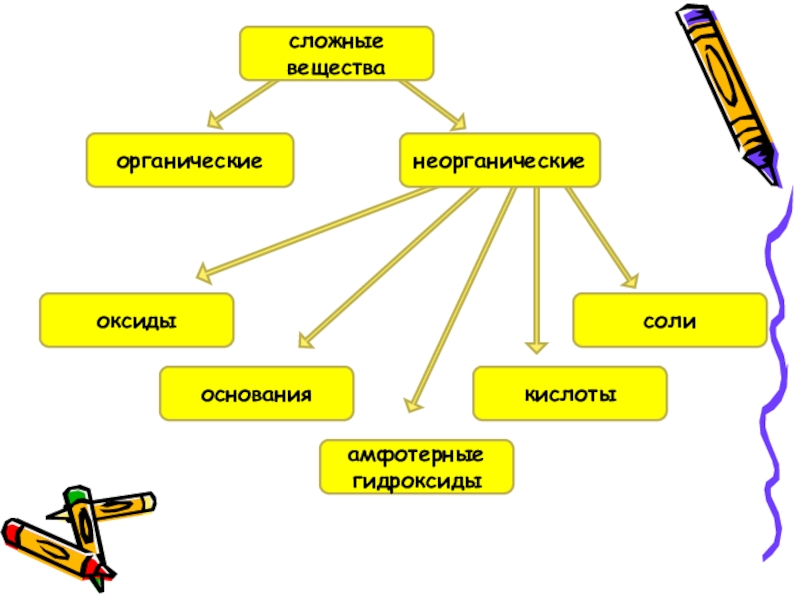
- 2. органическиеоснованиякислотыамфотерные гидроксидысолиоксидынеорганическиесложные вещества
- 3. СОЛИ - это сложные вещества, молекулы
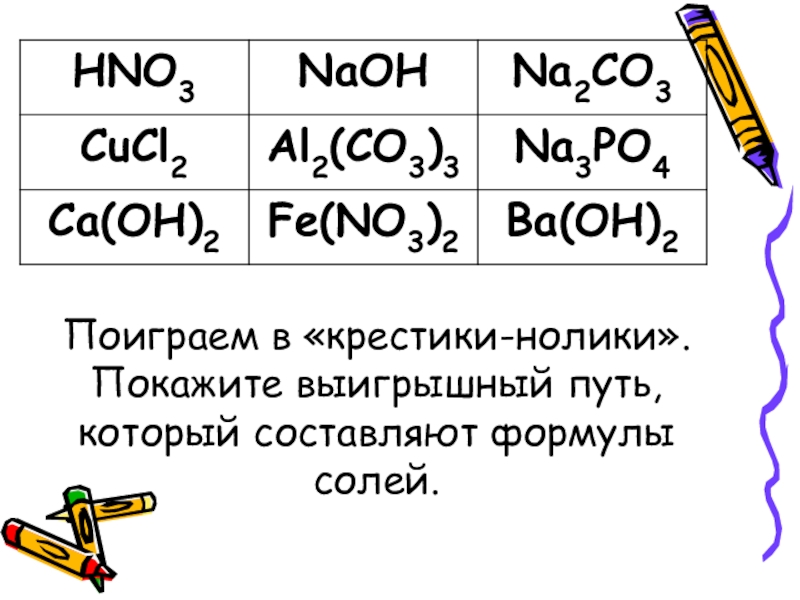
- 4. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы солей.
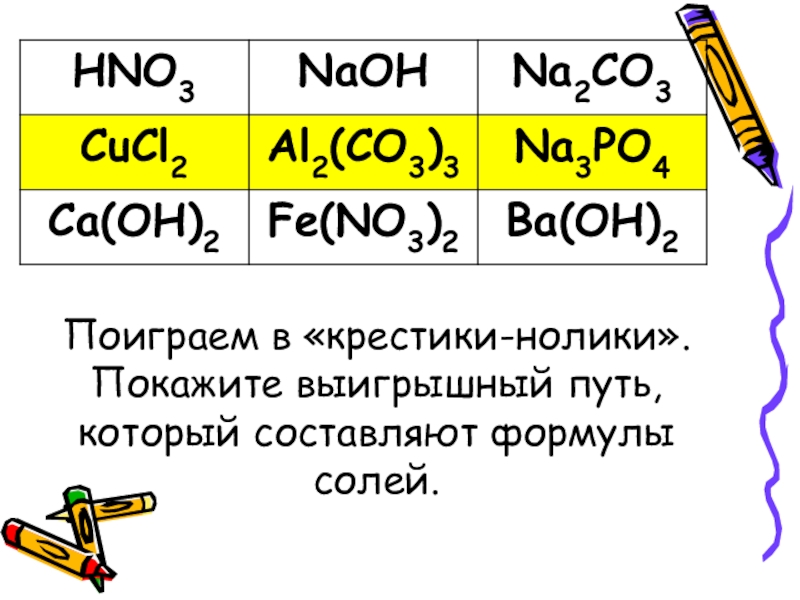
- 5. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы солей.
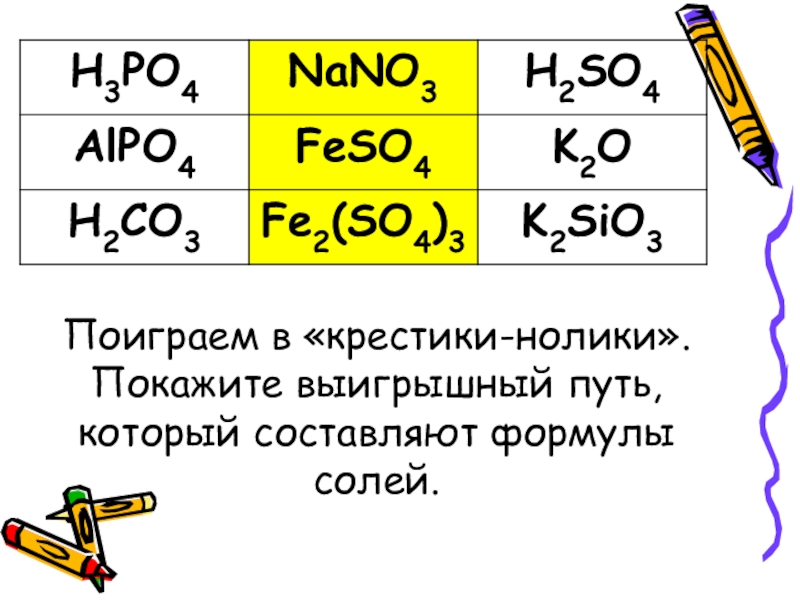
- 6. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы солей.
- 7. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы солей.
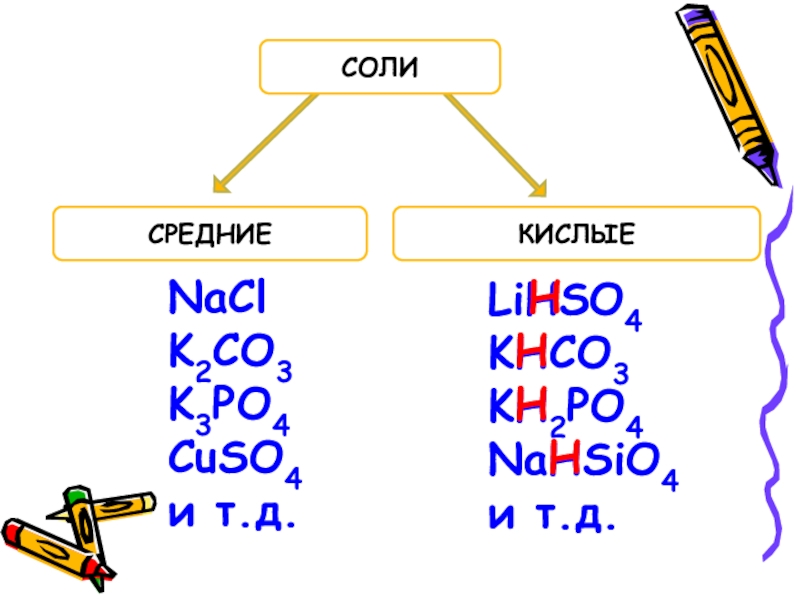
- 8. СРЕДНИЕКИСЛЫЕСОЛИNaClK2CO3K3PO4CuSO4 и т.д.LiHSO4 KHCO3KH2PO4NaHSiO4 и т.д.HHHH
- 9. НОМЕНКЛАТУРА (НАЗВАНИЯ) СРЕДНИХ СОЛЕЙ БЕСКИСЛОРОДНЫХ КИСЛОТKCl –
- 10. НОМЕНКЛАТУРА (НАЗВАНИЯ) СРЕДНИХ СОЛЕЙ КИСЛОРОДСОДЕРЖАЩИХ КИСЛОТK2SO4 –
- 11. НОМЕНКЛАТУРА (НАЗВАНИЯ) КИСЛЫХ СОЛЕЙK2CO3KHCO3Li2SO4LiHSO4K3PO4KH2PO4 – карбонат калия
- 12. СОЛИ
- 13. --------
- 14. Составьте формулы солей по названиям:хлорид натриянитрат меди(II)фосфат кальциякарбонат калиясиликат натриясульфат алюминия
- 15. Определите заряды ионов, степени окисления элементов в кислотах, запишите формулы соответствующих им оксидов.
- 16. ЗАДАЧА 1. Вычислите, какое количество вещества составляет
- 17. ЗАДАЧА 2. Определите массу хлороводорода HCl, который
- 18. Слайд 18
- 19. Домашнее задание§27, упр.1-4 (новый). §29,упр.1-4 (старый).
- 20. Спасибо за внимание!
органическиеоснованиякислотыамфотерные гидроксидысолиоксидынеорганическиесложные вещества
Слайд 3
СОЛИ - это сложные вещества, молекулы которых состоят из ионов
металла и кислотного остатка
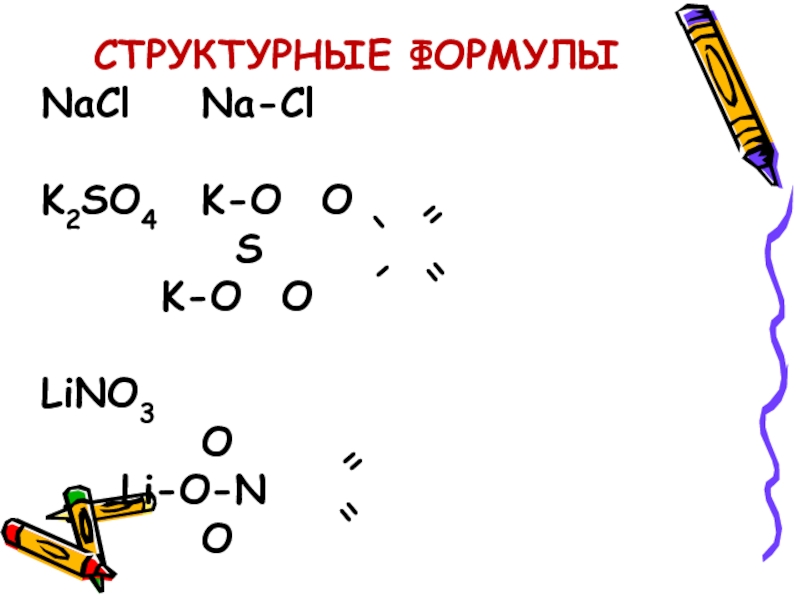
Na Cl
Li2 SO4
K3 PO4
Na Cl
Li2 SO4
K3 PO4
Cl-
SO42-
PO4 3-
кислотные остатки
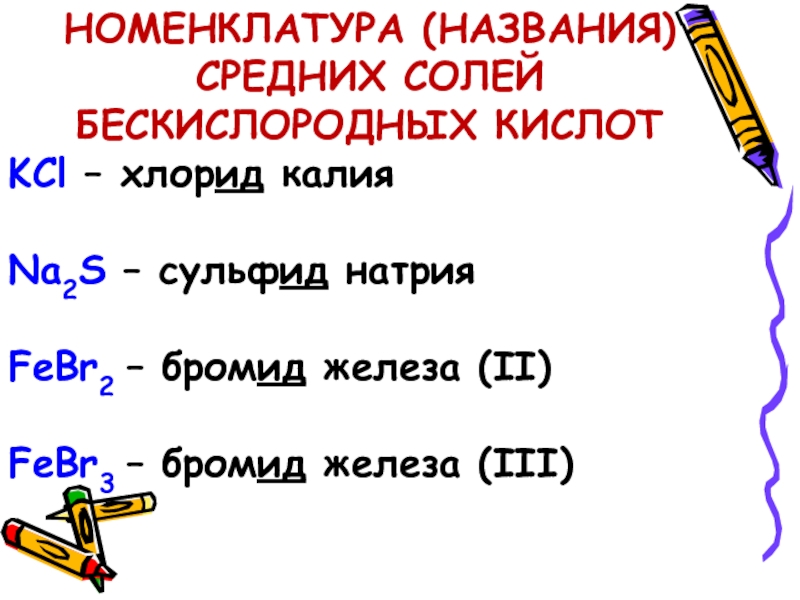
Слайд 9НОМЕНКЛАТУРА (НАЗВАНИЯ) СРЕДНИХ СОЛЕЙ БЕСКИСЛОРОДНЫХ КИСЛОТ
KCl – хлорид калия
Na2S – сульфид
натрия
FeBr2 – бромид железа (II)
FeBr3 – бромид железа (III)
FeBr2 – бромид железа (II)
FeBr3 – бромид железа (III)
Слайд 10НОМЕНКЛАТУРА (НАЗВАНИЯ) СРЕДНИХ СОЛЕЙ КИСЛОРОДСОДЕРЖАЩИХ КИСЛОТ
K2SO4 –
K2SO3 –
NaNO3 –
NaNO2 –
сульфат калия
сульфит калия
нитрат натрия
нитрит натрия
Слайд 11НОМЕНКЛАТУРА (НАЗВАНИЯ) КИСЛЫХ СОЛЕЙ
K2CO3
KHCO3
Li2SO4
LiHSO4
K3PO4
KH2PO4
– карбонат калия
– сульфат лития
– ортофосфат калия
– гидрокарбонат калия
– гидросульфат лития
– гидрофосфат калия
Слайд 14Составьте формулы солей по названиям:
хлорид натрия
нитрат меди(II)
фосфат кальция
карбонат калия
силикат натрия
сульфат алюминия
Слайд 15Определите заряды ионов, степени окисления элементов в кислотах, запишите формулы соответствующих
им оксидов.
Слайд 16ЗАДАЧА 1.
Вычислите, какое количество вещества составляет 490 г фосфорной кислоты. Рассчитайте
число атомов водорода, которое будет содержаться в этой порции кислоты.
Слайд 17ЗАДАЧА 2.
Определите массу хлороводорода HCl, который содержит столько же молекул, сколько
их заключено в 360 г воды.