- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Серная кислота и её свойства.
Содержание
- 1. Презентация по химии на тему Серная кислота и её свойства.
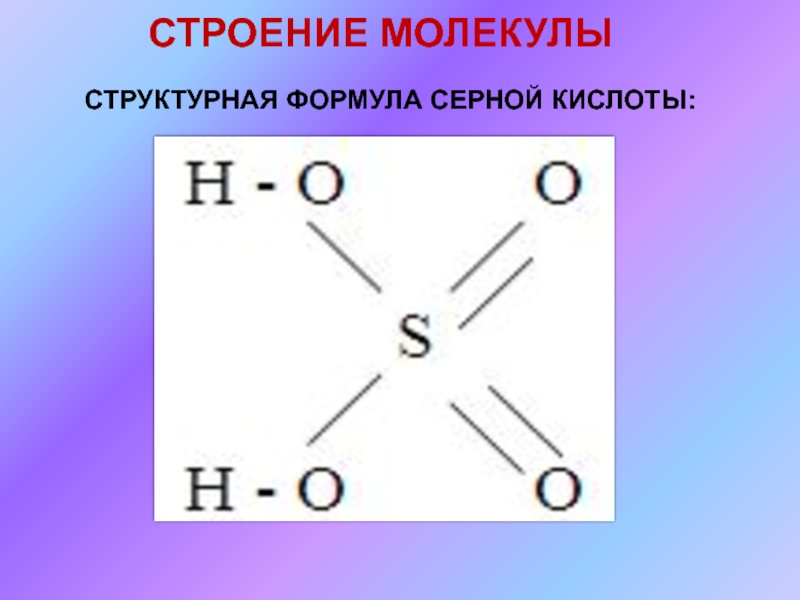
- 2. СТРОЕНИЕ МОЛЕКУЛЫСТРУКТУРНАЯ ФОРМУЛА СЕРНОЙ КИСЛОТЫ:
- 3. ПОЛУЧЕНИЕСерную кислоту в промышленности получают из серы
- 4. ФИЗИЧЕСКИЕ СВОЙСТВАСЕРНАЯ КИСЛОТА бесцветная, тяжёлая, нелетучая
- 5. ХИМИЧЕСКИЕ СВОЙСТВАРазбавленная кислота обладает общими свойствами, характерными для всех кислот.1) Водный раствор изменяет окраску индикаторов
- 6. ХИМИЧЕСКИЕ СВОЙСТВА2) Разбавленная серная кислота реагирует с металлами:Zn + H2SO4 → ZnSO4 + H2↑
- 7. ХИМИЧЕСКИЕ СВОЙСТВА3) Реагирует с оксидами металлов:H2SO4 + MgO → MgSO4 + H2O
- 8. ХИМИЧЕСКИЕ СВОЙСТВА4) Реагирует с основаниями (реакция нейтрализации):H2SO4 + 2NaOH → Na2SO4 + 2H2O
- 9. ХИМИЧЕСКИЕ СВОЙСТВА5) Реагирует с солями, вытесняя из них другие кислоты:3H2SO4 + Ca3(PO4)2→ 3CaSO4 + 2H3PO4
- 10. СПЕЦИФИЧЕСКИЕ СВОЙСТВА1) Концентрированная серная кислота – сильный
- 11. СПЕЦИФИЧЕСКИЕ СВОЙСТВА2) Качественная реакция на серную кислоту
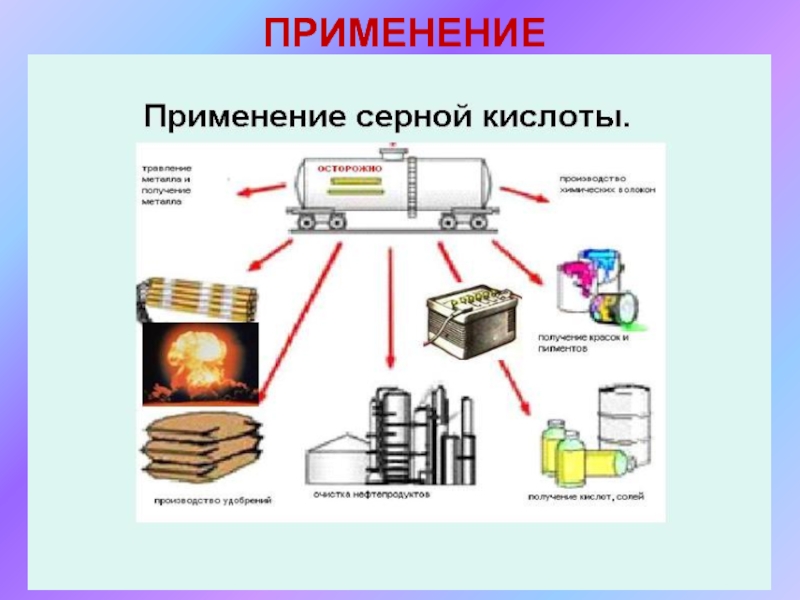
- 12. ПРИМЕНЕНИЕ
- 13. СОЛИ СЕРНОЙ КИСЛОТЫСЕРНАЯ КИСЛОТА ОБРАЗУЕТ ДВА РЯДА
- 14. ЛИТЕРАТУРА.Г.Е. Рудзитис, Ф.Г. Фельдман «Химия, 9 класс».О.С. Габриелян «Химия, 9 класс».Интернет ресурсы.
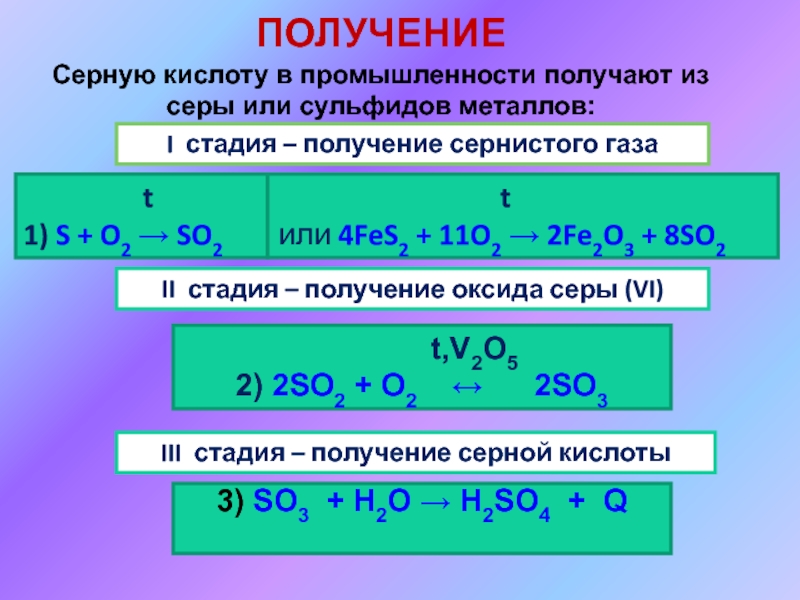
Слайд 3ПОЛУЧЕНИЕ
Серную кислоту в промышленности получают из серы или сульфидов металлов:
1) S + O2 → SO2
3) SO3 + H2O → H2SO4 + Q
t
или 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
I стадия – получение сернистого газа
II стадия – получение оксида серы (VI)
III стадия – получение серной кислоты
t,V2O5
2) 2SO2 + O2 ↔ 2SO3
Слайд 4ФИЗИЧЕСКИЕ СВОЙСТВА
СЕРНАЯ КИСЛОТА бесцветная, тяжёлая, нелетучая жидкость. При растворении её
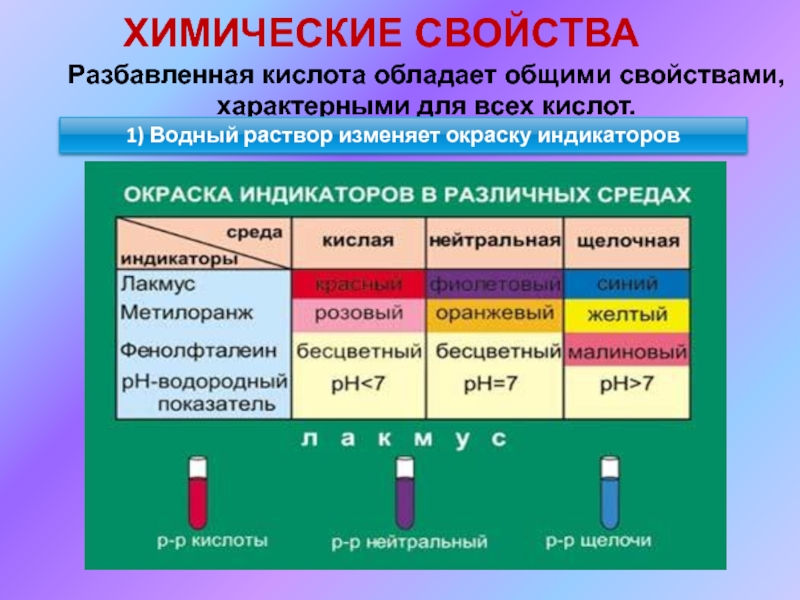
Слайд 5ХИМИЧЕСКИЕ СВОЙСТВА
Разбавленная кислота обладает общими свойствами, характерными для всех кислот.
1) Водный
Слайд 6ХИМИЧЕСКИЕ СВОЙСТВА
2) Разбавленная серная кислота реагирует с металлами:
Zn + H2SO4 →
Слайд 8ХИМИЧЕСКИЕ СВОЙСТВА
4) Реагирует с основаниями (реакция нейтрализации):
H2SO4 + 2NaOH → Na2SO4
Слайд 9ХИМИЧЕСКИЕ СВОЙСТВА
5) Реагирует с солями, вытесняя из них другие кислоты:
3H2SO4 +
Слайд 10СПЕЦИФИЧЕСКИЕ СВОЙСТВА
1) Концентрированная серная кислота – сильный окислитель: при нагревании она
t
Cu + 2H2SO4(конц) →
СuSO4 + SO2↑+ 2H2O
Слайд 11СПЕЦИФИЧЕСКИЕ СВОЙСТВА
2) Качественная реакция на серную кислоту и её соли- взаимодействие
H2SO4 + BaCl2 → BaSO4↓ + 2HCl
Слайд 13СОЛИ СЕРНОЙ КИСЛОТЫ
СЕРНАЯ КИСЛОТА ОБРАЗУЕТ ДВА РЯДА СОЛЕЙ – СРЕДНИЕ (СУЛЬФАТЫ)
МЕДНЫЙ КУПОРОС - СuSO4 ∙ 5H2O – используют для борьбы с вредителями и болезнями растений.
ГЛАУБЕРОВА СОЛЬ - Na2SO4 ∙ 10H2O – применяют в производстве стекла, соды, в медицине и ветеринарии.
ГИПС - СaSO4 ∙ 2H2O – применяют для получения полуводного гипса, необходимого в строительстве, а в медицине – для накладывания гипсовых повязок.