- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Серная кислота
Содержание
- 1. Презентация по химии на тему Серная кислота
- 2. Актуализация знанийИзвестно, что серная кислота сильный окислитель,
- 3. Классификация
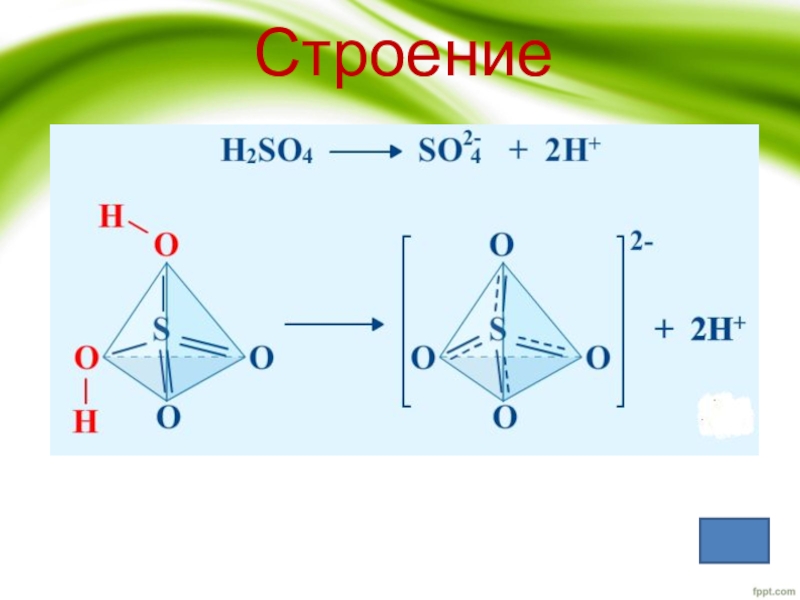
- 4. Строение
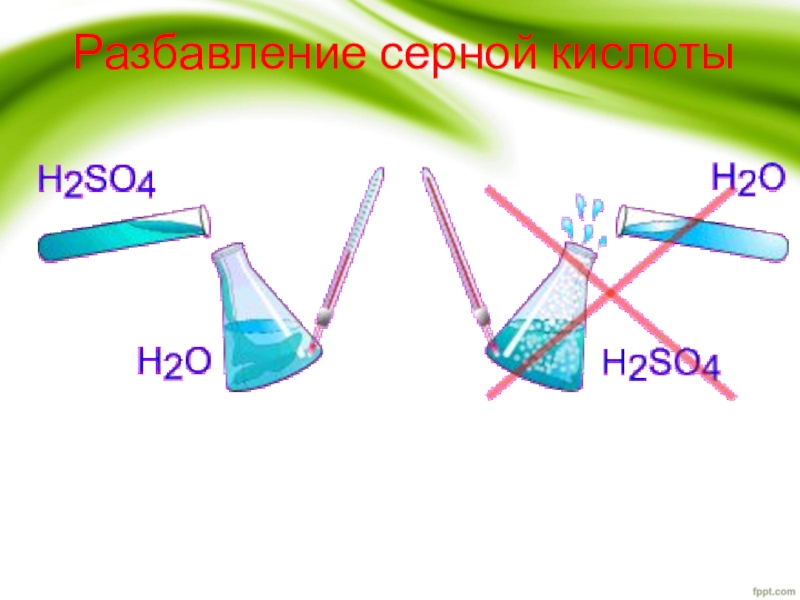
- 5. Разбавление серной кислоты
- 6. FeS2SH2SSO2 → SO3 → H2SO4 ПиритСерный колчедан Получение серной кислоты
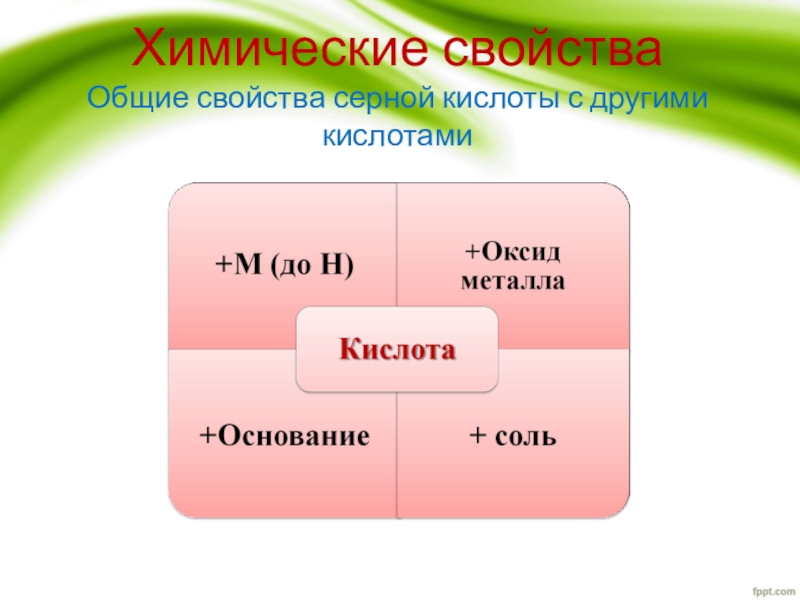
- 7. Химические свойства Общие свойства серной кислоты с другими кислотами
- 8. Химические свойстваДиссоциация:1 ступень H2SO4 2 ступень HSO4 Действие на индикаторы:Лакмус – Фенолфталеин –Метиловый оранжевый -
- 9. Химические свойстваВзаимодействие разбавленной серной кислоты с металлами:Zn + H2SO4 = Cu + H2SO4 =
- 10. Химические свойстваВзаимодействие разбавленной серной кислоты с металлами:CuO + H2SO4 =
- 11. Химические свойстваВзаимодействие разбавленной серной кислоты с солями:BaCl2 + H2SO4 =
- 12. Химические свойстваВзаимодействие разбавленной серной кислоты с основаниями:NaOH + H2SO4 =
- 13. Химические свойства Взаимодействие с металлами:Zn + H2SO4 (конц.) = Специфические свойства концентрированной серной кислоты
- 14. Химические свойстваОбугливание органических веществ: C6H12O6 + H2SO4 (конц.) = Специфические свойства концентрированной серной кислоты
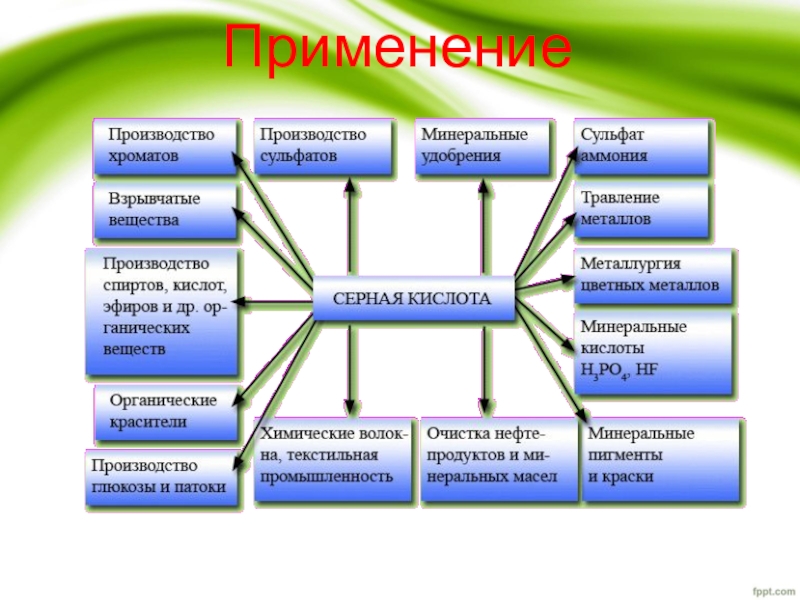
- 15. Применение
- 16. Закрепление Осуществите цепочку превращений:NaOH → Na2SO4 → BaSO4
Актуализация знанийИзвестно, что серная кислота сильный окислитель, значит сера в серной кислоте проявляет максимальную степень окисления, равную номеру группы, в которой она находится, т.е. +6. Как же это может быть, если на её внешнем энергетическом уровне
Слайд 2Актуализация знаний
Известно, что серная кислота сильный окислитель, значит сера в серной
кислоте проявляет максимальную степень окисления, равную номеру группы, в которой она находится, т.е. +6. Как же это может быть, если на её внешнем энергетическом уровне всего 2 неспаренных электрона. Схему строения атома серы я прилагаю к письму :
Слайд 8Химические свойства
Диссоциация:
1 ступень H2SO4
2 ступень HSO4
Действие на индикаторы:
Лакмус –
Фенолфталеин –
Метиловый оранжевый -
Слайд 9Химические свойства
Взаимодействие разбавленной серной кислоты с металлами:
Zn + H2SO4 =
Cu
+ H2SO4 =
Слайд 13
Химические свойства
Взаимодействие с металлами:
Zn + H2SO4 (конц.) =
Специфические свойства концентрированной
серной кислоты
Слайд 14Химические свойства
Обугливание органических веществ:
C6H12O6 + H2SO4 (конц.) =
Специфические свойства
концентрированной серной кислоты