свет,
По числу семи планет:
Дал им Космос на добро
Медь, железо, серебро,
Злато, олово, свинец…
Сын мой! Сера им отец!..
(Н.А.Михайлов.)
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Сера физические и химические свойства
Содержание
- 1. Презентация по химии на тему Сера физические и химические свойства
- 2. Цель урока: Определить положение серы в
- 3. План урокаПоложение серы в периодической системе Д.
- 4. История открытия серы и происхождение названия «сера»
- 5. Положение в периодической системе Д.И. МенделееваСераАтомный номер_Номер периода--Номер группы, подгруппа--
- 6. Строение атома серы Относительная атомная
- 7. Халькогены- рождающие руды Пирит FeS2Тиманнит HgS Антимонит Sb2S3
- 8. Сера– простое вещество Что такое аллотропия? Что называется аллотропной(видоизменением)?
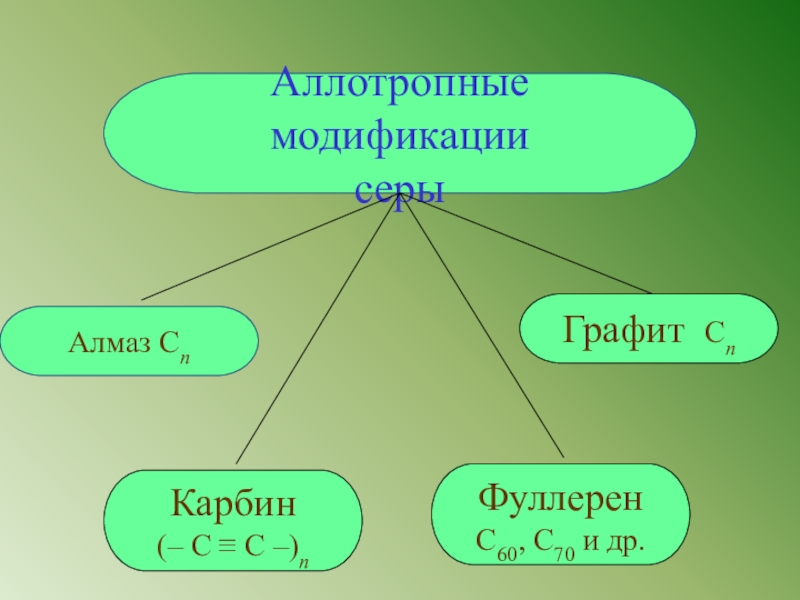
- 9. Аллотропные модификациисерыГрафит CnКарбин(– С ≡ С –)nФуллерен С60, С70 и др.Алмаз Cn
- 10. Слайд 10
- 11. Просмотр видео
- 12. Химические свойства серыПросмотр видео
- 13. Химические свойства углеродасстановительныеОкислительные Горение угля в кислороде:
- 14. Слайд 14
- 15. ФизкультминуткаХимию мы любим! Шеей вправо –влево крутим.К
- 16. Биологическая роль серыСера участвует в ОВР в
- 17. Применение серыПроизводство серной кислотыПолучение резиныПолучение гидросульфата кальция
- 18. тест 1. Какие степени окисления проявляет сера:а)
- 19. ответ1-б2-б3-б4-б5-г6-г
- 20. Слайд 20
- 21. ответ
- 22. Подведем итоги!
- 23. Спасибо !
- 24. Интернет-ресурсы, использованные для создания презентацииhttp://www.kamen-znak.ru/almaz.htmhttp://copypast.ru/2008/12/24/istorija_almaza_shakh_6_foto.htmlhttp://blogs.mail.ru/mail/livadas09/70C29CDB08B13644.htmlhttp://copypast.ru/2007/11/29/samye_izvestnye_almazy_mira_15_foto.htmlhttp://www.vokrugsveta.ru/telegraph/technics/182/http://mgudt.com/catalog/chemistryhttp://him.1september.ru/2003/33/1.htmhttp://www.celtica.ru/content/view/30/238/http://otvet.mail.ru/question/22419760/
Цель урока: Определить положение серы в периодической системе химических элементов Д.И. Менделеева, рассмотреть строение атома серы, физические и химические свойства, области применения серы.
Слайд 2Цель урока:
Определить положение серы в периодической системе химических элементов
Д.И. Менделеева, рассмотреть строение атома серы, физические и химические свойства, области применения серы.
Слайд 3План урока
Положение серы в периодической системе Д. И. Менделеева
Сера в
природе
Строение атома
Аллотропия серы
Физические свойства
Химические свойства
Применение серы
Биологическая роль серы
Строение атома
Аллотропия серы
Физические свойства
Химические свойства
Применение серы
Биологическая роль серы
Слайд 4История открытия серы и происхождение названия «сера»
Происхождение слова «сера» в русском языке не ясно. Существует несколько версий: по одной оно происходит от «серый», по другой - заимствовано из латинского языка (лат. sera - воск, serum - сыворотка); третья указывает на индоевропейский корень swelp - гореть, от которого произошло латинское sulfur. Есть и другие варианты.
Слайд 5Положение в периодической системе
Д.И. Менделеева
Сера
Атомный номер_
Номер периода--
Номер группы, подгруппа--
Слайд 6
Строение атома серы
Относительная атомная масса: Ar =32
Число протонов в ядре ядре:
р+ =16
Число нейтронов в ядре: n0 =16 (n0 = Ar- p+)
Общее число электронов в атоме: е- =16
Число нейтронов в ядре: n0 =16 (n0 = Ar- p+)
Общее число электронов в атоме: е- =16
Слайд 13
Химические свойства углерода
сстановительные
Окислительные
Горение угля в кислороде:
C + O2 = CO2,
2C
+ O2 = 2CO
(недостаток кислорода).
Взаимодействие со сложными веществами: C + CO2 = 2CO,
C + H2O = CO + H2.
Взаимодействие со сложными веществами: C + CO2 = 2CO,
C + H2O = CO + H2.
Взаимодействие
с активными металлами:
Ca + 2C = CaC2,
4Al + 3C = Al4C3.
t
t
t
t
t
t
Слайд 15Физкультминутка
Химию мы любим! Шеей вправо –влево крутим.
К знаниям найдем дорожку и
попрыгаем немножко
Есть в оксидах кислород – делай вправо поворот.
А в кислотах – водород! Делай влево поворот.
Лакмус в щелочи синеет. Шагом марш! Быстрей! Бодрее!
Есть гидроксигруппа в ней, сжали кулачки сильней!
Много разных есть солей. Приседаем! Веселей!
Вы учиться не ленитесь, поклонитесь, улыбнитесь!
Стоп, закончена зарядка, вдох и выдох для порядка.
И готовы вы опять на вопросы отвечать.
Спасибо!
Есть в оксидах кислород – делай вправо поворот.
А в кислотах – водород! Делай влево поворот.
Лакмус в щелочи синеет. Шагом марш! Быстрей! Бодрее!
Есть гидроксигруппа в ней, сжали кулачки сильней!
Много разных есть солей. Приседаем! Веселей!
Вы учиться не ленитесь, поклонитесь, улыбнитесь!
Стоп, закончена зарядка, вдох и выдох для порядка.
И готовы вы опять на вопросы отвечать.
Спасибо!
Слайд 16Биологическая роль серы
Сера участвует в ОВР в организмах растений и животных
Сера
входит в состав белков и аминокислот
Особенно много серы в волосах, шерсти, рогах, копытах
Соединения серы обнаружены в хрящах, костях, в желчи
Особенно много серы в волосах, шерсти, рогах, копытах
Соединения серы обнаружены в хрящах, костях, в желчи
Слайд 17Применение серы
Производство серной кислоты
Получение резины
Получение гидросульфата кальция (для производства бумаги)
Производство пороха,
пиротехники
Получение «сусального золота» – SnS2
В медицине для лечения кожных заболеваний
В сельском хозяйстве для борьбы с вредителями
Получение «сусального золота» – SnS2
В медицине для лечения кожных заболеваний
В сельском хозяйстве для борьбы с вредителями
Слайд 18тест
1. Какие степени окисления проявляет сера:
а) +2, +3, +4.
б) –2,
+4, +6.
в) –1, –2, +6.
2. Флотация – это свойство серы
а) растворяться в воде; б) не смачиваться в воде; в) частично растворяться в горячей воде
3. Какой модификации серы не существует:
а) ромбической; б) тетраэдрической;
в) моноклинной; г) пластической?
4. Сера не растворяется в:
а) ацетоне; б) воде;
в) сероуглероде; г) толуоле.
5. При комнатной температуре без первоначального нагревания сера реагирует с:
а) железом; б) цинком;
в) алюминием; г) ртутью.
6. В каком виде сера практически не встречается в природе:
а) самородная; б) сульфидная;
в) сульфатная; г) сульфитная?
2. Флотация – это свойство серы
а) растворяться в воде; б) не смачиваться в воде; в) частично растворяться в горячей воде
3. Какой модификации серы не существует:
а) ромбической; б) тетраэдрической;
в) моноклинной; г) пластической?
4. Сера не растворяется в:
а) ацетоне; б) воде;
в) сероуглероде; г) толуоле.
5. При комнатной температуре без первоначального нагревания сера реагирует с:
а) железом; б) цинком;
в) алюминием; г) ртутью.
6. В каком виде сера практически не встречается в природе:
а) самородная; б) сульфидная;
в) сульфатная; г) сульфитная?
Слайд 20 Кроссворд
1.На внешнем энергетическом
уровне у атома серы… электронов
2. Явление, когда один и тот же химический элемент образует несколько простых веществ.
3.Процесс всплытия пустой породы.
4.Элемент – неметалл шестой группы.
5.Соли сероводородной кислоты
6.Газ с запахам тухлых яиц.
.
2. Явление, когда один и тот же химический элемент образует несколько простых веществ.
3.Процесс всплытия пустой породы.
4.Элемент – неметалл шестой группы.
5.Соли сероводородной кислоты
6.Газ с запахам тухлых яиц.
.