- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Роль воды в химических реакциях
Содержание
- 1. Презентация по химии на тему Роль воды в химических реакциях
- 2. ВОДАВода – это жидкость без цвета, запаха
- 3. РОЛЬ ВОДЫ В ХИМИЧЕСКИХ РЕАКЦИЯХ:водаРеакционная средаФактор диссоциацииТранспорт веществРеагентКатализатор
- 4. РАСТВОРИМОСТЬ ВЕЩЕСТВ В ВОДЕПо растворимости в воде все вещества условно делятся на три группы
- 5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯЭлектролиты – это вещества, которые
- 6. ПО РАСТВОРИМОСТИ В ВОДЕРастворимые (в 100г воды
- 7. ТИПЫ ЭЛЕКТРОЛИТОВ:Кислоты – это электролиты, диссоциирующие на
- 8. Слайд 8
- 9. ЭЛЕКТРОЛИТЫ СЛАБЫЕСЛАБЫЕ(Степень диссоциации стремиться
- 10. Слайд 10
- 11. H2O как транспортировщик веществВсе жидкие среды более
- 12. Слайд 12
Слайд 1«РОЛЬ ВОДЫ
В ХИМИЧЕСКИХ РЕАКЦИЯХ»
Выполнила:
учитель МБОУ «Спеховская СОШ»
Кротикова Оксана Владимировна
Урок
Слайд 2ВОДА
Вода – это жидкость без цвета, запаха и вкуса, tкип =
Вода - единственное вещество, которое при затвердении сжимается. Поэтому плотность льда меньше плотности жидкой воды. Вот почему лёд плавает на поверхности воды.
Вода – это жидкость без цвета, запаха и вкуса,
tкип = 100 °C, tпл = 0 °C, p= 1г/см3 (при 4 °С).
Вода проводит электрический ток, плохо проводит тепло, удельная теплоемкость воды очень высокая.
Вода - единственное вещество, которое при затвердении сжимается. Поэтому плотность льда меньше плотности жидкой воды. Вот почему лёд плавает на поверхности воды.
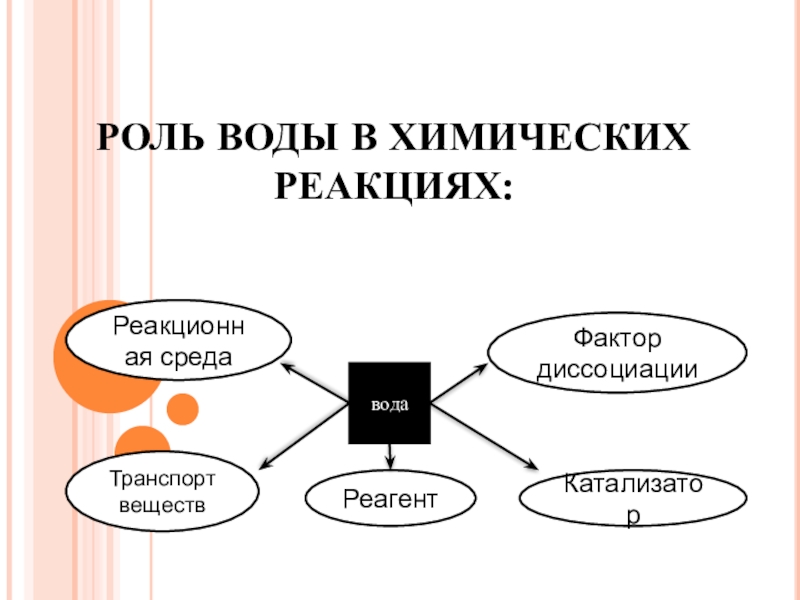
Слайд 3РОЛЬ ВОДЫ В ХИМИЧЕСКИХ РЕАКЦИЯХ:
вода
Реакционная среда
Фактор диссоциации
Транспорт веществ
Реагент
Катализатор
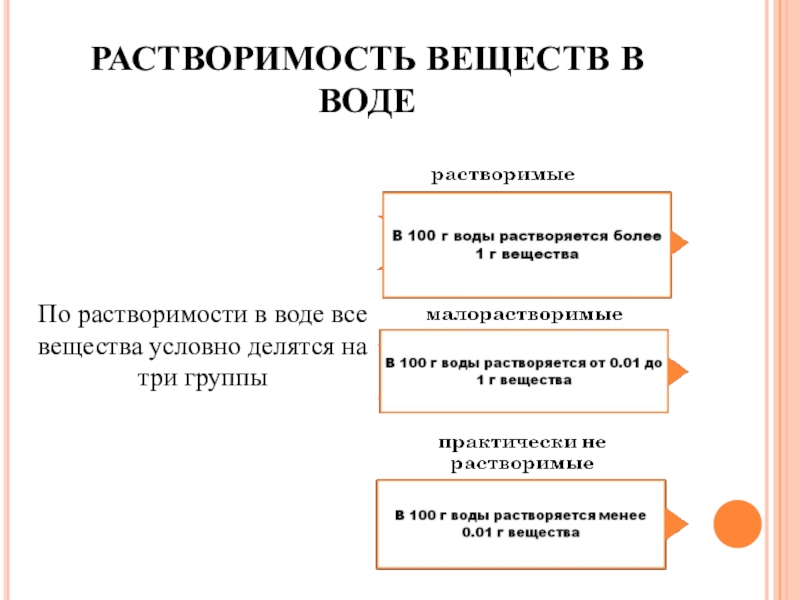
Слайд 4РАСТВОРИМОСТЬ ВЕЩЕСТВ В ВОДЕ
По растворимости в воде все вещества условно делятся
Слайд 5 ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ
Электролиты
– это вещества, которые в растворах распадаются на
Степень электролитической диссоциации – отношение числа молей вещества, распавшегося на ионы, к общему количеству растворённого вещества
Слайд 6ПО РАСТВОРИМОСТИ В ВОДЕ
Растворимые
(в 100г воды растворяется более 1 г
Гидроксиды щелочных Me;
Почти все нитраты;
Все моносахариды;
Низшие спирты
Карбоновые кислоты
Малорастворимые
(в 100г воды растворяется
от 0,01 до 1 г вещества)
Ca(OH)2;
BaF2 и AlF3;
Сульфат серебра и свинца
Анилин и фенол
Практически нерастворимые
(в 100г воды растворяется менее 0,01 г вещества)
Почти все фосфаты и карбонаты;
Все углеводороды;
Высшие спирты
Альдегиды
Карбоновые кислоты
Слайд 7ТИПЫ ЭЛЕКТРОЛИТОВ:
Кислоты – это электролиты, диссоциирующие на катионы водорода и анионы
Основания – это электролиты, диссоциирующие на катионы металла (аммония или органического основания) и гидроксид-анионы
Соли – это электролиты, диссоциирующие на катионы металла и анион кислотного остатка
Слайд 9ЭЛЕКТРОЛИТЫ
СЛАБЫЕ
СЛАБЫЕ
(Степень диссоциации стремиться к единице)
(Степень диссоциации
Все щёлочи;
Все соли;
Кислоты: HCl, HNO3, H2SO4, HClO4, HBr, HJ, CF3COOH и др.
Многие неорганические кислоты (H2S, H2CO3, HCN);
Почти все органические кислоты.
Слайд 10 H2O КАК КАТАЛИЗАТОР
H2O
* Если их просто смешать, реакция не идет - если добавить каплю воды, то реакция сразу же начнется и будет идти бурно.
Взаимодействие сухих порошков алюминия и йода.
2Al + 3J2 = 2AlJ3 + Q
Слайд 11H2O как транспортировщик веществ
Все жидкие среды более чем на 90 –
Разносит по организму O2, питательные вещества, гормоны и т.д.
Кровь:
Доставляет СO2 и продукты распада к местам их удаления из организма
Слайд 12 ДОМАШНЕЕ ЗАДАНИЕ
1. Реакции ионного
А) K2S + 2HCl =
Б) K2S + NaNO3 =
В) K2SO4 + Pb(NO3)2 =
2. Восстановите молекулярные уравнения:
А) Fe + 3OH = Fe(OH)3
Б) 2H + S = H2S
В) 3Ca + 2PO4 = Ca3(PO4)2
+
2-
3+
-