- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Основные сведения о строении атома
Содержание
- 1. Презентация по химии на тему: Основные сведения о строении атома
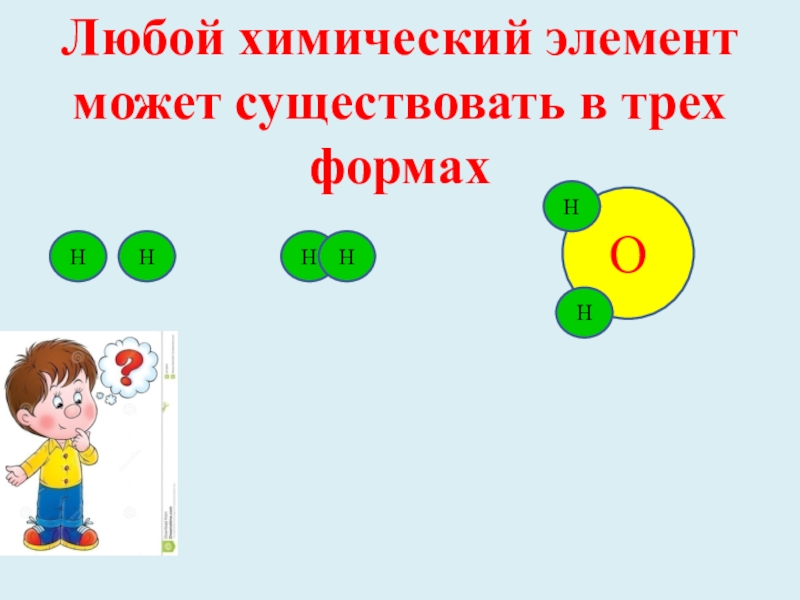
- 2. Любой химический элемент может существовать в трех формах ННННОНН
- 3. Понятие атом возникло ещё в античном мире для обозначения частиц вещества.
- 4. Ученые древности о строении веществаДревнегреческий ученый Демокрит
- 5. История открытия строения атомовИрландский физик СТОНИ на
- 6. История открытия строения атомовУильям КруксВ 1879 году открыл катодные лучи.
- 7. История открытия строения атомовДжозеф Томсон и Жан Перрен доказали, что электроны несут на себе отрицательный заряд
- 8. История открытия строения атомовДжозеф Томсон доказал, что
- 9. Открытие радиактивностиАнри БеккерельРасщепление радиоактивного излучения
- 10. Различают 3 вида радиоактивных лучейα-лучи – поток
- 11. В 1910 г. Эрнест Резерфорд со своими
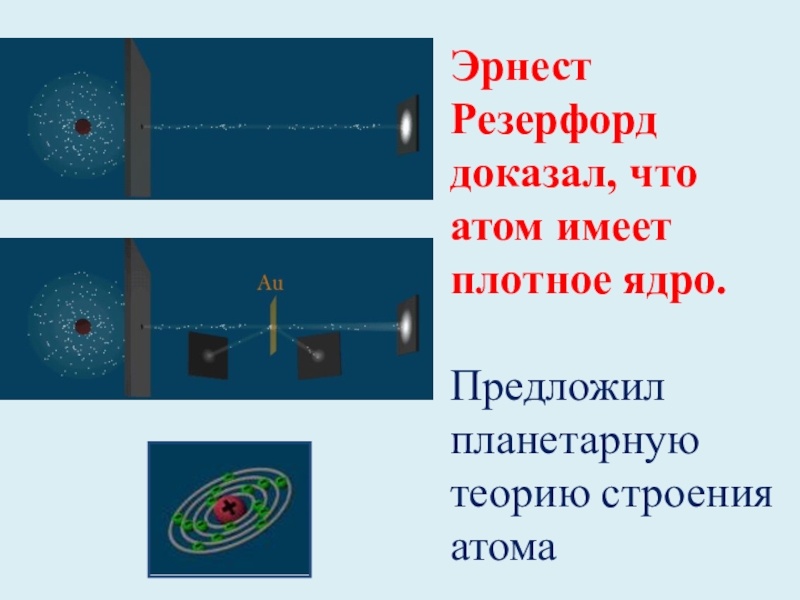
- 12. Эрнест Резерфорд доказал, что атом имеет плотное ядро. Предложил планетарную теорию строения атома
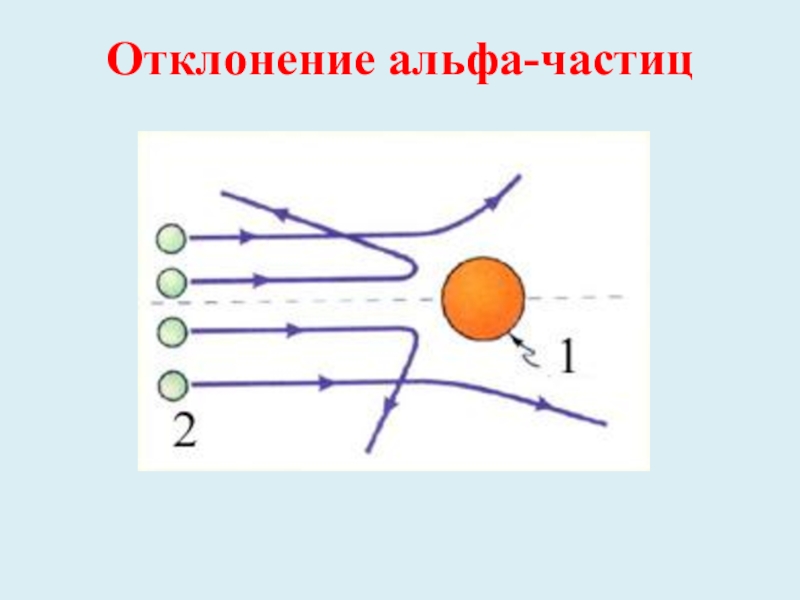
- 13. Отклонение альфа-частиц
- 14. В 1911 г. Эрнест Резерфорд доказал, что в центре атома имеется положительно заряженное ядро.
- 15. Планетарная модель строения атома Резерфорд предположил, что
- 16. Ядро состоит из 2 частиц – протонов
- 17. Масса электрона ничтожна мала, поэтому ей можно
- 18. Основные характеристики элементарных частиц
Любой химический элемент может существовать в трех формах ННННОНН
Слайд 4Ученые древности о строении вещества
Древнегреческий ученый Демокрит 2500 лет назад считал,
что любое вещество состоит из мельчайших частиц, которые впоследствии были названы «атомами», что в переводе на русский язык означает «неделимый»
Долгое время считалось, что атом является неделимой частицей.
Долгое время считалось, что атом является неделимой частицей.
Слайд 5История открытия строения атомов
Ирландский физик СТОНИ на основании опытов пришёл к
выводу, что электричество переносится мельчайшими частицами, существующими в атомах всех химических элементов
В 1891 предложил название «электрон», что по-гречески означает «янтарь» для элементарного
В 1891 предложил название «электрон», что по-гречески означает «янтарь» для элементарного
Слайд 7История открытия строения атомов
Джозеф Томсон и Жан Перрен доказали, что электроны
несут на себе отрицательный заряд
Слайд 8История открытия строения атомов
Джозеф Томсон доказал, что электроны несут на себе
отрицательный заряд, определил массу и скорость движения.
е
- электрон
Слайд 10Различают 3 вида радиоактивных лучей
α-лучи – поток ядер атомов гелия
β-лучи –
поток электронов
γ-лучи – электромагнитные волны, не несущие электрического заряда
Слайд 11В 1910 г. Эрнест Резерфорд со своими учениками и коллегами изучал
рассеивание альфа-частиц, проходящих через тонкую золотую фольгу и попадавших на экран.
Слайд 12Эрнест Резерфорд доказал, что атом имеет плотное ядро.
Предложил планетарную теорию
строения атома
Слайд 14В 1911 г. Эрнест Резерфорд доказал, что в центре атома имеется
положительно заряженное ядро.
Слайд 15
Планетарная модель строения атома
Резерфорд предположил, что атом устроен подобно планетарной
системе.
Суть модели строения атома по Резерфорду заключается в следующем: в центре атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца).
Заряд ядра совпадает с номером химического элемента в таблице Менделеева.
Суть модели строения атома по Резерфорду заключается в следующем: в центре атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца).
Заряд ядра совпадает с номером химического элемента в таблице Менделеева.
Слайд 16Ядро состоит из 2 частиц – протонов и нейтронов
Протоны имеют положительный
заряд, и массу, примерно равную массе атома водорода
Нейтроны не несут заряда, они нейтральны и имеют массу, примерно равную массе протона
p ;p+
n ;n0
Слайд 17Масса электрона ничтожна мала, поэтому ей можно пренебречь
Обозначение электрона е
Сумма протонов
и нейтронов в атоме называется массовым числом (А)