- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Основания
Содержание
- 1. Презентация по химии на тему Основания
- 2. ОСНОВАНИЯГидроксид натрияГидроксид железа(II)Гидроксид кальция
- 3. NaOH – гидроксид натрияMg(OH)2– гидроксид магнияFe(OH)2 –
- 4. – это сложные вещества, имеющие в
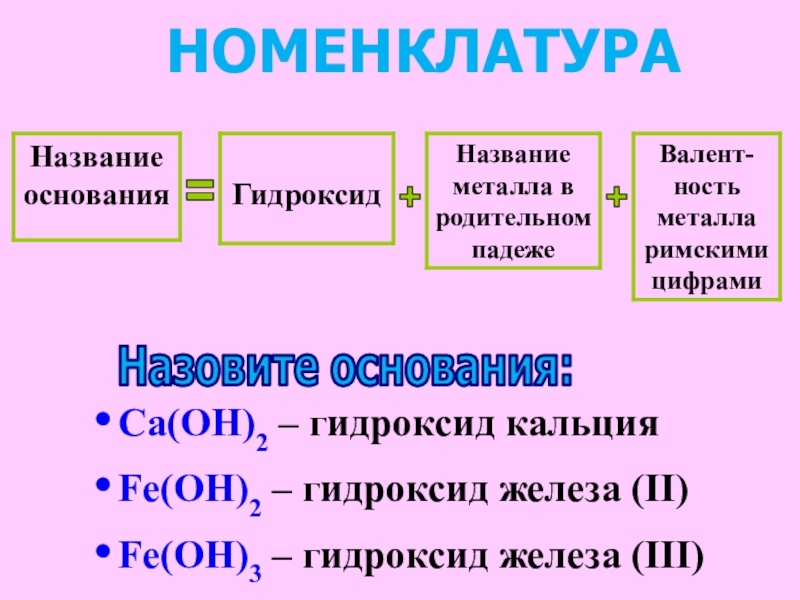
- 5. НОМЕНКЛАТУРАCa(OH)2 – гидроксид кальцияFe(OH)2 – гидроксид железа (II)Fe(OH)3 – гидроксид железа (III)=++Назовите основания:
- 6. 1. Основание + кислота → соль +
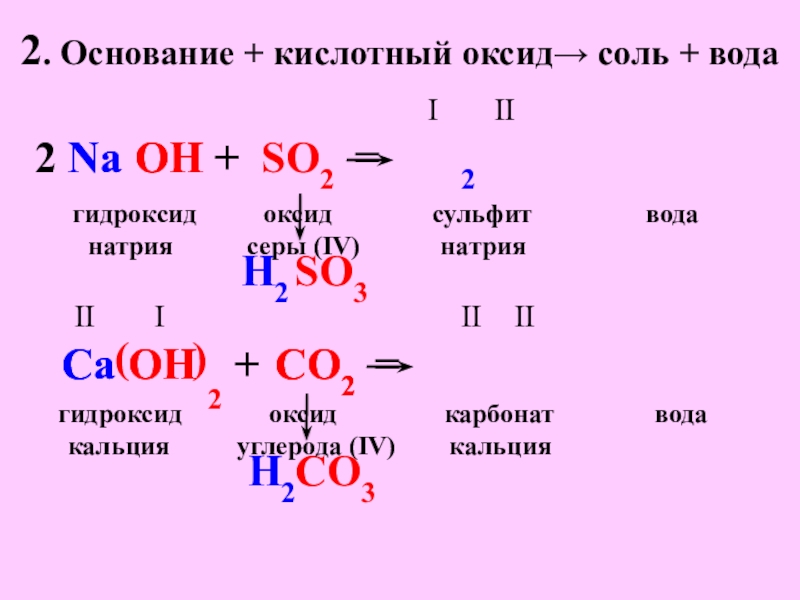
- 7. 2. Основание + кислотный оксид→ соль +
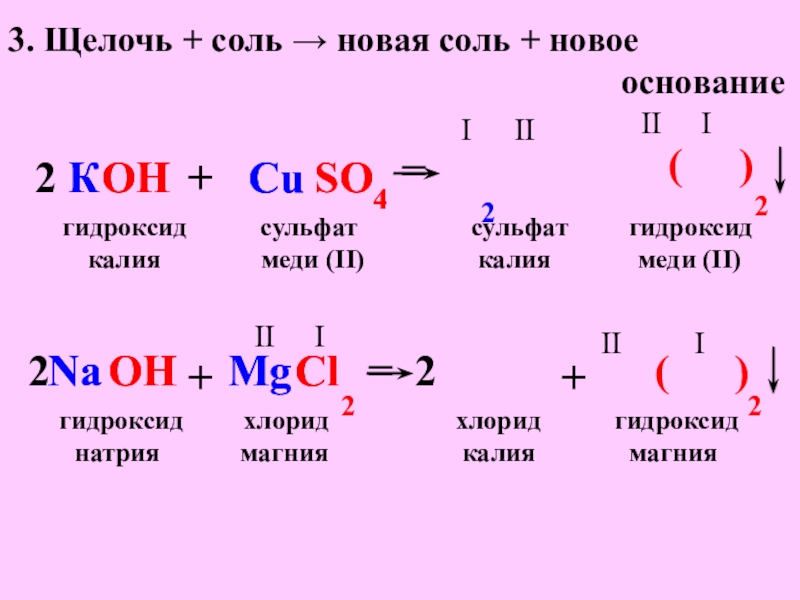
- 8. 3. Щелочь + соль → новая соль
- 9. 4. Разложение нерастворимых оснований при
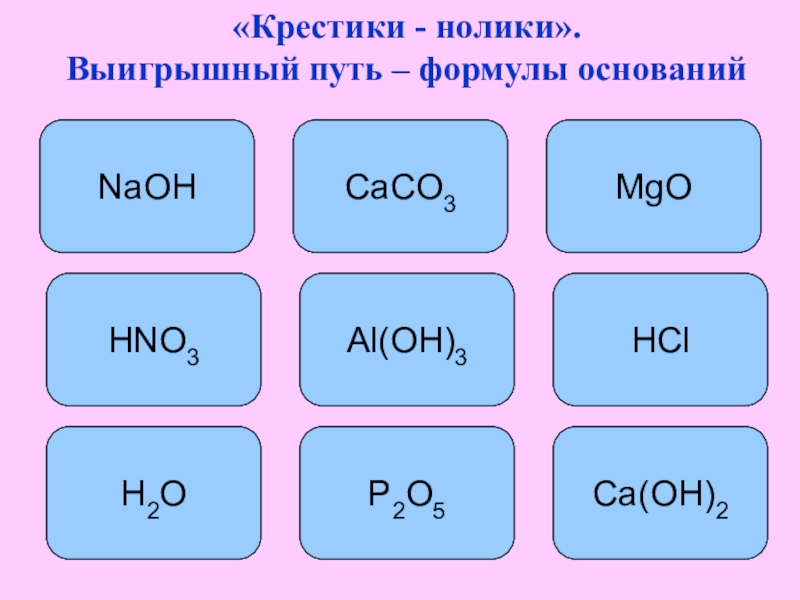
- 10. «Крестики - нолики». Выигрышный путь – формулы основанийNaOHAl(OH)3Ca(OH)2CaCO3MgOHNO3HClH2OP2O5
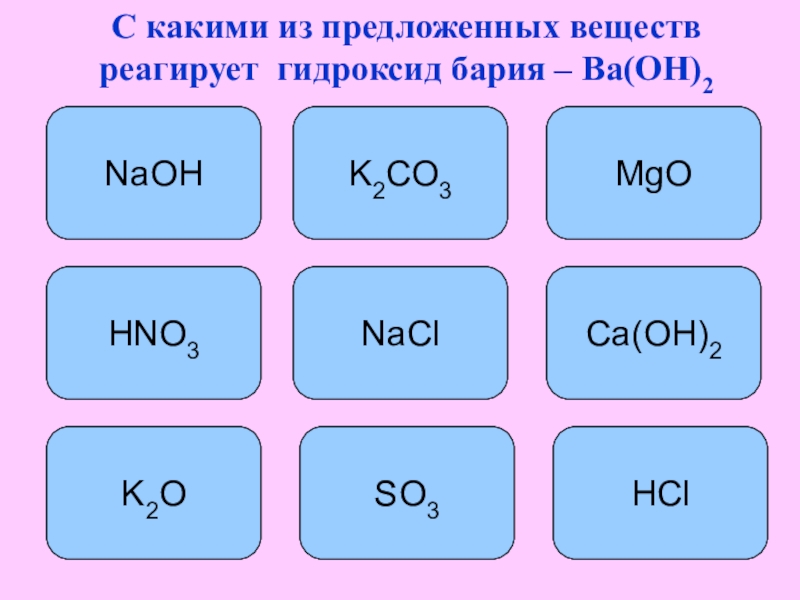
- 11. С какими из предложенных веществ реагирует гидроксид бария – Ba(OH)2K2CO3MgOHClK2ONaOHHNO3SO3Ca(OH)2NaCl
Слайд 1ХИМИЯ 8 КЛАСС
ОСНОВАНИЯ. КЛАССИФИКАЦИЯ. СВОЙСТВА.
УЧИТЕЛЬ ХИМИИ
МБОУ СОШ №41 Г.ШАХТЫ
Слайд 3NaOH – гидроксид натрия
Mg(OH)2– гидроксид магния
Fe(OH)2 – гидроксид железа (II)
Fe(OH)3 –
П О Н Я Т И Е
Рассматривая формулы, какой можно сделать вывод о составе оснований?
Слайд 4 – это сложные вещества, имеющие в своем составе атомы металла
ОСНОВАНИЯ
Слайд 5НОМЕНКЛАТУРА
Ca(OH)2 – гидроксид кальция
Fe(OH)2 – гидроксид железа (II)
Fe(OH)3 – гидроксид железа
=
+
+
Назовите основания:
Слайд 61. Основание + кислота → соль + вода
Na
Na
OH
OH
+
+
Сl
Сl
Н
Н
I
I
(Н2О)
=
гидроксид
натрия кислота натрия
Cu
Cu
I
OH
OH
(
)
2
+
H2
H
SO4
SO4
+
2
гидроксид серная сульфат вода
меди (II) кислота меди (II)
=
II
II
II
Fe(OH)2
+
HCl
2
=
FeCl2
+
Н2О
2
Химические свойства оснований
Слайд 72. Основание + кислотный оксид→ соль + вода
Na
Na
OH
OH
+
SO2
H
SO3
II
I
2
+
2
гидроксид оксид сульфит вода
натрия серы (IV) натрия
=
Ca
OH
OH
+
+
Ca
II
I
(
)
2
СO2
СO2
Н
СO3
II
II
2
гидроксид оксид карбонат вода
кальция углерода (IV) кальция
=
Слайд 83. Щелочь + соль → новая соль + новое
Cu
OH
К
К
OH
+
+
Cu
SO4
SO4
2
I
II
(
)
2
II
I
2
гидроксид сульфат сульфат гидроксид
калия меди (II) калия меди (II)
Na
Na
OH
OH
+
=
Mg
Cl
II
I
Mg
Cl
2
+
(
)
II
I
2
гидроксид хлорид хлорид гидроксид
натрия магния калия магния
=
2
2
Слайд 9 4. Разложение нерастворимых оснований при нагревании:
2 Fe(OH)3 = Fe2О3 + 3 Н2О
гидроксид оксид вода
железа (III) железа (III)
t
Cu(OH)2 = CuO + Н2О
гидроксид оксид вода
меди (II) меди (II)