- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Оксиды , их классификация, свойства и применение.
Содержание
- 1. Презентация по химии на тему Оксиды , их классификация, свойства и применение.
- 2. Древний философ Фалес из Милета еще в
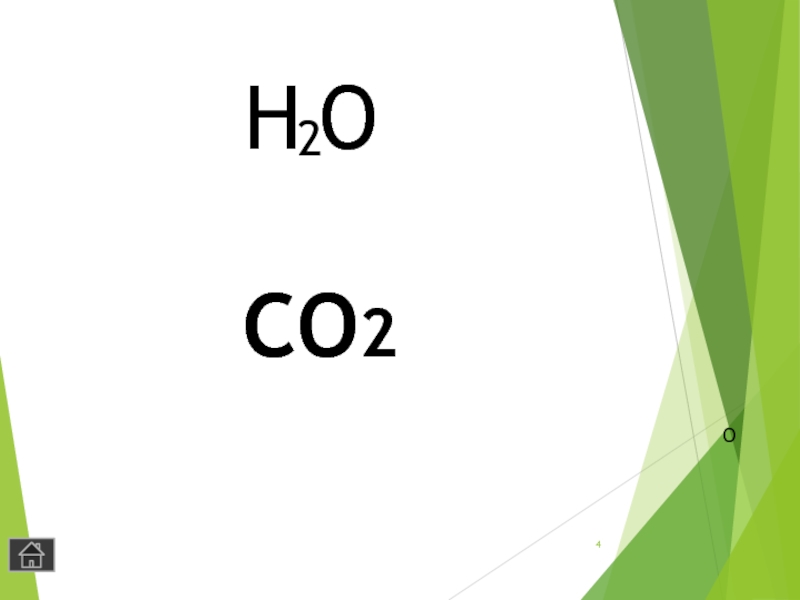
- 3. Это газ, необходимый растениям для фотосинтеза. Это газ, выделяемый нами при выдохе.
- 4. CO2H2OО
- 5. Оксиды - это
- 6. пс
- 7. Вещества:Сложные Простые S, Fe, H2 ,O2 ,
- 8. Из предложенных формул веществ выписать в столбик
- 9. SO3 MgO Na2O
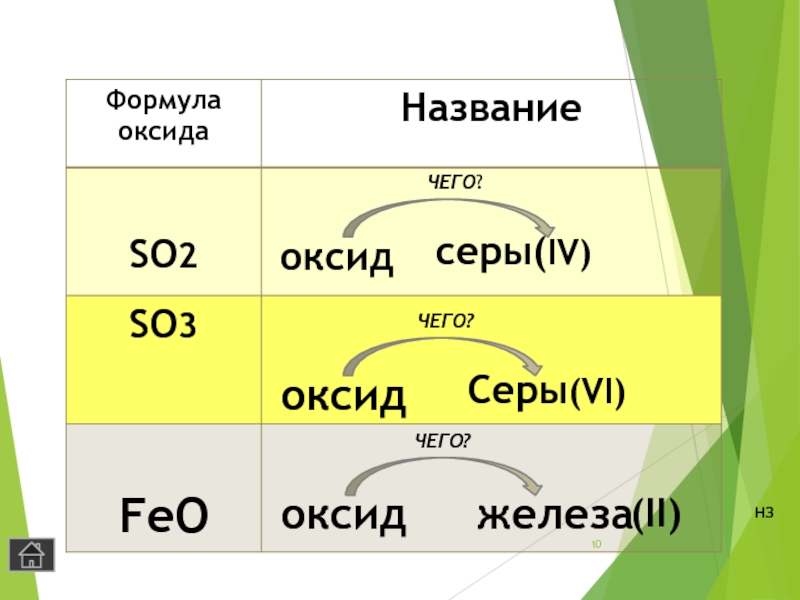
- 10. оксидсеры(IV)ЧЕГО?оксидCеры(VI)ЧЕГО?оксиджелезаЧЕГО?(II)нз
- 11. П.
- 12. SO3MgONa2OP2O5SO2P2O3CaOОксид серы (VI)Оксид серы( Оксид фосфора( VОксид фосфора(Оксид натрияОксид магнияОксид кальцияIV))III)З.
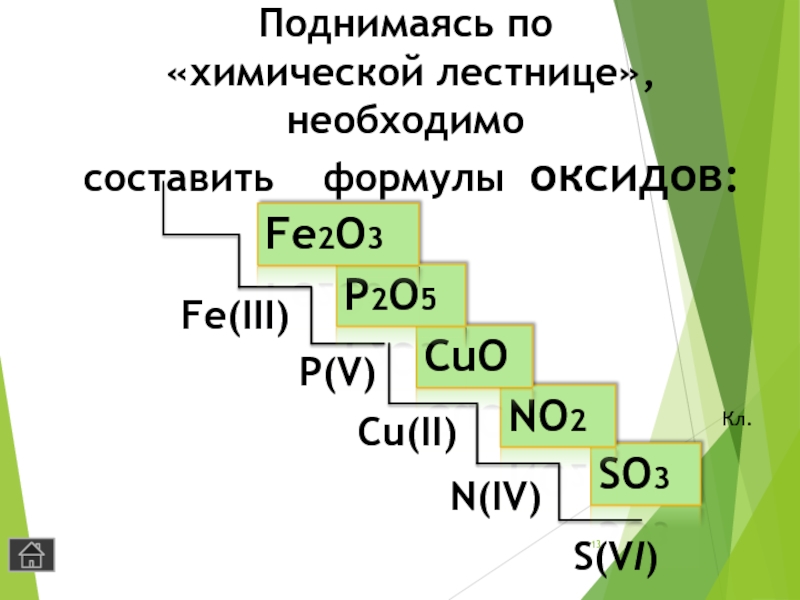
- 13. Поднимаясь по «химической лестнице», необходимо составить формулы оксидов:S(VI)N(IV)Cu(II)P(V)Fe(III)SO3NO2CuOP2O5Fe2O3Кл.
- 14. I. По составу
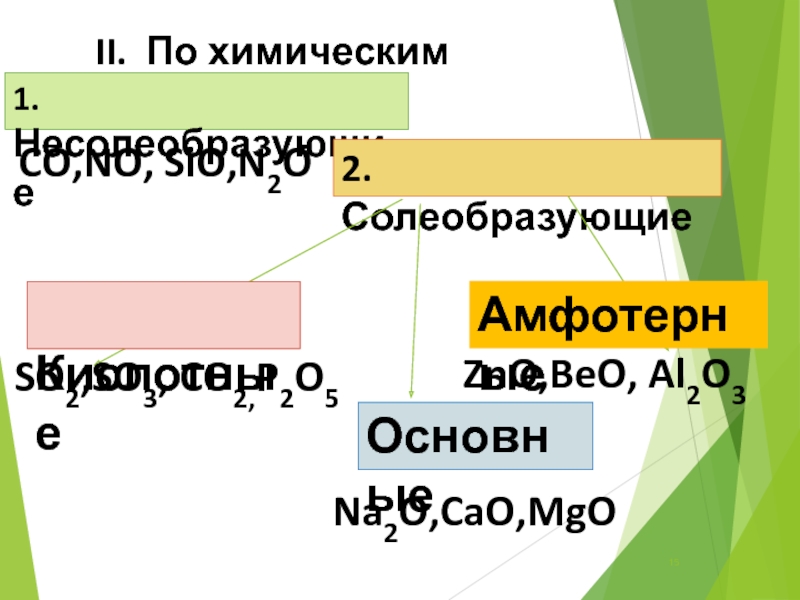
- 15. II. По химическим свойствам1. Несолеобразующие2.СолеобразующиеCO,NO, SiO,N2O Кислотные ОсновныеАмфотерныеSO2,SO3, CO2,P2O5 Na2O,CaO,MgOZnO,BeO, Al2O3
- 16. Кислотные оксиды образуются атомами неметаллов,а также атомами
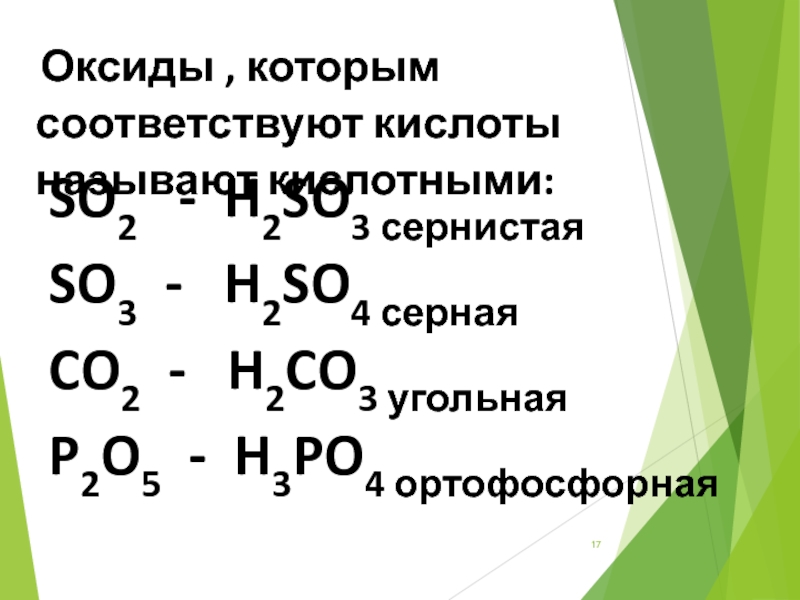
- 17. Оксиды , которым соответствуют кислоты называют
- 18. Основные оксиды образуются атомами только металлов, валентность которых меньше 4-хЗ-О
- 19. Оксиды , которым соответствуют основания называют
- 20. Распределите предложенные формулы оксидов на кислотные и
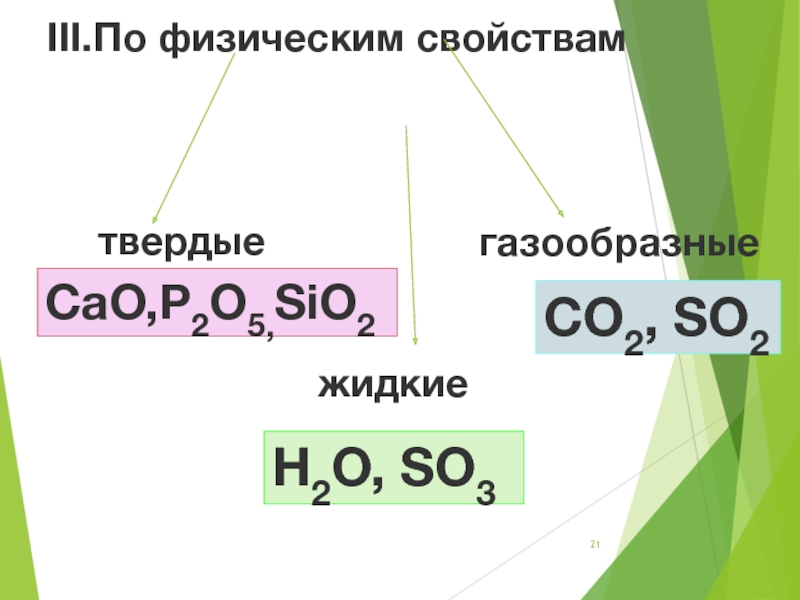
- 21. III.По физическим свойствамтвердыежидкие газообразныеCaO,P2O5,SiO2 H2O, SO3 CO2, SO2
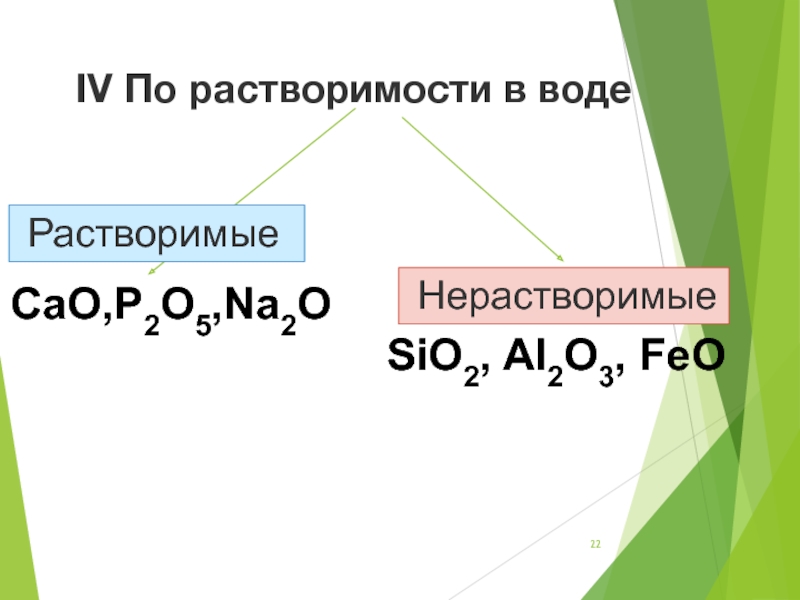
- 22. IV По растворимости в воде Растворимые НерастворимыеCaO,P2O5,Na2O SiO2, Al2O3, FeO
- 23. О.
- 24. Получение оксидов1.Взаимодействие простых веществ с кислородом .
- 25. 3. Разложение сложных веществ:а) Нерастворимых оснований :
- 26. Слайд 26
- 27. Работа по слайду1). S + O2
- 28. Нахождениев природеоксидов
- 29. В земной коре – литосфере – находятся:
- 30. Водная оболочка Земли – гидросфера – это оксид водорода
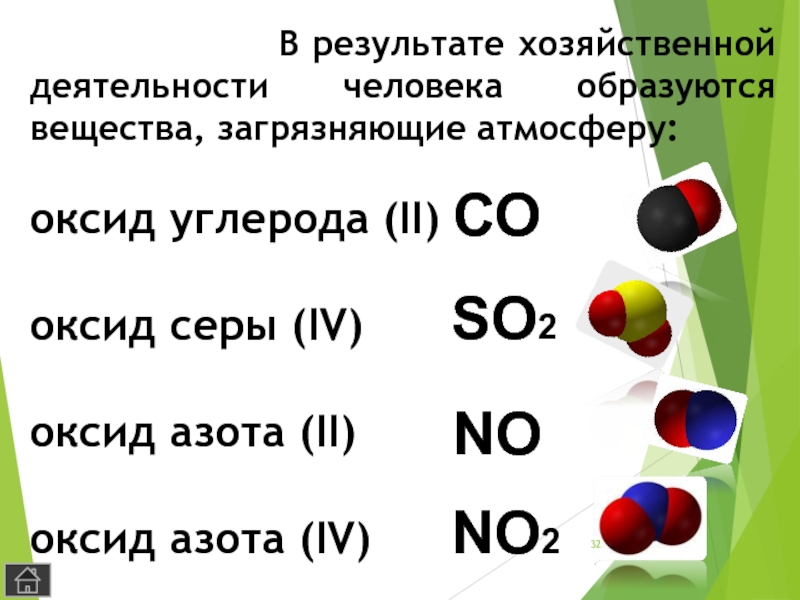
- 31. В воздухе есть оксид углерода (IV)(углекислый газ) СО2СОО
- 32. Слайд 32
- 33. Применение некоторыхОКСИДОВ
- 34. Оксид кремния (SiO2) применяют в производстве стекла, керамики и других материалов
- 35. Оксид кальция (негашёная известь) используется в строительствеОксид кальция ( CaO )
- 36. Оксид цинка (ZnO)Это вещество белого цвета, используется для приготовления белой краски (цинковые белила)
- 37. Оксид хрома(III) (Cr2 O3)Это кристаллы зеленого цвета. Используется при изготовлении декоративного зелёного стекла
- 38. Оксид углерода(II)(CO) применяется для обработки мяса животных
- 39. Оксид углерода(IV) (углекислый газ)применяется в пищевой промышленности для производства газированных напитковСО2
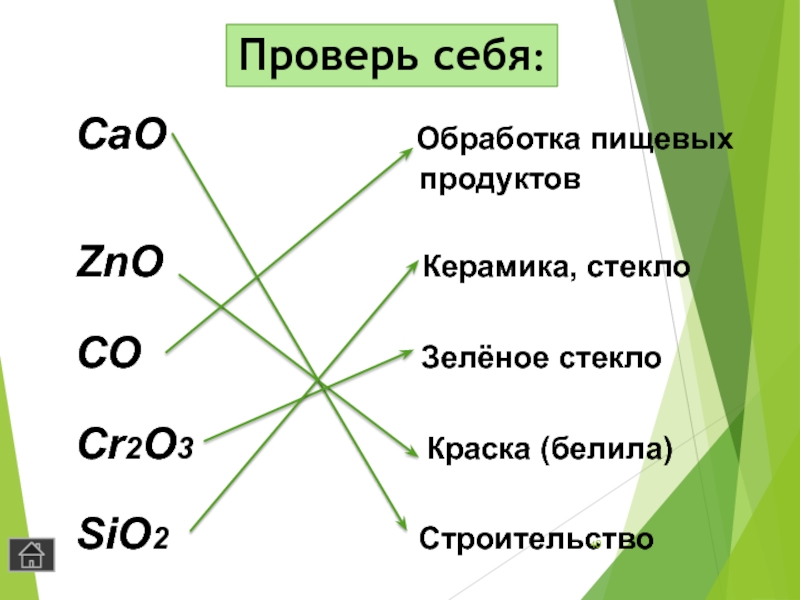
- 40. Проверь себя: CaO
- 41. На уроке мы:-выбирали оксиды среди других веществ;-называли
- 42. 1. Сегодня на уроке я вспомнил(а)… 2. Я
- 43. Домашнее задание :§ 40 , упр.1-4Стр.135тесты
- 44. Спасибо за работу на уроке
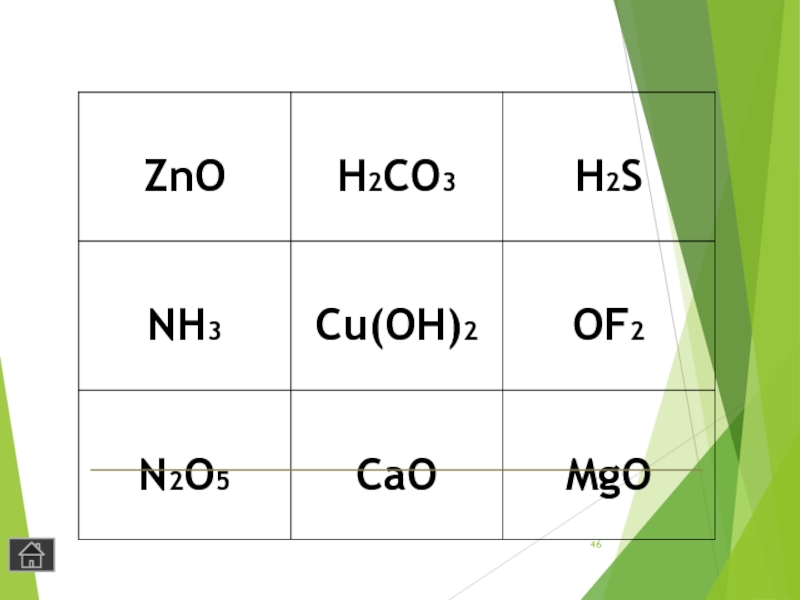
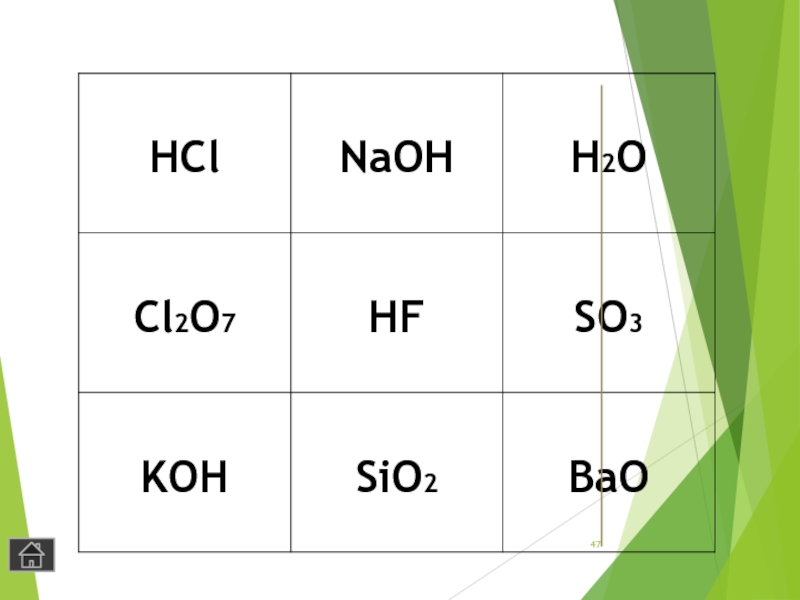
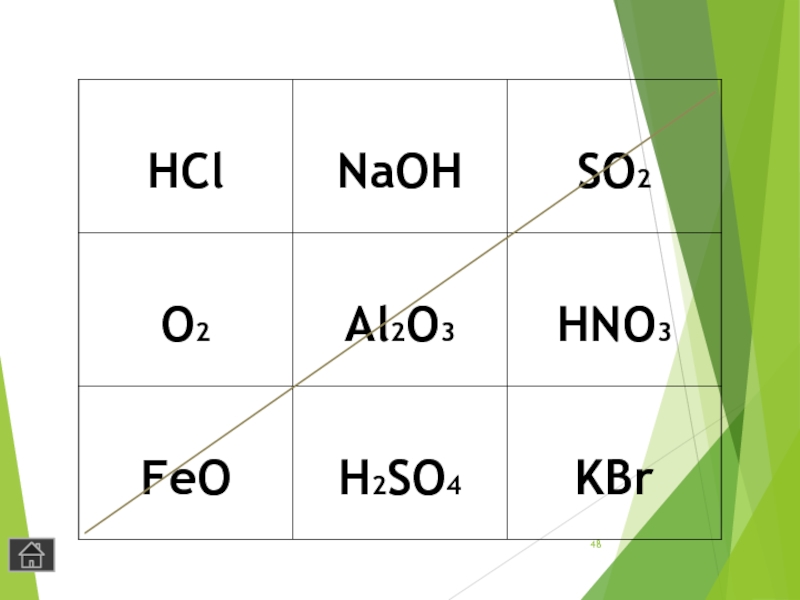
- 45. Игра «Крестики – нолики»Покажите выигрышный путь, который составляют формулы ОКСИДОВ
- 46. Слайд 46
- 47. Слайд 47
- 48. Слайд 48
Слайд 1«Оксиды, их классификация, свойства и применение».
Выполнила :учитель химии ГБОУ СОШ
№262 Абакумова Т.С.
Слайд 2Древний философ Фалес из Милета еще в VI веке до нашей
«Она и дождь, и град, и снег, Туман и гололед, Носитель благ, предвестник бед - И радуга и лед.»
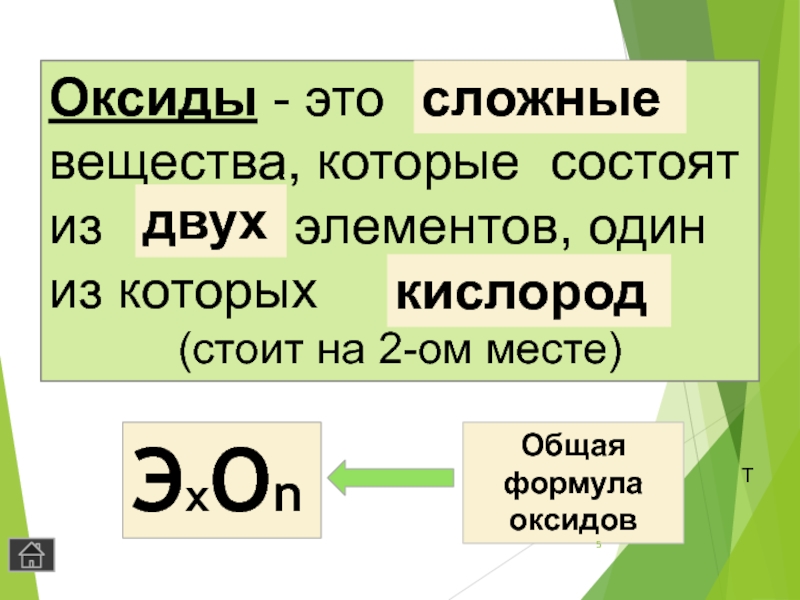
Слайд 5Оксиды - это (какие?)
(стоит на 2-ом месте)
сложные
двух
кислород
ЭxОn
Общая
формула
оксидов
Т
Слайд 7Вещества:
Сложные
Простые
S, Fe, H2 ,O2 ,
Оксиды-H2O, CO2 ,MgO
Основания-NaOH, Mg(OH)2,
Кислоты-H2SO4, H2CO3 , HCl
Соли-NaCl, Na2SO4, CaCO3
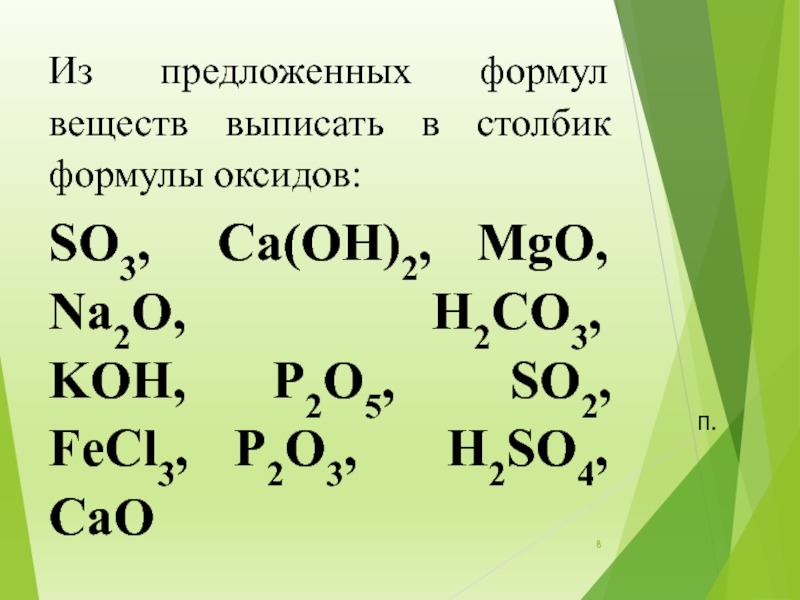
Слайд 8Из предложенных формул веществ выписать в столбик формулы оксидов:
SO3, Ca(OH)2,
П.
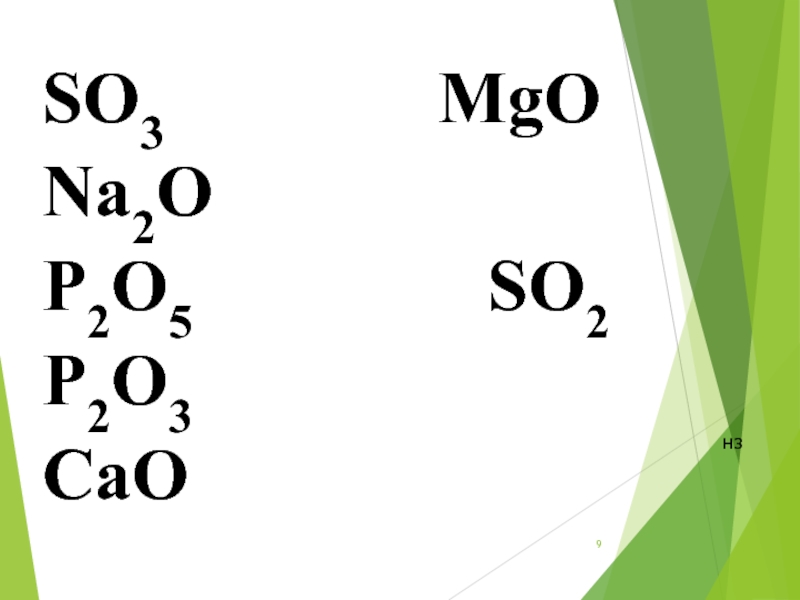
Слайд 12SO3
MgO
Na2O
P2O5
SO2
P2O3
CaO
Оксид серы (VI)
Оксид серы(
Оксид фосфора( V
Оксид фосфора(
Оксид натрия
Оксид
Оксид кальция
IV)
)
III)
З.
Слайд 13Поднимаясь по
«химической лестнице», необходимо
составить формулы оксидов:
S(VI)
N(IV)
Cu(II)
P(V)
Fe(III)
SO3
NO2
CuO
P2O5
Fe2O3
Кл.
Слайд 14 I. По составу
Оксиды металлов
Оксиды неметаллов
ZnO , BeO ,Al2O3 ,Na2O , CaO , MgO
SO2 , SO3, CO2, P2O5
Классификация оксидов
Слайд 15 II. По химическим свойствам
1. Несолеобразующие
2.Солеобразующие
CO,NO, SiO,N2O
Кислотные
Основные
Амфотерные
SO2,SO3, CO2,P2O5
Na2O,CaO,MgO
ZnO,BeO, Al2O3
Слайд 16Кислотные оксиды образуются атомами неметаллов,
а также атомами металлов, валентность которых
больше 4-х.
Пример:
З-К.
Слайд 17 Оксиды , которым соответствуют кислоты называют кислотными:
SO2 - H2SO3
SO3 - H2SO4 серная
CO2 - H2CO3 угольная
P2O5 - H3PO4 ортофосфорная
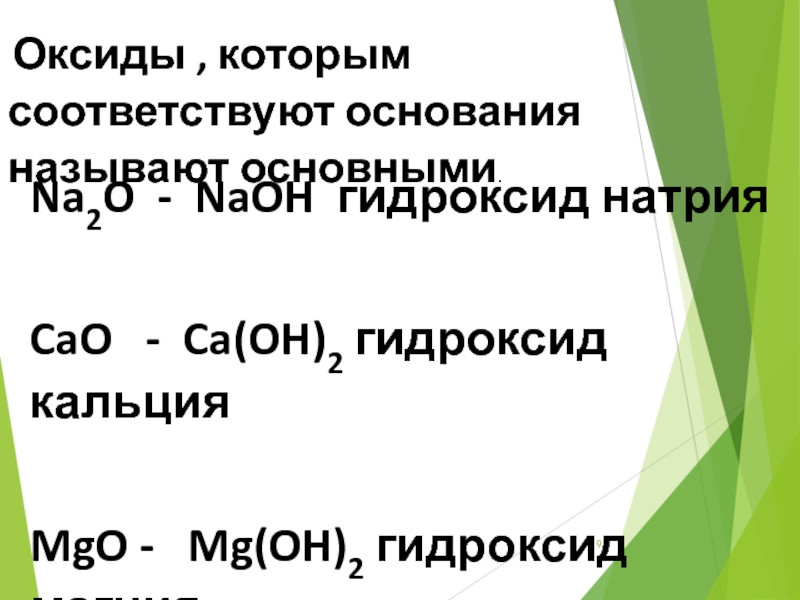
Слайд 19 Оксиды , которым соответствуют основания называют основными.
Na2O - NaOH гидроксид
CaO - Ca(OH)2 гидроксид кальция
MgO - Mg(OH)2 гидроксид магния
Слайд 20Распределите предложенные формулы оксидов на кислотные и основные, запишите их в
BaO, SiO2, FeO , CuO, N2O5 , CrO3 K2O
Ф
Слайд 24Получение оксидов
1.Взаимодействие простых веществ с кислородом .
2 Cu + O2
2. Взаимодействие сложных веществ с кислородом :
2ZnS + 3O2 →2ZnO +2 SO2↑
Слайд 253. Разложение сложных веществ:
а) Нерастворимых оснований :
Fe(OH)2→ FeO + H2O
б)
H2SO3 → SO2 + H2O
в) солей:
CaSiO3→ CaO + SiO2
t
t
t
Слайд 27Работа по слайду
1). S + O2 = SO2
2). CH4 +
3). Mg(OH)2= MgO + H2O
4). H2SiO3 = SiO2 + H2O
5). Ca CO3 = CaO + CO2↑
Н
Слайд 29В земной коре – литосфере – находятся:
оксид алюминия
оксид кремния(IV) (песок),
оксид железа(III) (содержится
в красном железняке).
Al2O3
SiO2
Fe2O3
Слайд 32 В
оксид углерода (II)
оксид серы (IV)
оксид азота (II)
оксид азота (IV)
СО
SO2
NO
NO2
Слайд 36Оксид цинка
(ZnO)
Это вещество белого цвета,
используется для приготовления
белой краски
(цинковые белила)
Слайд 37Оксид хрома(III)
(Cr2 O3)
Это кристаллы зеленого цвета. Используется при изготовлении декоративного
Слайд 38Оксид углерода(II)
(CO)
применяется для
обработки мяса животных и рыбы.
Он придает
не изменяя вкусовых качеств.
Слайд 39Оксид углерода(IV)
(углекислый газ)
применяется в пищевой промышленности для производства газированных
СО2
Слайд 40Проверь себя:
CaO
продуктов
ZnO Керамика, стекло
CO Зелёное стекло
Cr2O3 Краска (белила)
SiO2 Строительство
Слайд 41На уроке мы:
-выбирали оксиды среди других веществ;
-называли оксиды;
-составляли формулы оксидов;
2) знакомились
нахождением оксидов в природе;
применением оксидов.
1) выполняли задания, а именно:
● со способами получения оксидов
Слайд 421. Сегодня на уроке я вспомнил(а)…
2. Я узнал(а)…
3. Мне было интересно…
4.
5. Я работал(а) на уроке