- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Метод химического анализа
Содержание
- 1. Презентация по химии на тему Метод химического анализа
- 2. Задачей качественного анализа является установление состава вещества,
- 3. Качественный анализ«Сухой» метод анализаПри выполнении анализа «сухим»
- 4. «Мокрый» метод анализаПри анализе мокрым путем исследуемое
- 5. Методы разделения смеси катионов
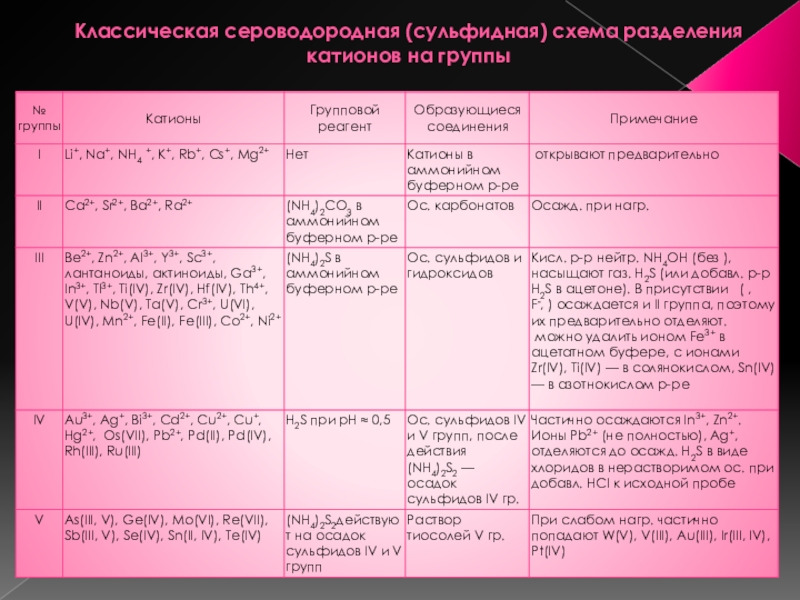
- 6. Классическая сероводородная (сульфидная) схема разделения катионов на группы
- 7. Классификация катионов по кислотно-щелочной схеме
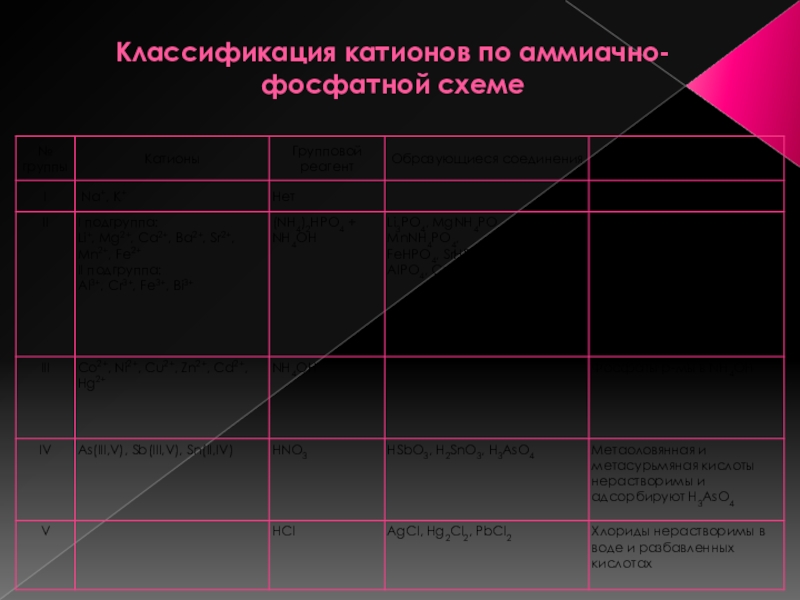
- 8. Классификация катионов по аммиачно-фосфатной схеме
- 9. Частные аналитические реакции катионов металловBa2+Sr2+Са2+Cr3+Fe2+Fe3+Mn2+
- 10. Частные аналитические реакции катионов металловMg2+Cd2+Co2+Сu2+
- 11. Количественный анализ
- 12. Йодометрическое титрованиеИодометрическим титрованием называется титриметрический метод анализа,
- 13. Перманганатометрическое титрованиеПерманганатометрическим титрованием называетсятитриметрический метод анализа, основанный на использовании в качестве титранта раствор KMnO4.
- 14. Бихроматометрическое титрованиеБихроматометрией называется титриметрический метод анализа, основанный
- 15. Комплексонометрическое титрованиеКомплексонометрическое титрование основано на реакциях образования
- 16. Спасибо за внимание!
Слайд 2Задачей качественного анализа является установление состава вещества, то есть выяснение из
Количественный анализ позволяет установить элементный и молекулярный состав исследуемого объекта или содержание отдельных его компонентов.
Слайд 3Качественный анализ
«Сухой» метод анализа
При выполнении анализа «сухим» методом исследуемые вещества и
Основан на способности некоторых элементов и их соединений (щелочные, щелочноземельные металлы, медь, бор и др.) окрашивать пламя в определенный цвет.
Присутствие ионов того или иного элемента обнаруживают по образованию соединений с характерным цветом или запахом.
Слайд 4«Мокрый» метод анализа
При анализе мокрым путем исследуемое вещество переводят в раствор,
Слайд 12Йодометрическое титрование
Иодометрическим титрованием называется титриметрический метод анализа, основанный на определении количества
Слайд 13Перманганатометрическое титрование
Перманганатометрическим титрованием называется
титриметрический метод анализа, основанный на использовании в качестве
Слайд 14Бихроматометрическое титрование
Бихроматометрией называется титриметрический метод анализа, основанный на использовании в качестве
Применение
Определение железа в различных пробах после предварительного восстановления его до Fe(II)
Восстановители анализируют по методу замещения. Например, Cu(I) реагирует с Fe(III) в кислой среде:
Cu+ + Fe3+ = Fe2+ + Cu2+
В результате реакции в растворе появляется количество ионов Fe2+, эквивалентное количеству Cu(I) в исходной пробе.
Окислители определяют методом обратного титрования.
Индикаторы
Дифениламин, дифениламинсульфоновая кислота, фенилантраниловая кислота
Слайд 15Комплексонометрическое титрование
Комплексонометрическое титрование основано на реакциях образования хелатных комплексов при взаимодействии
Реакции взаимодействия различных катионов с ЭДТА в растворе протекают по уравнениям:
Ca2+ + H2Y2- = CaY2- + 2H+,
Bi3+ + H2Y2- = BiY- + 2H+,
Zr4+ + H2Y2- = ZrY + 2H+.