- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Металлы побочной подгруппы 11 класс
Содержание
- 1. Презентация по химии на тему Металлы побочной подгруппы 11 класс
- 2. Положение хрома в ПСХЭ Д.И. Менделеева. Строение
- 3. Получение Из хромистого железняка
- 4. ПолучениеЧтобы получить чистый хром, реакцию ведут следующим
- 5. Физические свойства Устойчив на воздухе. При 2000 °C
- 6. Химические свойства В ряду напряжений хром находится
- 7. Применение Хром - постоянная составная часть растительных
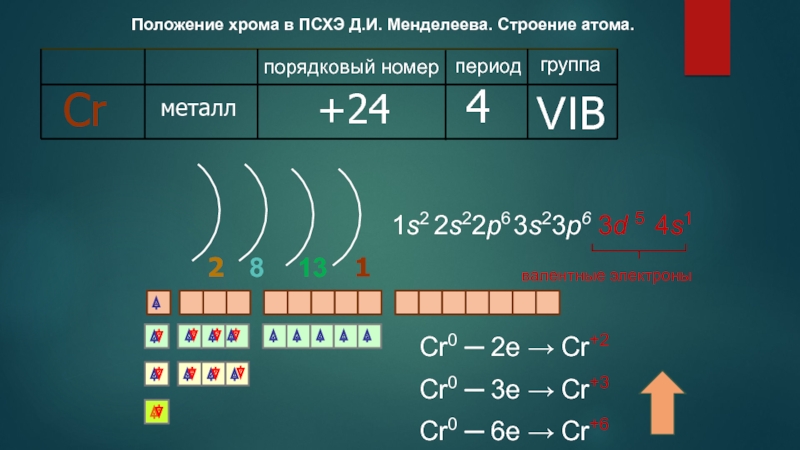
Положение хрома в ПСХЭ Д.И. Менделеева. Строение атома.периодгруппапорядковый номерCrметалл4VIB+24218валентные электроны131s22s22p64s13s23p63d 5Cr0 ─ 2e → Cr+2Cr0 ─ 3e → Cr+3Cr0 ─ 6e → Cr+6
Слайд 2Положение хрома в ПСХЭ Д.И. Менделеева. Строение атома.
период
группа
порядковый номер
Cr
металл
4
VIB
+24
2
1
8
валентные электроны
13
1s2
2s22p6
4s1
3s23p6
3d 5
Cr0
─ 2e → Cr+2
Cr0 ─ 3e → Cr+3
Cr0 ─ 6e → Cr+6
Слайд 3 Получение
Из хромистого железняка Fe(CrO2)2 (хромита железа) получают феррохром
восстановлением в электропечах коксом (углеродом):
Феррохром — сплав железа и хрома (около 60% ),
основные примеси – углерод (до5%) кремний (до 8%), сера (до 0,05 %),
фосфор (до 0,05 %).
Феррохром применяют для производства легированных
сталей.
Слайд 4Получение
Чтобы получить чистый хром, реакцию ведут следующим образом:
1) сплавляют хромит железа
с карбонатом натрия (кальцинированная сода) на воздухе:
4Fe(CrO2)2 + 8Na2CO3 + 7O2 → 8Na2CrO4 + 2Fe2O3 + 8CO2↑
2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата углём:
Na2Cr2O7 + 2C → Cr2O3 + Na2CO3 + CO↑
5) с помощью алюминотермии получают металлический хром:
Cr2O3 + 2Al → Al2O3 + 2Cr + 130 ккал
4Fe(CrO2)2 + 8Na2CO3 + 7O2 → 8Na2CrO4 + 2Fe2O3 + 8CO2↑
2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата углём:
Na2Cr2O7 + 2C → Cr2O3 + Na2CO3 + CO↑
5) с помощью алюминотермии получают металлический хром:
Cr2O3 + 2Al → Al2O3 + 2Cr + 130 ккал
Слайд 5Физические свойства
Устойчив на воздухе. При 2000 °C сгорает с образованием зелёного оксида
хрома (III) Cr2O3.
Плотность 7,19 г/см3;
t плавления 1890°С;
t кипения 2480°С
Плотность 7,19 г/см3;
t плавления 1890°С;
t кипения 2480°С
Слайд 6Химические свойства
В ряду напряжений хром находится левее водорода и поэтому
в
отсутствии воздуха может вытеснять водород из растворов
соляной и серной кислот, образуя соли хрома (II).
соляной и серной кислот, образуя соли хрома (II).
В присутствии кислорода
хром реагирует с растворами
кислот c образованием
солей хрома (III)
Слайд 7Применение
Хром - постоянная составная часть растительных и животных организмов. В
крови содержится от 0,012 до 0,0035 % хрома. Хром имеет большое значение в метаболизме углеводов и жиров, а также участвует в процессе синтеза инсулина.
Хром важный компонент во многих легированных сталях.
Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование)
Хром применяется для производства сплавов.
Хром важный компонент во многих легированных сталях.
Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование)
Хром применяется для производства сплавов.