- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Коррозия металлов
Содержание
- 1. Презентация по химии на тему Коррозия металлов
- 2. Слайд 2
- 3. Слайд 3
- 4. Слайд 4
- 5. Слайд 5
- 6. Слайд 6
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Слайд 11
- 12. ???
- 13. Коррозия металлов Подготовила: Умеренкова Т.И.
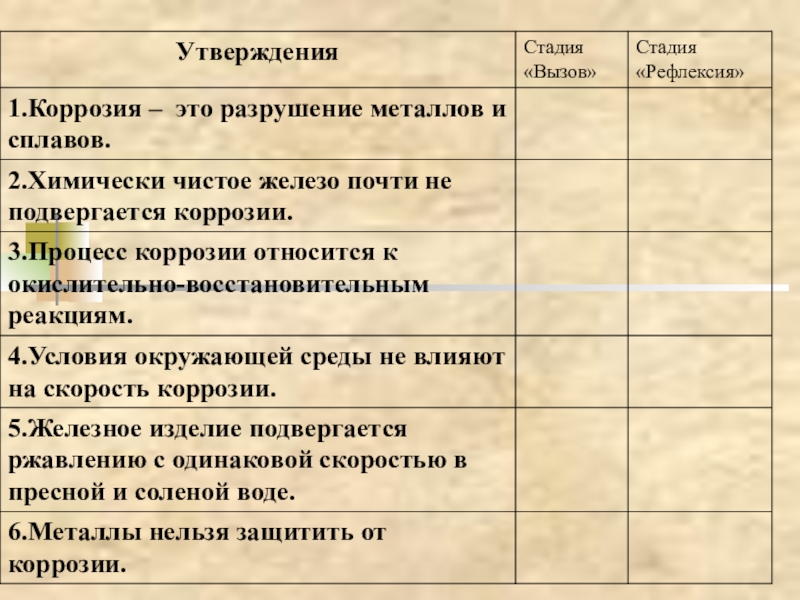
- 14. Слайд 14
- 15. «Знать – значит победить» А.Н.НесмеяновЦели урока:Познакомиться с
- 16. Коррозия – рыжая крыса, Грызет металлический
- 17. Путешествие в царство «Рыжего дьявола»
- 18. Этапы путешествияСтанция «Информационная»Станция «Историческая»Станция «Экспериментальная»Станция «Экологическая»Станция «Практическая»
- 19. Станция «Информационная»КОРРОЗИЯ – (от латинского corrodere –
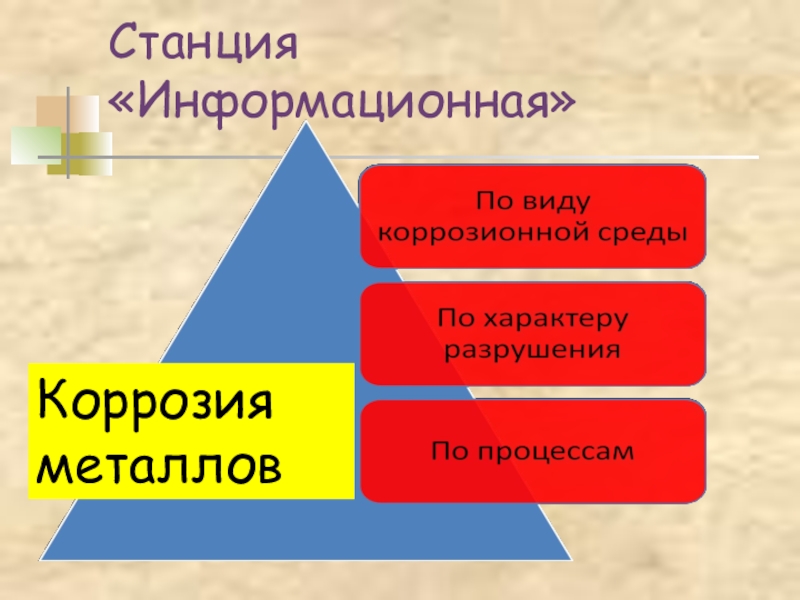
- 20. Станция «Информационная»Коррозияметаллов
- 21. Станция «Информационная»По виду коррозионной среды:газовая;жидкостная; атмосферная;почвенная.
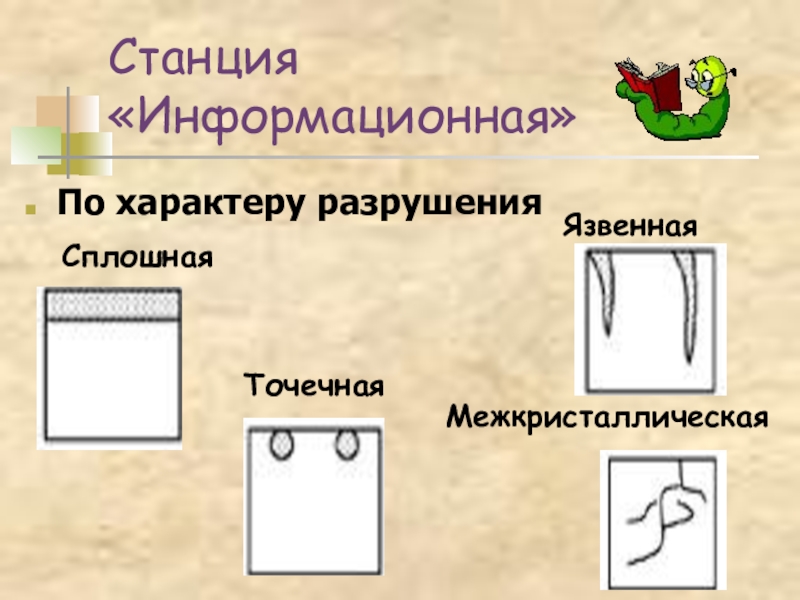
- 22. Станция «Информационная»По характеру разрушенияСплошнаяЯзвеннаяТочечнаяМежкристаллическая
- 23. Станция«Информационная»
- 24. Химическая коррозияЭтот вид коррозии наблюдается в процессе
- 25. Электрохимическая коррозияПроцесс происходит при соприкосновении двух металлов
- 26. Электрохимическая коррозия на контакте двух металлов
- 27. Электрохимическая коррозия железаFe →Fe(OH)2 →Fe(OH)3 →Fe2O3
- 28. Знаменитая Кутубская колонна в Индии близ Дели
- 29. Станция «Историческая»Люди издавна гадали:Как металлы уберечь?И
- 30. Станция «Историческая»Английские ученые Гемфри Деви и Майкл Фарадей - 19 век изучали электрофизическую коррозию
- 31. Станция «Историческая»Советские ученые А.И. Шултин и
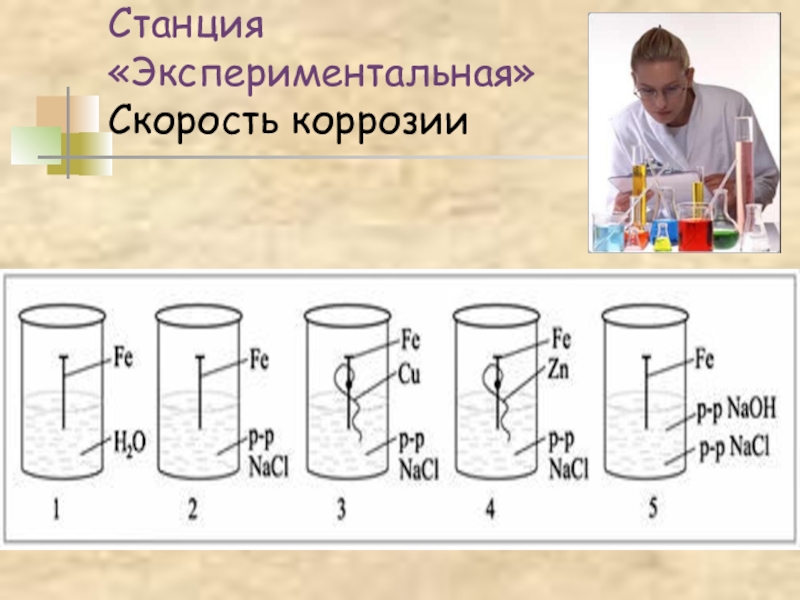
- 32. Станция «Экспериментальная» Скорость коррозии
- 33. Станция «Экологическая» Коррозия –результат и фактор
- 34. Станция «Экологическая» Коррозия –результат и фактор
- 35. Борьба с коррозией – борьба за окружающую
- 36. Станция «Практическая» Просто знать – еще
- 37. Станция «Практическая»
- 38. Станция «Практическая»Шлифование поверхностей изделия чтобы на них не задерживалась влага, провоцирующая процесс разрушения металлов.
- 39. Станция «Практическая» Применение легированных сплавов, содержащих
- 40. Нанесение защитных покрытий
- 41. Нанесение защитных покрытий Металлические – это
- 42. Слайд 42
- 43. Слайд 43
- 44. Слайд 44
- 45. Станция «Практическая»Электрохимические методы защиты: Анодная защита
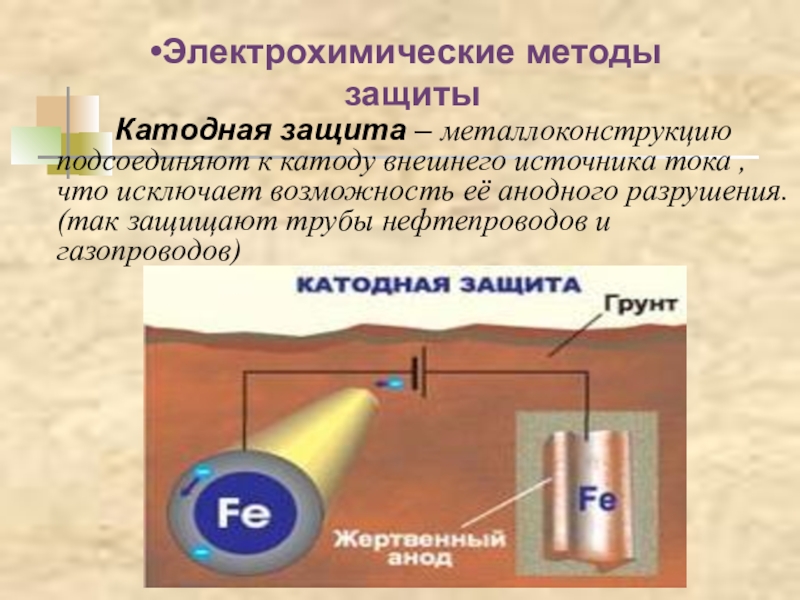
- 46. Электрохимические методы защитыПротекторная защита (анодная)- используются магний, алюминий, цинк
- 47. Электрохимические методы защиты
- 48. Введение веществ - ингибиторов, замедляющих коррозию.
- 49. « Стоп! Красный свет! »Коль хотите домой
- 50. «Стоп! Красный свет!»Вопросы:Что такое коррозия?Какие виды
- 51. Слайд 51
- 52. Слайд 52
- 53. Сегодня на уроке я:-Научился…………-Мне показалось важным…….-Я понял,
- 54. Кроссворд «Коррозия»1. Вид коррозии, связанный с
- 55. морхиическтеклэяафнржавлилшваниеторпкторхомбтоигнириемальСлово 1. Вид коррозии , связанный с
- 56. Домашнее задание7.2Описать практическое применение знаний о способах защиты металлов от коррозии
- 57. СпасибоМолодцы!
Слайд 15«Знать – значит победить»
А.Н.Несмеянов
Цели урока:
Познакомиться с сущностью коррозии;
Объяснить процессы, протекающие на
Научиться практически защищать металлы от коррозии.
Слайд 16
Коррозия – рыжая крыса,
Грызет металлический лом
В. Шефнер
Ржа ест железо
Рыжий дьявол - говорят о ней люди.
Слайд 18Этапы путешествия
Станция «Информационная»
Станция «Историческая»
Станция «Экспериментальная»
Станция «Экологическая»
Станция «Практическая»
Слайд 19Станция «Информационная»
КОРРОЗИЯ – (от латинского corrodere – разъедать)- самопроизвольное разрушение металлов
о + n
Ме – n е → Ме
Окисление металла
Слайд 21Станция «Информационная»
По виду коррозионной среды:
газовая;
жидкостная;
атмосферная;
почвенная.
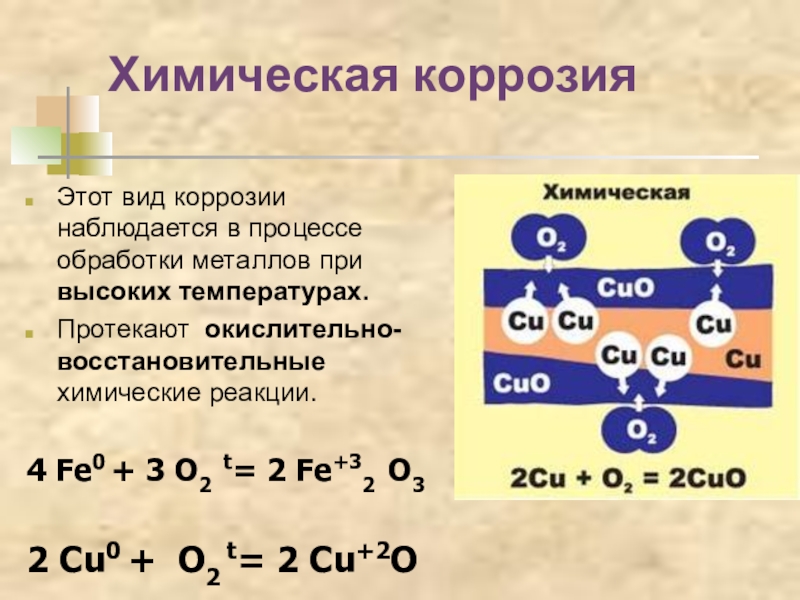
Слайд 24Химическая коррозия
Этот вид коррозии наблюдается в процессе обработки металлов при высоких
Протекают окислительно-восстановительные химические реакции.
4 Fe0 + 3 O2 t= 2 Fe+32 O3
2 Cu0 + O2 t= 2 Cu+2O
Слайд 25Электрохимическая коррозия
Процесс происходит при соприкосновении двух металлов в присутствии воды или
Более активный металл (анод) разрушается.
Скорость коррозии тем больше, чем сильнее отличаются металлы по своей активности.
Анод: Fe0 – 2e = Fe2+ окисление
Катод: 2H+ + 2e = H20 восстановление
Слайд 26Электрохимическая коррозия
на контакте двух металлов
Fe/Cu
0
Fe - 2ē ?Fe
разрушение
на меди:
+
2Н + 2ē ? H2↑
Zn/Fe
0 2+
Zn - 2ē ? Zn
разрушение
на железе :
+
2Н + 2ē ? H2 ↑
Слайд 28
Знаменитая Кутубская колонна в Индии близ Дели вот уже полторы тысячи
Слайд 29Станция
«Историческая»
Люди издавна гадали:
Как металлы уберечь?
И теорию создали, -
Вот о
Слайд 30Станция
«Историческая»
Английские ученые Гемфри Деви и Майкл Фарадей - 19 век
Слайд 31Станция
«Историческая»
Советские ученые
А.И. Шултин и
Я.В. Дурдин в 1935 году
Слайд 33Станция «Экологическая»
Коррозия –результат и фактор загрязнения окружающей среды
В мире ежегодно
0,6 млрд. т стали.
Уничтожается в результате коррозии
10-25 % от этой величины
Слайд 34Станция «Экологическая»
Коррозия –результат и фактор загрязнения окружающей среды
Интенсивность коррозии связана
Источник – промышленные зоны.
Слайд 35Борьба с коррозией – борьба за окружающую среду
Главная задача:
создание безотходных
процессов и технологических схем,
исключающих загрязнение биосферы
Слайд 37
Станция
«Практическая»
Способы защиты от коррозии
Шлифование поверхностей изделия
Применение химически
Нанесение защитных покрытий
Неметаллические
Химические
Металлические
Электрохимические методы защиты
Протекторная (анодная)
Катодная
Подавление влияния коррозионной среды
Использование ингибиторов
Деаэрация (удаление растворенного в воде кислорода
Слайд 38Станция
«Практическая»
Шлифование поверхностей изделия чтобы на них не задерживалась влага, провоцирующая
Слайд 39Станция
«Практическая»
Применение легированных сплавов, содержащих специальные добавки : хром, никель,
Слайд 40
Нанесение защитных покрытий
Неметаллические – неокисляющиеся масла, специальные лаки, краски, эмали.
Химические – искусственно создаваемые поверхностные плёнки: оксидные, нитридные, силицидные, полимерные и др. Например, все стрелковое оружие и детали многих точных приборов подвергают воронению – это процесс получения тончайшей плёнки оксидов железа на поверхности стального изделия.
Слайд 41Нанесение защитных покрытий
Металлические – это покрытие другими металлами, на поверхности
Нанесение хрома- хромирование,
никеля - никелирование,
цинка – цинкование.
Покрытием может служить и пассивный в химическом отношении металл – золото, серебро, медь.
Слайд 45Станция
«Практическая»
Электрохимические методы защиты:
Анодная защита (покрытие или прикрепление более активного
Катодная защита (покрытие менее активным металлом)
Электрозащита (нейтрализация возникающего тока постоянным током)
Слайд 46Электрохимические методы защиты
Протекторная защита (анодная)- используются магний, алюминий, цинк
Слайд 47Электрохимические методы защиты
Катодная защита –
Слайд 48
Введение веществ - ингибиторов, замедляющих коррозию. Примеры использования современных ингибиторов:
Удаление растворённого в воде кислорода - деаэрация. Этот процесс используют при подготовке воды, поступающей в котельные установки.
ПОДАВЛЕНИЕ ВЛИЯНИЯ КОРРОЗИОННОЙ СРЕДЫ
Слайд 49« Стоп! Красный свет! »
Коль хотите домой возвратиться,
То придется вам
Если сделана будет работа,
Я открою из царства ворота!
Рыжий дьявол
Слайд 50
«Стоп! Красный свет!»
Вопросы:
Что такое коррозия?
Какие виды коррозии вы знаете?
При каких условиях
Как можно замедлить коррозию?
Требуется скрепить железные детали. Какими заклепками следует пользоваться медными или цинковыми, чтобы замедлить коррозию железа? Ответ обоснуйте.
Контакты некоторых радиодеталей покрывают слоем золота, зачем это делается?
Слайд 53Сегодня на уроке я:
-Научился…………
-Мне показалось важным…….
-Я понял, что………..
Своей работой на уроке
-Доволен…..
-Не совсем доволен….
-Я не доволен потому, что…..
Слайд 54Кроссворд «Коррозия»
1. Вид коррозии, связанный с возникновением электрического тока.
2.
3. Неметаллическое покрытие от коррозии.
4. Коррозия железа и его сплавов.
5. Один из способов защиты изделия от коррозии.
6. Вещество, способное замедлять протекание химических процессов или останавливать их.
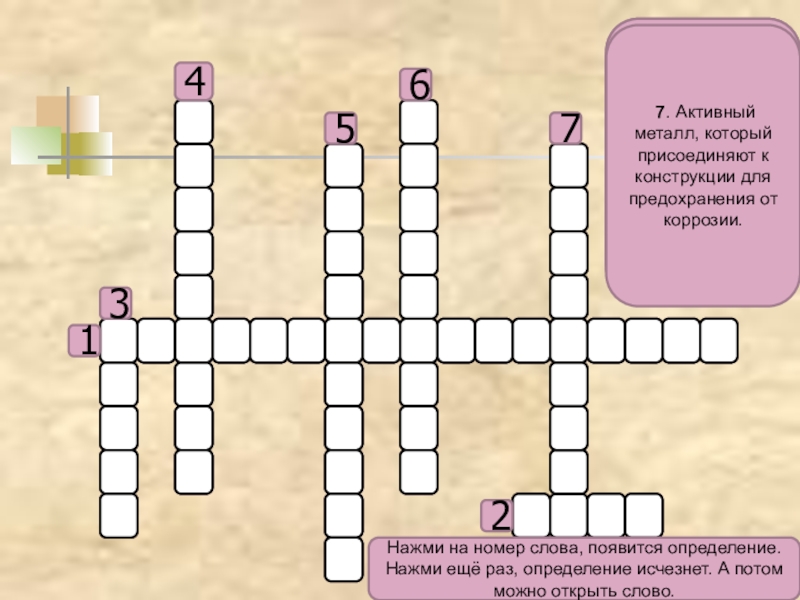
7. Активный металл, который присоединяют к конструкции для предохранения от коррозии.
Слайд 55м
о
р
х
и
и
ч
е
с
к
т
е
к
л
э
я
а
ф
н
р
ж
а
в
л
и
л
ш
в
а
н
и
е
т
о
р
п
к
т
о
р
х
о
м
б
т
о
и
г
н
и
р
и
е
м
а
л
ь
Слово 1.
Вид коррозии , связанный с возникновением электрического тока.
Слово 2.
Слово 3. Неметаллическое покрытие от коррозии.
1
3
4
2
5
6
7
Слово 5. Один из способов защиты изделия от коррозии.
Слово 4. Коррозия железа и его сплавов.
Слово 6 . Вещество, способное замедлять протекание химических процессов или останавливать их.
7. Активный металл, который присоединяют к конструкции для предохранения от коррозии.
Нажми на номер слова, появится определение. Нажми ещё раз, определение исчезнет. А потом можно открыть слово.