- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Кислород
Содержание
- 1. Презентация по химии на тему Кислород
- 2. Слайд 2
- 3. Слайд 3
- 4. Элемент № 8 OXYGENIUM КИСЛОРОД
- 5. Oxygenium C лат. оxygenium – “ рождающий
- 6. Английский ученый.В 1774 году разложениемoксида ртути (
- 7. Шведский ученый.В 1771 году провел опыты по
- 8. 1743 - 1794С целью
- 9. Слайд 9
- 10. Кислород занимает 1
- 11. В земной коре – 49 %(атмосфера, литосфера,
- 12. В 1774 г. А. Лавуазье доказал,
- 13. Выдыхаемый человеком воздух содержит ( в
- 14. Отличается от лесного воздуха наличием выбросов:
- 15. Химический знак – О
- 16. Химический элемент кислород образует два простых вещества,
- 17. Озон Жидкий озон имеетвид индигоПростейший озонаторВнутрь широкой
- 18. Способы собирания и обнаружения кислорода а –
- 19. 2 KMnO4 = K2MnO4 + MnO2 +
- 20. 2 Н2O2 = 2 Н2O + O2
- 21. Условия реакций – нагревание ( t )
- 22. Кислород получают из воздуха
- 23. 1. Отношение к простым веществам
- 24. 2. Отношение к сложным веществам При
- 25. Слайд 25
- 26. Условия, способствуюшие
- 27. Медленное окисление - химический процесс
- 28. Реакции веществ с кислородом - реакции окисления.
- 29. Кислород входит в состав воды, которая составляет
- 30. Кислород на
- 31. Слайд 31
- 32. Кислород расходуется в природе на процессы окисления
- 33. Приложение 1 «Вопросник к теме «Кислород»
- 34. Приложение 1 «Вопросник
- 35. Приложение 2 «Некоторые химические свойства озона.
Слайд 2
1. Элемент № 8
2. Oxygenium - 2. Oxygenium - Кислород
3. Джозеф Пристли
4. Карл Вильгельм Шееле
5. 5. Антуан Лоран Лавуазье
6. 6. Корнелиус Дреббел
7. Распространение 7. Распространение 7. Распространение элементов 7. Распространение элементов 7. Распространение элементов в 7. Распространение элементов в 7. Распространение элементов в земной коре
8. Нахождение кислорода в природе
9. Состав воздуха
10. Выдыхаемый воздух
11. Городской воздух
12. Общая характеристика элемента
13. Аллотропия кислорода
14. Озон
15. Способы 15. Способы 15. Способы собирания газа 15. Способы собирания газа, 15. Способы собирания газа, обнаружение
16. Получение 16. Получение 16. Получение кислорода в 16. Получение кислорода в 16. Получение кислорода в лаборатории из перманганата калия
17. Получение 17. Получение 17. Получение кислорода в лаборатории из пероксида водорода
(продолжение следует – см. следующий слайд)
СОДЕРЖАНИЕ
Слайд 3
( продолжение )
18. Некоторые реакции 18. Некоторые реакции, 18. Некоторые реакции, идущие с образованием кислорода
19. Получение 19. Получение 19. Получение кислорода в 19. Получение кислорода в 19. Получение кислорода в промышленности
20. Химические 20. Химические 20. Химические свойства кислорода 20. Химические свойства кислорода. 20. Химические свойства кислорода. Отношение к простым
веществам
21. Отношение кислорода к сложным веществам
22. Окислительное – восстановительная амфотерность
кислорода
23. Условия 23. Условия, 23. Условия, способствующие возникновению и прекращению
огня
24. Медленное окисление
25. Выводы по химическим свойствам кислорода 25. Выводы по химическим свойствам кислорода
26. Кислород – элемент жизни
27. Самая важная функция кислорода на Земле
28. Применение кислорода
29. Круговорот кислорода в природе
30. Приложение 1 30. Приложение 1 30. Приложение 1 «Вопросник к теме «Кислород»
31. Приложение 1 31. Приложение 1 31. Приложение 1 «Вопросник к теме «Кислород» (продолжение)
32. Приложение 2 «Некоторые химические свойства озона 32. Приложение 2 «Некоторые химические свойства озона. 32. Приложение 2 «Некоторые химические свойства озона. Применение озона»
Слайд 5Oxygenium
C лат. оxygenium – “ рождающий кислоту”
С греч. oxygenes
Название кислороду Oxygenium
дал А. Лавуазье
Слайд 6
Английский ученый.
В 1774 году разложением
oксида ртути ( II )
получил кислород
и
изучил
2HgO = 2Hg + O2↑
1733 - 1804
ДЖОЗЕФ ПРИСТЛИ
Слайд 7
Шведский ученый.
В 1771 году провел опыты
по разложению
оксида ртути (
изучил свойства
образующегося газа.
Однако результаты
его исследований
были опубликованы
лишь в 1777 году.
1742 - 1786
КАРЛ ВИЛЬГЕЛЬМ ШЕЕЛЕ
Слайд 8
1743 - 1794
С целью проверки опытов
Шееле и
в 1774 году получил кислород,
установил его природу и изучил
его способность соединяться
с фосфором и серой при горении
и металлами при обжиге.
Изучил состав атмосферного воздуха.
Создал кислородную теорию горения.
Совместно с Ж. Менье установил
сложный состав воды и получил
воду из кислорода и водорода.
2H2 + O2 = 2H2O
Лавуазье показал, что процесс дыхания
подобен процессу горения.
АНТУАН ЛОРАН ЛАВУАЗЬЕ
Слайд 9
КОРНЕЛИУС
Голландский алхимик и технолог.
Получил кислород примерно за 150 лет
до Пристли и Шееле при нагревании нитрата калия:
2КNO3 = 2KNO2 + O2 ↑
Его открытие было засекречено, т.к. использование полученного газа предполагалось для дыхания людей на подводных лодках
1572 - 1633
Слайд 10
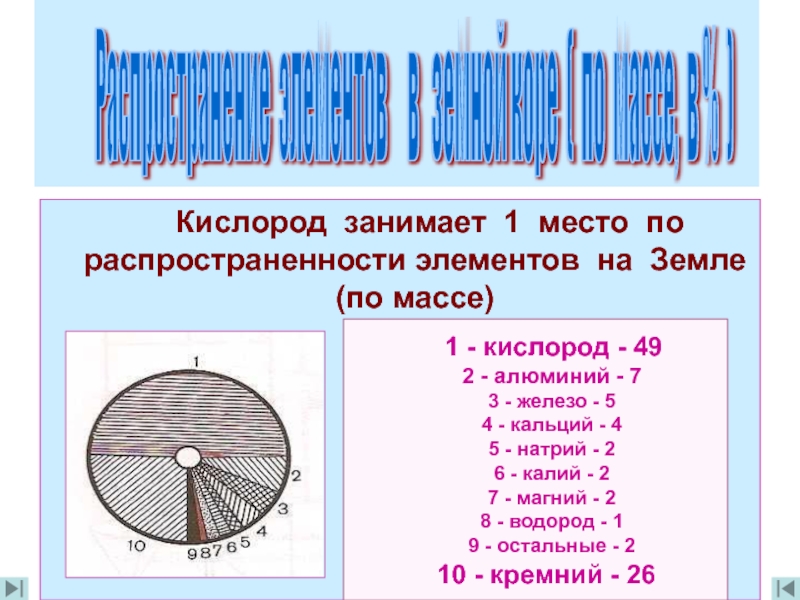
Кислород занимает 1 место по распространенности элементов
Распространение элементов в земной коре ( по массе, в % )
1 - кислород - 49
2 - алюминий - 7
3 - железо - 5
4 - кальций - 4
5 - натрий - 2
6 - калий - 2
7 - магний - 2
8 - водород - 1
9 - остальные - 2
10 - кремний - 26
Слайд 11
В земной коре – 49 %
(атмосфера, литосфера, гидросфера)
В воздухе –
В воде
(в чистой воде – 88,8 %, в морской воде – 85,8 % )
В песке , многих горных породах и минералах
В составе органических соединений:
белков, жиров, углеводов и др.
В организме человека – 62 %
Нахождение кислорода в природе ( по масее, в % )
Слайд 12 В 1774 г. А. Лавуазье доказал, что воздух – это
СОСТАВ ВОЗДУХА
Сжигание фосфора
под колоколом:
а – горение фосфора;
б – уровень воды
поднялся на 1 / 5 объема
Примечание
К другим газам (1%) относятся:
углекислый газ (0,03%);
инертные газы
( в основном аргон - 0,93% );
водяные пары
Кислород - 21%
Азот - 78%
Другие газы -1%
( по объему, в % )
Слайд 13
Выдыхаемый человеком воздух
содержит ( в %, по объему)
Выдыхаемый воздух
1 – Кислород 16%
2 – Углекислый газ 4%
3 – Остальное: азот,
водяные пары и пр.
Слайд 14
Отличается от лесного воздуха наличием выбросов:
от автотранспорта ( в Москве - 90% всех загрязнений)
от котельных установок
от промышленных предприятий
Автомашины выбрасывают в атмосферу:
углекислый газ СО2, сернистый газ SO2, оксиды азота NO и NO2 , угарный газ СО, формальдегид НСОН, а также сажу
Металлургические предприятия выбрасывают в воздух:
сернистый газ, угарный газ, формальдегид, циановодород НСN
Алюминиевые заводы
фтороводород НF
Целлюлозно – бумажныые комбинаты
сероводород, хлор, фенол C6H5OH и формальдегид
,
Городской воздух
Слайд 15
Химический знак – О
Относительная атомная масса: Ar = 16
Изотопы кислорода – ( 99,75 %), ,
Строение атома: ( 8p+ + 8n0 ) + 8
Заряд ядра: ( +8)
Электронная конфигурация атома: 1s22s2 2p4
Типичный неметалл. Сильный окислитель ( по электроотрицательности уступает лишь фтору )
Валентные возможности: в соединениях обычно 2-х валентен, реже – 3-х, (4-х) валентен
Возможные степени окисления: - 2 , - 1 , 0 , + 2, (+4)
(наиболее характерные степени окисления: 0, - 2)
Общая характеристика элемента
Слайд 16
Химический элемент кислород образует два простых вещества, аллотропа - кислород О2
Аллотропия кислорода
t, либо УФ-
О3 = О2 + О
3О2 <═> 2О3 - Q
Свет
6СО2+ 6Н2О = С6Н12О6 + 6О2
Слайд 17
Озон
Жидкий озон имеет
вид индиго
Простейший озонатор
Внутрь широкой стеклянной трубки
вставлена проволока.
обмотана другой проволокой. Если
к концам двух проволок приложить
напряжение в несколько тысяч вольт,
а через трубку пропустить кислород,
то выходящий из нее газ будет соде-
ржать несколько процентов озона.
Озон образуется в атмосфере на высоте 10-30 км
при действием УФ излучения на воздух
и при грозовых разрядах
Слайд 18
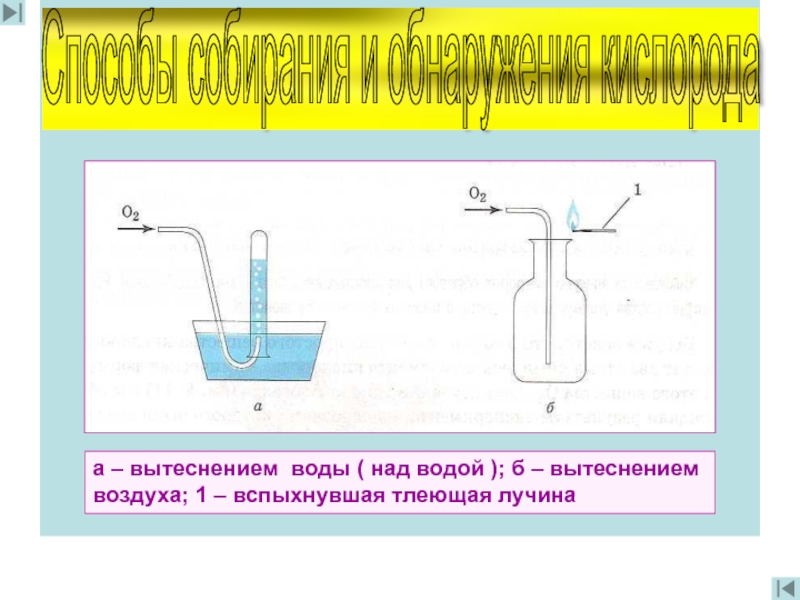
Способы собирания и обнаружения кислорода
а – вытеснением воды ( над
Слайд 19
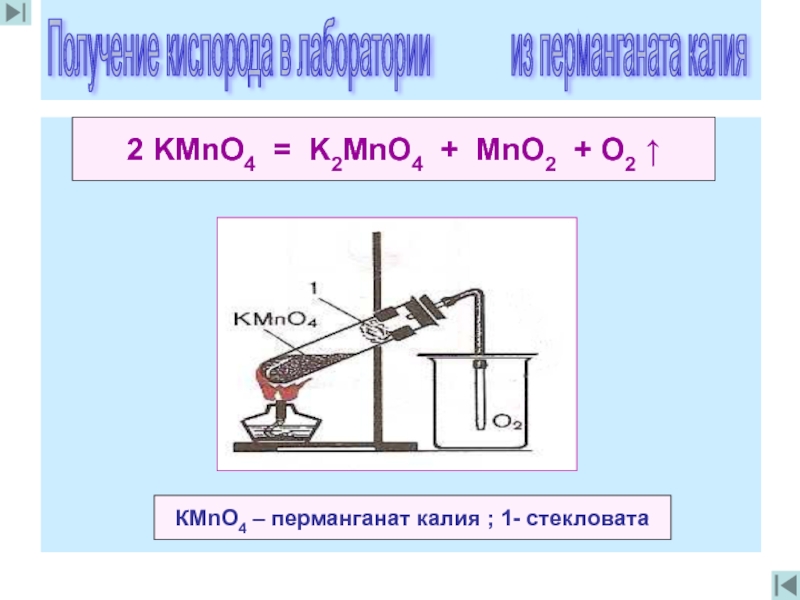
2 KMnO4 = K2MnO4 + MnO2 + O2 ↑
КМnO4 – перманганат
Получение кислорода в лаборатории из перманганата калия
Слайд 20
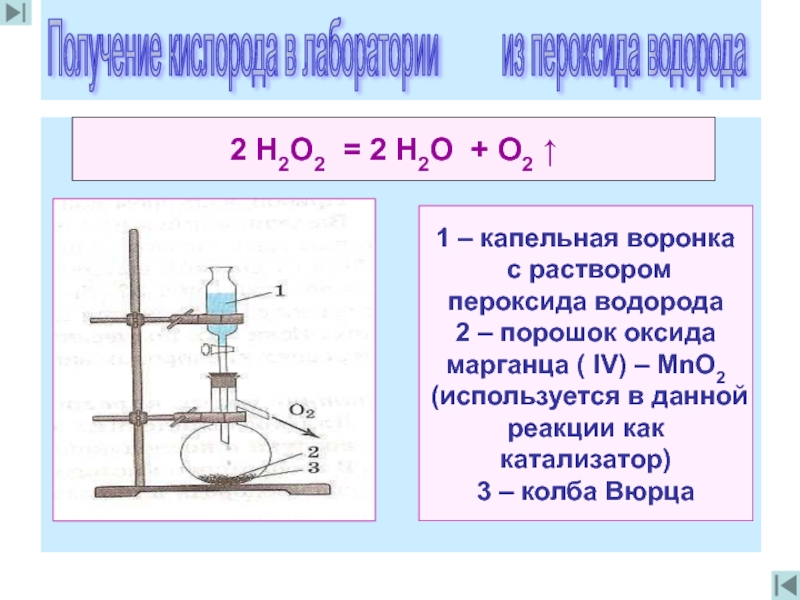
2 Н2O2 = 2 Н2O + O2 ↑
1 – капельная воронка
пероксида водорода
2 – порошок оксида
марганца ( IV) – МnO2
(используется в данной
реакции как катализатор)
3 – колба Вюрца
Получение кислорода в лаборатории из пероксида водорода
Слайд 21
Условия реакций – нагревание ( t )
2 КМnО4 = К2МnО4 + МnO2 + О2 ↑
2КСlО3 = 2КСl + О2 ↑ 2НgO = 2Hg + О2 ↑
3РbO2 = Рb3O4 + О2 ↑ 2КNO3 = 2КNO2 + О2 ↑
Условия реакции – присутствие катализатора ( K )
2Н2О2 = 2Н2О + О2 ↑ ( К – МnО2 )
Условия реакции – действие электрического тока ( )
(р. электролиза )
2Н2О = 2Н2 ↑ + О2 ↑
Некоторые реакции, идущие с образованием кислорода
Слайд 22 Кислород получают из воздуха
газовой ректификацией
Воздух охлаждают
Далее жидкий воздух подвергают перегонке
Жидкий азот испаряется при – 196 ОС
( t кип. жидкого азота)
Жидкий кислород испаряется при – 183 ОС
( t кип. жидкого кислорода)
Газообразный кислород хранят в стальных баллонах, окрашенных в голубой цвет, под давлением 1 - 1,5 МПА
Получение в промышленности
Слайд 23
1. Отношение к простым веществам
Химические свойства
Реакции окисления, сопровождающиеся выделением теплоты и света,
называют горением (вещества при этом воспламеняются)
Реакции окисления без горения
2Cu + O2 ═ 2CuO + Q
Воспламенения меди не происходит
В реакциях окисления, как правило, образуются оксиды
t
t
t
t
t
t
( FeО · Fe2О3 )
t
Слайд 24
2. Отношение к сложным веществам
При полном сгорании углеводородов
образуются оксиды -
СН4 + 2О2 = СО2 + 2Н2О + Q
метан
2С2Н2 + 5О2 = 4СО2 + 2Н2О + Q
ацетилен
При неполном сгорании углеводородов
(например, при недостатке кислорода О2) образуются еще угарный газ СО и сажа С:
2СН4 + 3О2 = 2СО + 4Н2О + Q
СН4 + О2 = С + 2Н2О + Q
t
t
t
t
Слайд 25
О - как окислитель : О0 + 2 → О–2 (1)
( как правило )
О - как восстановитель : О0 - 2 → О+2 (2)
( например, в реакции со F2 )
2Mg + O2 = 2MgO ( 1 )
C + О2 = CО2 ( 1 )
2F2 + О2 = 2F2О ( 2 )
Окислительно - восстановительная амфотерность кислорода
Слайд 27
Медленное окисление - химический процесс медленного взаимодействия вещества
В ходе этого процесса теплота выделяется постепенно и вещество не нагревается до температуры воспламенения
Примеры:
В процессах окисления (аэробного распада)
некоторых веществ пищи и продуктов обмена веществ в клетках и тканях живых организмов выделяется энергия, нужная организму
В процессе гниения (окисления) навоза выделяется теплота и др.
Медленное окисление
Слайд 28
Реакции веществ с кислородом - реакции окисления.
Реакции окисления
– восстановительных реакций (ОВР)
Преобладающая функция кислорода – окислительная.
При комнатной температуре О2 – малоактивен, при высокой – сильный окислитель
В реакциях окисления, как правило, получаются оксиды (ЭО )
Реакции окисления, сопровождающиеся воспламенением вещества, - реакции горения
Реакции горения всегда – экзотермические реакции (+ Q )
Медленное окисление - химический процесс медленного взаимодействия вещества с кислородом без воспламенения вещества
Выводы по химическим свойствам
Слайд 29
Кислород входит в состав воды, которая составляет большую часть массы живых
Кислород входит в состав биологически важных молекул, образующих живую материю
(белки, углеводы, жиры, гормоны, ферменты и др. )
Кислород в виде простого вещества О2 необходим как окислитель для протекания реакций, дающих клеткам необходимую для жизнедеятельности энергию
Кислород - элемент жизни
Слайд 30
Кислород на Земле является
т.к он обеспечивает протекание
таких важных процессов, как:
дыхание всех живых организмов
гниение органических масс
(помимо воздействия грибов и бактерий)
горение веществ
Какая cамая важная функция у кислорода на Земле ?
Слайд 31
В чистом виде:
В металлургии – при получении чугуна, стали, цветных металлов ( для интенсификации окислительных процессов)
Во многих химических производствах
Как жидкий окислитель для ракет
При резке и сварке металлов и сплавов
В медицине - для приготовления лечебных водных и воздушных ванн, лечебных коктейлей
В медицине - в кислородных подушках
В чистом виде и в составе смесей:
На космических кораблях, подводных лодках в подводном плавании, на больших высотах
В составе воздуха:
Для сжигания топлива (в двигателях автомобилей, тепловозов, теплоходов; на тепловых электростанциях, на многих производствах и др.)
Применение кислорода
Слайд 32
Кислород расходуется в природе на процессы окисления
(дыхания,
Масса кислорода в воздухе пополняется в ходе процесса фотосинтеза
свет
6СО2 + 6 Н2О = С6Н12О6 +6О2 ↑
Круговорот кислорода в природе
Слайд 33
Приложение 1 «Вопросник к теме «Кислород»
1. Назовите восьмой
2. Кем2. Кем 2. Кем и когда был2. Кем и когда был 2. Кем и когда был открыт кислород? (слайды № 2. Кем и когда был открыт кислород? (слайды № 62. Кем и когда был открыт кислород? (слайды № 6 -2. Кем и когда был открыт кислород? (слайды № 6 - 92. Кем и когда был открыт кислород? (слайды № 6 - 9)
3. Почему элемент № 3. Почему элемент № 83. Почему элемент № 8 был назван кислородом3. Почему элемент № 8 был назван кислородом? (3. Почему элемент № 8 был назван кислородом? (слайд № 3. Почему элемент № 8 был назван кислородом? (слайд № 53. Почему элемент № 8 был назван кислородом? (слайд № 5)
4. Где4. Где 4. Где и4. Где и 4. Где и в 4. Где и в 4. Где и в каком виде (свободном или связанном) кислород4. Где и в каком виде (свободном или связанном) кислород
встречается в природе встречается в природе? встречается в природе? (слайды № встречается в природе? (слайды № 10 встречается в природе? (слайды № 10 - 1 встречается в природе? (слайды № 10 - 11 встречается в природе? (слайды № 10 - 11)
5. Каков состав атмосферного воздуха? (слайд № 5. Каков состав атмосферного воздуха? (слайд № 125. Каков состав атмосферного воздуха? (слайд № 12)
6. Каков состав выдыхаемого человеком воздуха?6. Каков состав выдыхаемого человеком воздуха? 6. Каков состав выдыхаемого человеком воздуха? (слайд №6. Каков состав выдыхаемого человеком воздуха? (слайд №13)
7. Перечислите известные вам загрязнители воздуха? (слайд № 7. Перечислите известные вам загрязнители воздуха? (слайд № 147. Перечислите известные вам загрязнители воздуха? (слайд № 14)
8. Дайте характеристику кислороду как химическому элементу (слайд №8. Дайте характеристику кислороду как химическому элементу (слайд №15)
9. Какие аллотропные модификации кислорода вам известны? (слайд №9. Какие аллотропные модификации кислорода вам известны? (слайд №16)
10. Какими примечательными свойствами обладает озон в отличие от кислорода?10. Какими примечательными свойствами обладает озон в отличие от кислорода? 10. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности10. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности?10. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности? (слайды № 10. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности? (слайды № 16-1710. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности? (слайды № 16-17, 3510. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности? (слайды № 16-17, 35 10. Какими примечательными свойствами обладает озон в отличие от кислорода? Какие свойства озона использует человек в своей практической деятельности? (слайды № 16-17, 35 )
11. На каких физических свойствах кислорода основаны способы На каких физических свойствах кислорода основаны способы На каких физических свойствах кислорода основаны способы собирания егоНа каких физических свойствах кислорода основаны способы собирания его? На каких физических свойствах кислорода основаны способы собирания его? Как можно обнаружить кислород?На каких физических свойствах кислорода основаны способы собирания его? Как можно обнаружить кислород? На каких физических свойствах кислорода основаны способы собирания его? Как можно обнаружить кислород? (слайд № На каких физических свойствах кислорода основаны способы собирания его? Как можно обнаружить кислород? (слайд № 1На каких физических свойствах кислорода основаны способы собирания его? Как можно обнаружить кислород? (слайд № 18На каких физических свойствах кислорода основаны способы собирания его? Как можно обнаружить кислород? (слайд № 18)
Слайд 34 Приложение 1 «Вопросник к теме «Кислород»
12. Как кислород12. Как кислород 12. Как кислород получают в лаборатории12. Как кислород получают в лаборатории? 12. Как кислород получают в лаборатории? (слайды № 12. Как кислород получают в лаборатории? (слайды № 112. Как кислород получают в лаборатории? (слайды № 19 - 2112. Как кислород получают в лаборатории? (слайды № 19 - 21)
13. Как кислород получают в промышленности13. Как кислород получают в промышленности? 13. Как кислород получают в промышленности? (слайд № 2213. Как кислород получают в промышленности? (слайд № 22)
14. Перечислите важнейшие химические свойства кислорода14. Перечислите важнейшие химические свойства кислорода. 14. Перечислите важнейшие химические свойства кислорода. Что такое окисление14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? 14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты,14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты, как правило14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты, как правило,14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты, как правило, получаются в реакциях окисления14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты, как правило, получаются в реакциях окисления 14. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты, как правило, получаются в реакциях окисления веществ кислородом? (слайды № 23 - 2414. Перечислите важнейшие химические свойства кислорода. Что такое окисление? Какие продукты, как правило, получаются в реакциях окисления веществ кислородом? (слайды № 23 - 24)
15. Что понимается под окислительно – восстановительными способностями15. Что понимается под окислительно – восстановительными способностями 15. Что понимается под окислительно – восстановительными способностями кислорода? Какие функции преобладают у него15. Что понимается под окислительно – восстановительными способностями кислорода? Какие функции преобладают у него? 15. Что понимается под окислительно – восстановительными способностями кислорода? Какие функции преобладают у него? Приведите примеры (слайд № 2515. Что понимается под окислительно – восстановительными способностями кислорода? Какие функции преобладают у него? Приведите примеры (слайд № 25)
16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше,16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше, чем на воздухе16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше, чем на воздухе? 16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше, чем на воздухе? (слайд №16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше, чем на воздухе? (слайд № 16. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше, чем на воздухе? (слайд № 2616. Какие условия способствуют возникновению и прекращению горения? Почему скорость горения веществ в кислороде выше, чем на воздухе? (слайд № 26)
17. Чем отличаются процессы горения и медленного окисления? (слайд № 2717. Чем отличаются процессы горения и медленного окисления? (слайд № 27)
18. Какие выводы можно сделать по химическим свойствам кислорода? 18. Какие выводы можно сделать по химическим свойствам кислорода? 18. Какие выводы можно сделать по химическим свойствам кислорода? (слайд № 2818. Какие выводы можно сделать по химическим свойствам кислорода? (слайд № 28)
19. Почему кислород относят к «элементам жизни»19. Почему кислород относят к «элементам жизни»? 19. Почему кислород относят к «элементам жизни»? (слайд № 29)
20. Какая самая важная функция у кислорода на Земле20. Какая самая важная функция у кислорода на Земле?20. Какая самая важная функция у кислорода на Земле? (слайд № 3020. Какая самая важная функция у кислорода на Земле? (слайд № 30)
21. Перечислите области применения кислорода21. Перечислите области применения кислорода 21. Перечислите области применения кислорода (слайд № 3121. Перечислите области применения кислорода (слайд № 31)
22. Как вы понимаете сущность круговорота22. Как вы понимаете сущность круговорота 22. Как вы понимаете сущность круговорота кислорода в природе? (слайд № 3222. Как вы понимаете сущность круговорота кислорода в природе? (слайд № 32)
Слайд 35Приложение 2 «Некоторые химические свойства озона. Применение озона»
Окислительная активность озона
Например, уже при об. у. он окисляет многие малоактивные простые вещества ( Ag, Hg и пр.):
8Аg + 2О3 = 4Ag2О + О2
При действии на щелочные металлы и некоторые щелочи
образует озониды:
К + О3 = КО3
4КОН + 4О3 = 4КО3 + О2 + Н2О
Качественно и количественно озон определяется с помощью
следующей реакции:
2KI + Н2О + О3 = 2КОН + I2 + О2
Восстановленный йод обнаруживают с помощью крахмального
клейстера.
Озон используется для обеззараживании воды и воздуха, дезодориро-вания продуктов питания, как бактерицидное средство при лечении некоторых заболеваний человека, отбеливания тканей и масел, в раз-личных химических синтезах.