никоим образом научиться невозможно, не видав самой практики и не принимаясь за химические операции. (М.В. Ломоносов)
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Ионные реакции
Содержание
- 1. Презентация по химии на тему Ионные реакции
- 2. Домашнее задание§37, понятия 1-3, упр.1-3 (письменно) стр.209
- 3. Ионные уравненияЦель: выяснить, какие реакции называют реакциями ионного обмена, какие уравнения называют ионными уравнениями реакций.
- 4. Цель: выяснить, какие реакции называют реакциями ионного
- 5. Запись уравнений реакций ионного обмена в формах:Молекулярной
- 6. Слайд 6
- 7. Слайд 7
- 8. Практическая работа №4-5 «Ионные реакции. Условия протекания
- 9. Задача 1: докажем, что в растворе
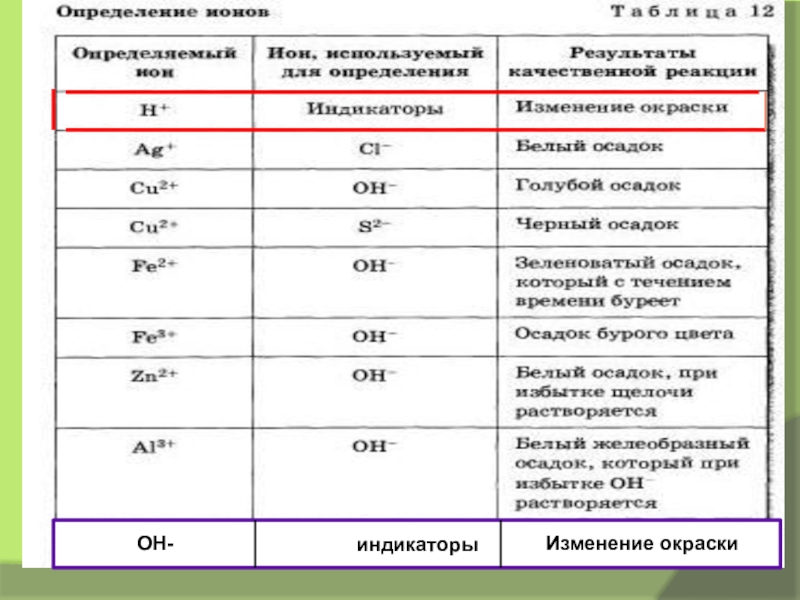
- 10. индикаторыОН-Изменение окраски
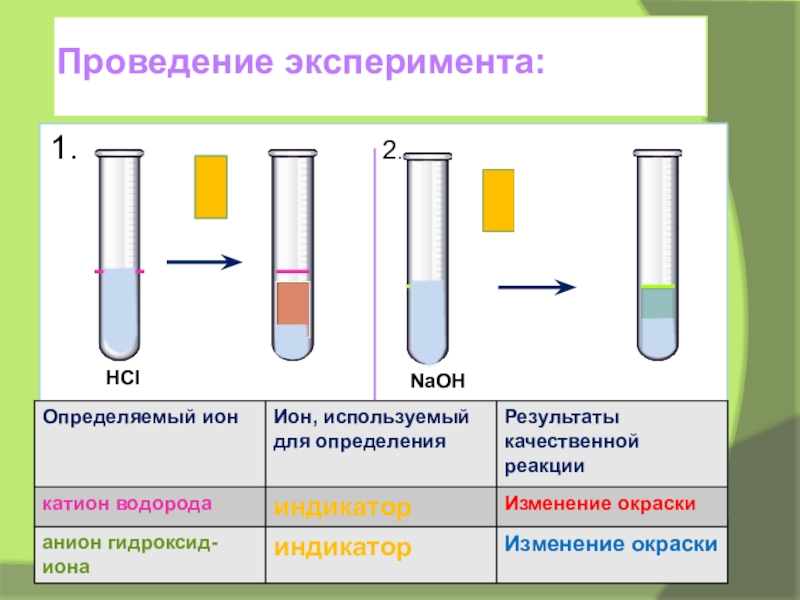
- 11. Проведение эксперимента: 1.2.HClNaOH
- 12. Описание эксперимента 1.Берём: соляная кислота и универсальный
- 13. Описание эксперимента 1.Берём: гидроксид натрия и универсальный
- 14. Задача 2. Доказать, что реакции
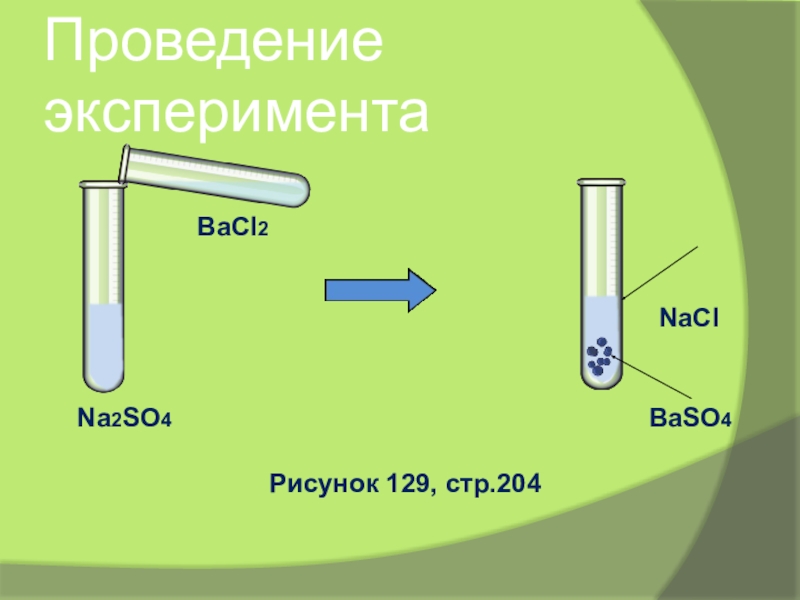
- 15. Проведение экспериментаNa2SO4BaCl2NaClBaSO4Рисунок 129, стр.204
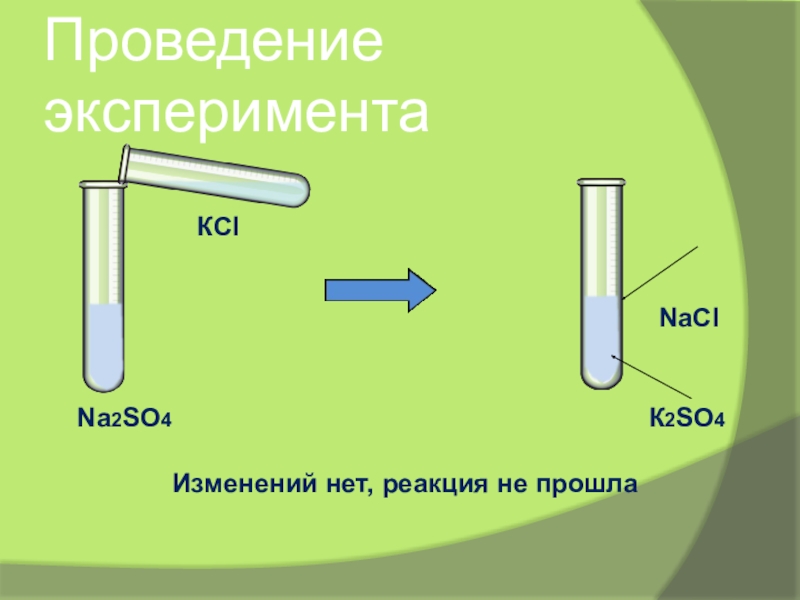
- 16. Проведение экспериментаNa2SO4КClNaClК2SO4Изменений нет, реакция не прошла
- 17. Описание эксперимента 1.Берём: сульфат натрия и хлори
- 18. Описание эксперимента 1.Берём: сульфат натрия и хлорид
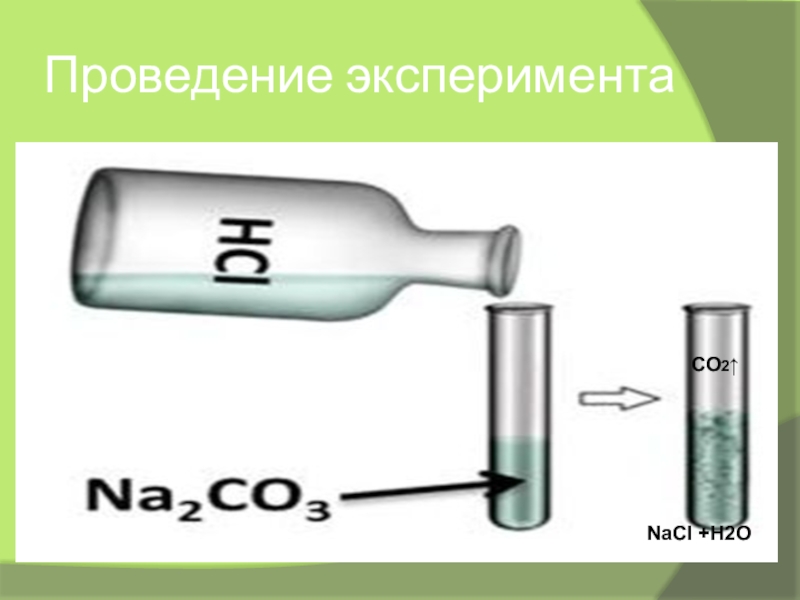
- 19. Проведение экспериментаNaCl +H2OCO2↑
- 20. Описание эксперимента 1.Берём: карбонат натрия и соляную
- 21. Проведение экспериментаNaОН + фенолфталеинHClNaClH2OОкраска индикатора обесцветилась, реакция прошла
- 22. Описание эксперимента 1.Берём: гидроксид натрия, фенолфталеин и
Домашнее задание§37, понятия 1-3, упр.1-3 (письменно) стр.209
Слайд 1Ионные уравнения.
ПР №4-5 «Ионные реакции», «Условия протекания химических реакций между растворами»
Химии
Слайд 3Ионные уравнения
Цель: выяснить, какие реакции называют реакциями ионного обмена, какие уравнения
называют ионными уравнениями реакций.
Слайд 4Цель: выяснить, какие реакции называют реакциями ионного обмена, какие уравнения называют
ионными уравнениями реакций.
Задание: 1) прочтите текст на стр.203, о каких понятиях говорится в тексте?
Ответьте на вопросы:
1) Почему реакции в растворах электролитов протекают между ионами, а не между молекулами?
2) Какие вещества нельзя записывать в ионном виде?
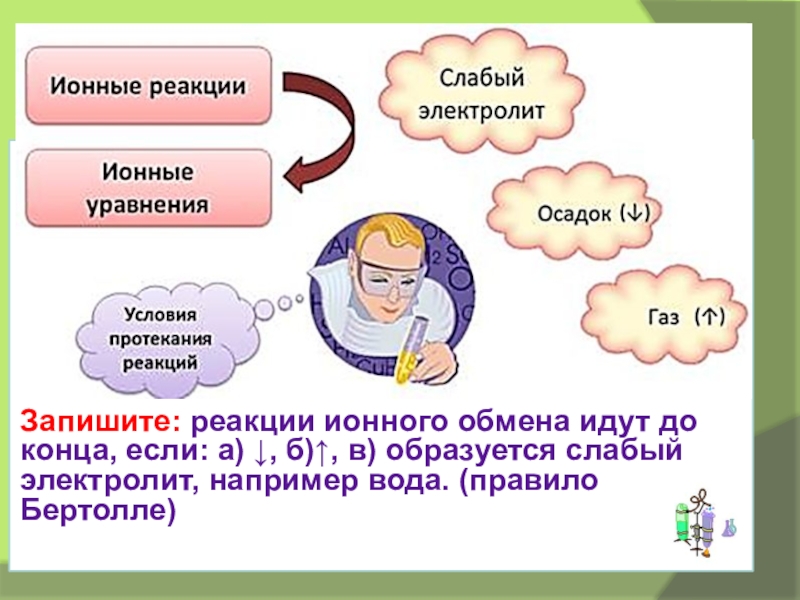
Запишите: реакции ионного обмена идут до конца, если: а) ↓, б)↑, в) образуется слабый электролит, например вода. (правило Бертолле)
Слайд 5Запись уравнений реакций ионного обмена в формах:
Молекулярной форме;
Полной ионной форме;
Краткой ионной
форме, которая показывает суть реакции ионного обмена
Слайд 8Практическая работа №4-5
«Ионные реакции. Условия протекания химических реакций между растворами»
Работаем в тетради для
практических работ
практических работ
Слайд 9
Задача 1: докажем, что в растворе электролитов содержатся ионы:
В растворах кислот
всегда есть катионы водорода;
В растворах щелочей всегда есть анионы гидроксид – ионов.
Как доказать?
Таблица 12 стр. 238-239
В растворах щелочей всегда есть анионы гидроксид – ионов.
Как доказать?
Таблица 12 стр. 238-239
Слайд 12Описание эксперимента
1.Берём: соляная кислота и универсальный индикатор
2.Наблюдаем: окраска индикатора из жёлтой
стала красной
3.Вывод: в растворе кислоты присутствуют ионы водорода:
HCl=H+ + Cl-
3.Вывод: в растворе кислоты присутствуют ионы водорода:
HCl=H+ + Cl-
Слайд 13Описание эксперимента
1.Берём: гидроксид натрия и универсальный индикатор
2.Наблюдаем: окраска индикатора из жёлтой
стала синей
3.Вывод: в растворе щелочи присутствуют гидроксид-ионы:
NaOH=Na+ + OH-
3.Вывод: в растворе щелочи присутствуют гидроксид-ионы:
NaOH=Na+ + OH-
Слайд 14
Задача 2. Доказать, что реакции между электролитами протекают при условии:
если
образуется осадок;
Если выделяется газ;
Если образуется вода (слабый электролит).
Если выделяется газ;
Если образуется вода (слабый электролит).
Слайд 17Описание эксперимента
1.Берём: сульфат натрия и хлори бария
2.Наблюдаем: выпал белый мелкий осадок
(хим.молоко)
3.Вывод: реакция прошла, т.к. выпал осадок
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное. Стр.204.
3.Вывод: реакция прошла, т.к. выпал осадок
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное. Стр.204.
Слайд 18Описание эксперимента
1.Берём: сульфат натрия и хлорид калия
2.Наблюдаем: изменений нет
3.Вывод: реакция не
прошла
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное.
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное.
Слайд 20Описание эксперимента
1.Берём: карбонат натрия и соляную кислоту
2.Наблюдаем: выделение газа
3.Вывод: реакция идёт,
т.к. выделяется газ↑
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное. Стр. 207
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное. Стр. 207
Слайд 21Проведение эксперимента
NaОН + фенолфталеин
HCl
NaCl
H2O
Окраска индикатора обесцветилась,
реакция прошла
Слайд 22Описание эксперимента
1.Берём: гидроксид натрия, фенолфталеин и соляную кислоту
2.Наблюдаем: окраска фенолфталеина в
щелочи исчезла
3.Вывод: идёт реакция нейтрализации между щелочью и кислотой с образованием соли и воды. (стр.206)
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное. Стр. 205
3.Вывод: идёт реакция нейтрализации между щелочью и кислотой с образованием соли и воды. (стр.206)
4. Пишем уравнение: молекулярное, полное ионное и краткое ионное. Стр. 205