- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Химические источники тока. Электролиз
Содержание
- 1. Презентация по химии на тему: Химические источники тока. Электролиз
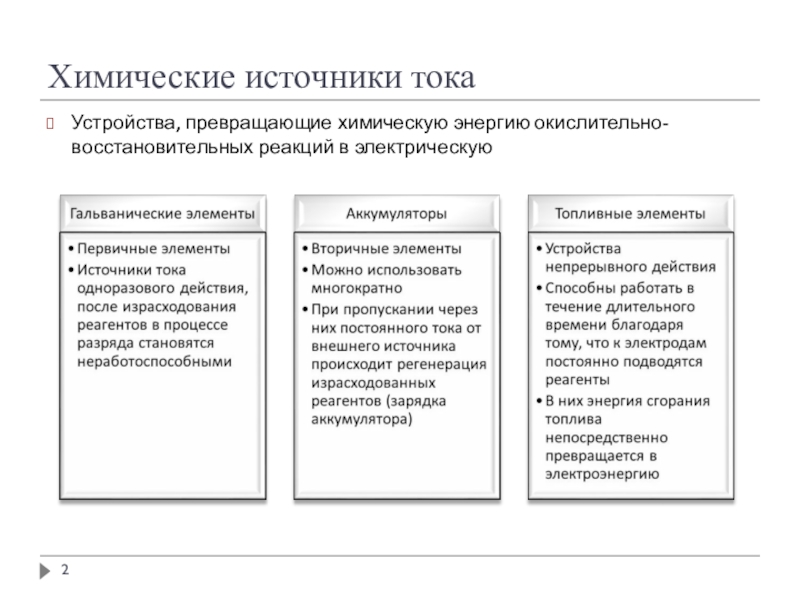
- 2. Химические источники токаУстройства, превращающие химическую энергию окислительно-восстановительных реакций в электрическую
- 3. Гальванические элементыНа практике наиболее распространены сухие гальванические
- 4. Сухой марганцево-цинковый элемент (1) — металлической колпачок (2) —
- 5. АккумуляторыУстройства, в которых поэтапно происходит преобразование электрической
- 6. Топливные элементыВ них энергия реакции горения топлива
- 7. Электролиз Электролиз – это совокупность окислительно-восстановительных процессов,
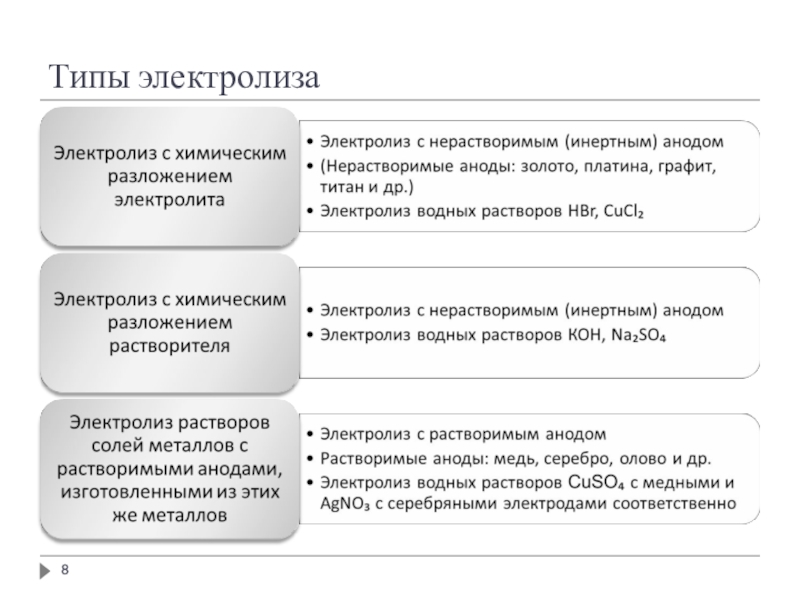
- 8. Типы электролиза
- 9. Практическое применение электролизаЭлектролизом раствора NaCl получают гидроксид
- 10. Спасибо за внимание☺
Химические источники токаУстройства, превращающие химическую энергию окислительно-восстановительных реакций в электрическую
Слайд 2Химические источники тока
Устройства, превращающие химическую энергию окислительно-восстановительных реакций в электрическую
Слайд 3Гальванические элементы
На практике наиболее распространены сухие гальванические элементы
Применяют как источники питания
в системах сигнализации, часах, калькуляторах, аудиосистемах, игрушках, радио, пультах дистанционного управления и т.д.
Принцип работы и устройство сходны, различия в химической природе электродов
Принцип работы и устройство сходны, различия в химической природе электродов
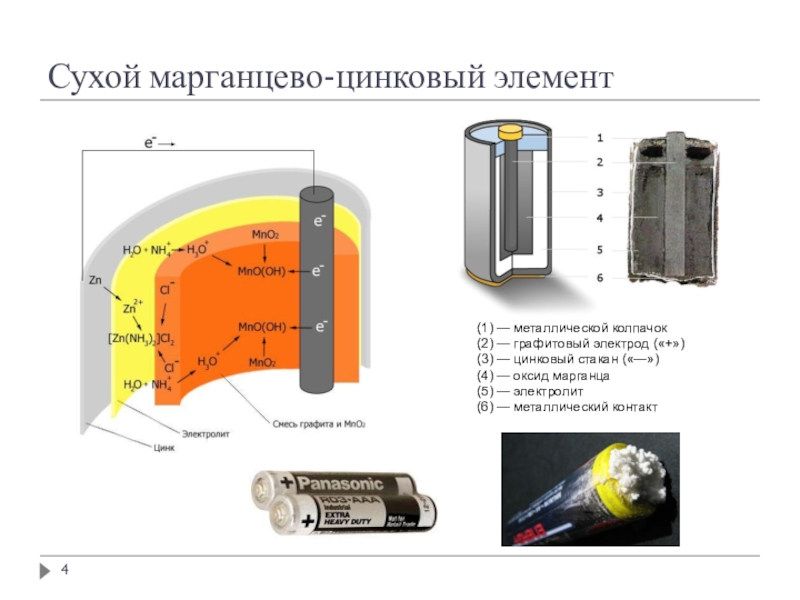
Слайд 4Сухой марганцево-цинковый элемент
(1) — металлической колпачок
(2) — графитовый электрод («+»)
(3) — цинковый стакан («—»)
(4) —
оксид марганца
(5) — электролит
(6) — металлический контакт
Слайд 5Аккумуляторы
Устройства, в которых поэтапно происходит преобразование электрической энергии в химическую, а
химической - в электрическую
Агрегат многоразового действия, сочетающий в себе гальванический элемент и электролизёр
Процесс накопления химической энергии под действием внешнего постоянного тока называют зарядкой аккумулятора (работает как электролизёр)
Процесс превращения химической энергии в электрическую называют разрядкой аккумулятора (работает как гальванический элемент)
Агрегат многоразового действия, сочетающий в себе гальванический элемент и электролизёр
Процесс накопления химической энергии под действием внешнего постоянного тока называют зарядкой аккумулятора (работает как электролизёр)
Процесс превращения химической энергии в электрическую называют разрядкой аккумулятора (работает как гальванический элемент)
Слайд 6Топливные элементы
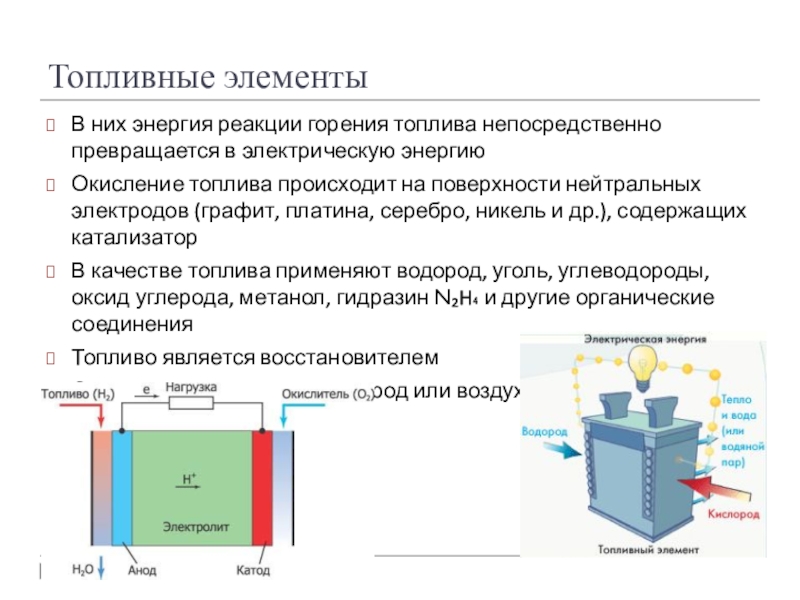
В них энергия реакции горения топлива непосредственно превращается в электрическую
энергию
Окисление топлива происходит на поверхности нейтральных электродов (графит, платина, серебро, никель и др.), содержащих катализатор
В качестве топлива применяют водород, уголь, углеводороды, оксид углерода, метанол, гидразин N₂H₄ и другие органические соединения
Топливо является восстановителем
Окислителем является кислород или воздух
Окисление топлива происходит на поверхности нейтральных электродов (графит, платина, серебро, никель и др.), содержащих катализатор
В качестве топлива применяют водород, уголь, углеводороды, оксид углерода, метанол, гидразин N₂H₄ и другие органические соединения
Топливо является восстановителем
Окислителем является кислород или воздух
Слайд 7Электролиз
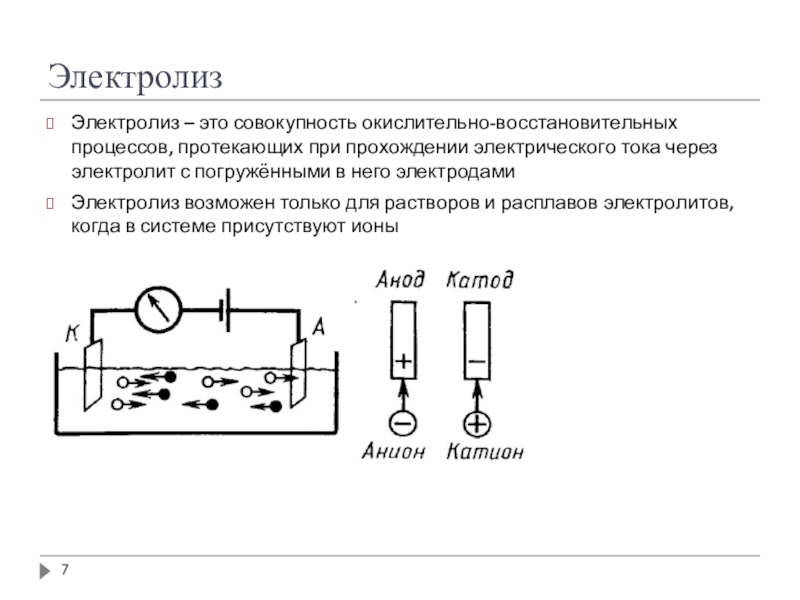
Электролиз – это совокупность окислительно-восстановительных процессов, протекающих при прохождении электрического
тока через электролит с погружёнными в него электродами
Электролиз возможен только для растворов и расплавов электролитов, когда в системе присутствуют ионы
Электролиз возможен только для растворов и расплавов электролитов, когда в системе присутствуют ионы
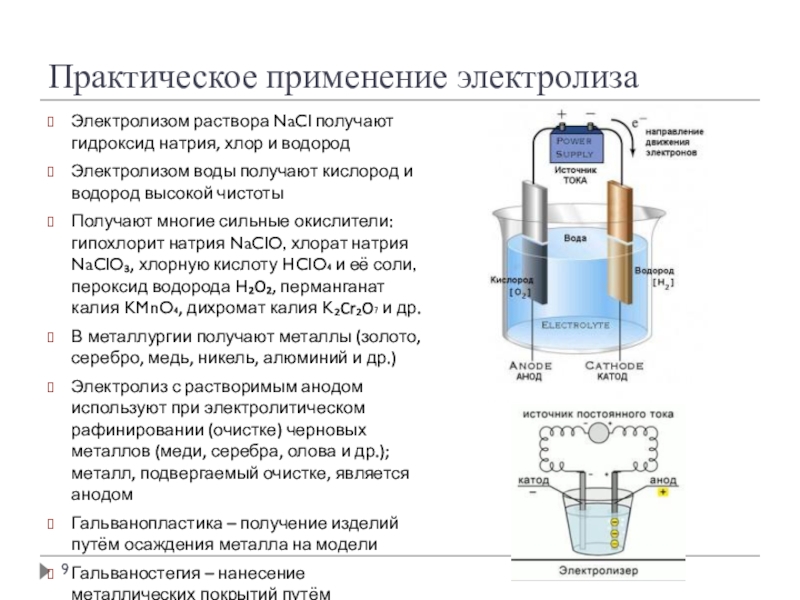
Слайд 9Практическое применение электролиза
Электролизом раствора NaCl получают гидроксид натрия, хлор и водород
Электролизом
воды получают кислород и водород высокой чистоты
Получают многие сильные окислители: гипохлорит натрия NaClO, хлорат натрия NaClO₃, хлорную кислоту HClO₄ и её соли, пероксид водорода H₂O₂, перманганат калия KMnO₄, дихромат калия K₂Cr₂O₇ и др.
В металлургии получают металлы (золото, серебро, медь, никель, алюминий и др.)
Электролиз с растворимым анодом используют при электролитическом рафинировании (очистке) черновых металлов (меди, серебра, олова и др.); металл, подвергаемый очистке, является анодом
Гальванопластика – получение изделий путём осаждения металла на модели
Гальваностегия – нанесение металлических покрытий путём электролиза
Получают многие сильные окислители: гипохлорит натрия NaClO, хлорат натрия NaClO₃, хлорную кислоту HClO₄ и её соли, пероксид водорода H₂O₂, перманганат калия KMnO₄, дихромат калия K₂Cr₂O₇ и др.
В металлургии получают металлы (золото, серебро, медь, никель, алюминий и др.)
Электролиз с растворимым анодом используют при электролитическом рафинировании (очистке) черновых металлов (меди, серебра, олова и др.); металл, подвергаемый очистке, является анодом
Гальванопластика – получение изделий путём осаждения металла на модели
Гальваностегия – нанесение металлических покрытий путём электролиза