- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: ХИМИЧЕСКИЕ ФОРМУЛЫ. ОТНОСИТЕЛЬНАЯ АТОМНАЯ И МОЛЕКУЛЯРНАЯ МАССЫ (8 класс)
Содержание
- 1. Презентация по химии на тему: ХИМИЧЕСКИЕ ФОРМУЛЫ. ОТНОСИТЕЛЬНАЯ АТОМНАЯ И МОЛЕКУЛЯРНАЯ МАССЫ (8 класс)
- 2. ХИМИЧЕСКИЕ ФОРМУЛЫ. ОТНОСИТЕЛЬНАЯ АТОМНАЯ И МОЛЕКУЛЯРНАЯ МАССЫ.
- 3. Знаки химических элементов.- название- произношениеAlBaCaNaKClSFPbCuHgHOCBBrZnAgAuNSiFeIПроверка знаний:
- 4. Химический диктант: КислородВодородКальцийСераАзотАлюминийЦинкЖелезоСереброНатрийКалийФосфорМагнийРтутьБарий
- 5. Атомно - молекулярное учение Все вещества
- 6. Химическая формулаХимическая формула - это условная запись состава
- 7. Химическая формулаИНДЕКС обозначает число атомов в молекуле.
- 8. Химическая формулаНапример: H2O-формула воды, где
- 9. Химическая формула воды
- 10. КИСЛОРОД (O2) Молекула кислорода (O2) состоит из двух
- 11. АЗОТ (N2) Молекула азота (N2) состоит из двух
- 12. СЕРА (S8) Молекула серы (S8) состоит из восьми
- 13. ХЛОР (Cl2) Молекула хлора (Сl2) состоит из двух атомов
- 14. Химические формулыЧтение химических формул:P2O5Fe2O3BaCO3Na2SO4Ca(OH)2(NH4)3PO4KHCO3PbSiO3AlCl3CH3COOHAgNO3ZnMnO4C8H18
- 15. Что означают записи? 3Fe
- 16. О какой форме существования химического элемента кислорода
- 17. Относительная атомная массаОтносительной атомной массой химического элемента
- 18. Атомная единица массыСовременные методы исследования позволяют определить
- 19. Относительная атомная массаМеждународная единица атомных масс равна 1/12 массы изотопа 12C - основного изотопа природного углерода.
- 20. Относительная атомная массаОтносительные атомные массы указаны в
- 21. Hg (ma=201 a.e.m.)Eu (ma=152 a.e.m.)N (ma=14 a.e.m.)K
- 22. Относительная молекулярная массаОтносительной молекулярной массой вещества называется
- 23. Относительная молекулярная массаОтносительная молекулярная масса (Mr) - безразмерная величина,
- 24. Относительная молекулярная массаВы знаете, что молекулы состоят
- 25. Относительная молекулярная массаОтносительная молекулярная масса (Mr) - безразмерная величина, показывающая,
- 26. Гимнастика для глаз
- 27. РЕШЕНИЕ ЗАДАЧ Определение относительной молекулярной массы.
- 28. ЗаданияОпределить относительные молекулярные массы следующих веществ: 1)
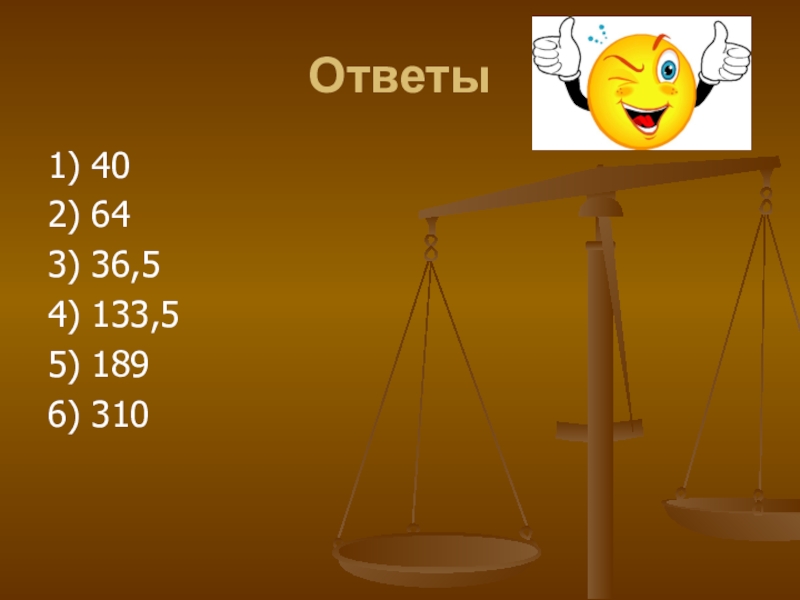
- 29. Ответы1) 402) 643) 36,54) 133,55) 1896) 310
- 30. Домашнее задание:Выучить § 5, №1-3 (письменно)
- 31. СПАСИБО ВСЕМ ЗА ВНИМАНИЕ!
ХИМИЧЕСКИЕ ФОРМУЛЫ. ОТНОСИТЕЛЬНАЯ АТОМНАЯ И МОЛЕКУЛЯРНАЯ МАССЫ.
Слайд 3Знаки химических элементов.
- название
- произношение
Al
Ba
Ca
Na
K
Cl
S
F
Pb
Cu
Hg
H
O
C
B
Br
Zn
Ag
Au
N
Si
Fe
I
Проверка знаний:
Слайд 4Химический диктант:
Кислород
Водород
Кальций
Сера
Азот
Алюминий
Цинк
Железо
Серебро
Натрий
Калий
Фосфор
Магний
Ртуть
Барий
Слайд 5Атомно - молекулярное учение
Все вещества состоят из молекул.
Молекула -
наименьшая частица вещества, обладающая его химическими свойствами.
Молекулы состоят из атомов.
Атом - наименьшая частица химического элемента, сохраняющая все его химические свойства.
Различным элементам соответствуют различные атомы.
Молекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания.
Молекулы состоят из атомов.
Атом - наименьшая частица химического элемента, сохраняющая все его химические свойства.
Различным элементам соответствуют различные атомы.
Молекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания.
Слайд 6Химическая формула
Химическая формула - это условная запись состава вещества с помощью химических
знаков и индексов (индекс - цифра, стоящая справа внизу от символа).
(предложены в 1814 г. Й. Берцелиусом)
(предложены в 1814 г. Й. Берцелиусом)
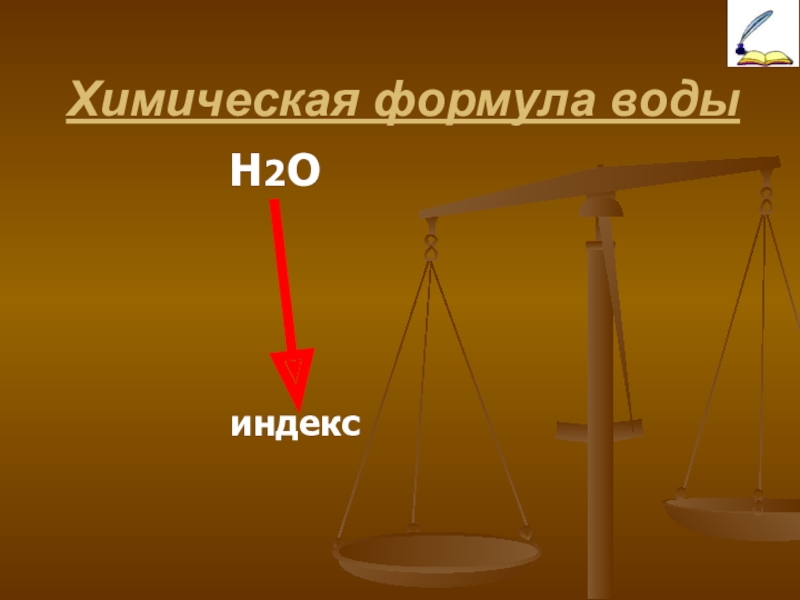
Слайд 7Химическая формула
ИНДЕКС обозначает число атомов в молекуле.
Химическая формула показывает на
то, атомы каких элементов и в каком отношении соединены между собой в молекуле.
Слайд 8Химическая формула
Например:
H2O-формула воды,
где Н и О-химические
знаки элементов,
2-индекс, который показывает число атомов данного элемента, входящих в состав молекулы воды. При названии веществ с переменной валентностью обязательно указывается его валентность, которая ставится в скобки.
Например, Р2О5- оксид фосфора (V).
2-индекс, который показывает число атомов данного элемента, входящих в состав молекулы воды. При названии веществ с переменной валентностью обязательно указывается его валентность, которая ставится в скобки.
Например, Р2О5- оксид фосфора (V).
Слайд 10КИСЛОРОД (O2)
Молекула
кислорода (O2) состоит из двух атомов
кислорода (O).
В свободном
виде кислород - газ без цвета, запаха и вкуса.
Слайд 11АЗОТ (N2)
Молекула азота (N2) состоит из двух атомов азота (N).
В свободном
виде -газ без цвета, запаха и вкуса, плохо растворим в воде.
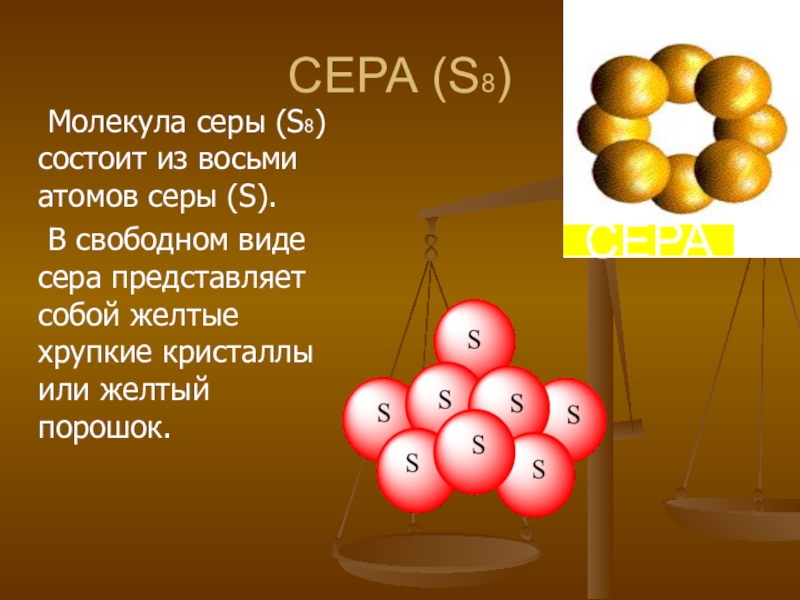
Слайд 12СЕРА (S8)
Молекула серы (S8) состоит из восьми атомов серы (S).
В свободном
виде сера представляет собой желтые хрупкие кристаллы или желтый порошок.
СЕРА
Слайд 13ХЛОР (Cl2)
Молекула хлора (Сl2)
состоит из двух атомов хлора (Cl).
В свободном виде
-желто-зеленый тяжелый газ с резким удушливым запахом.
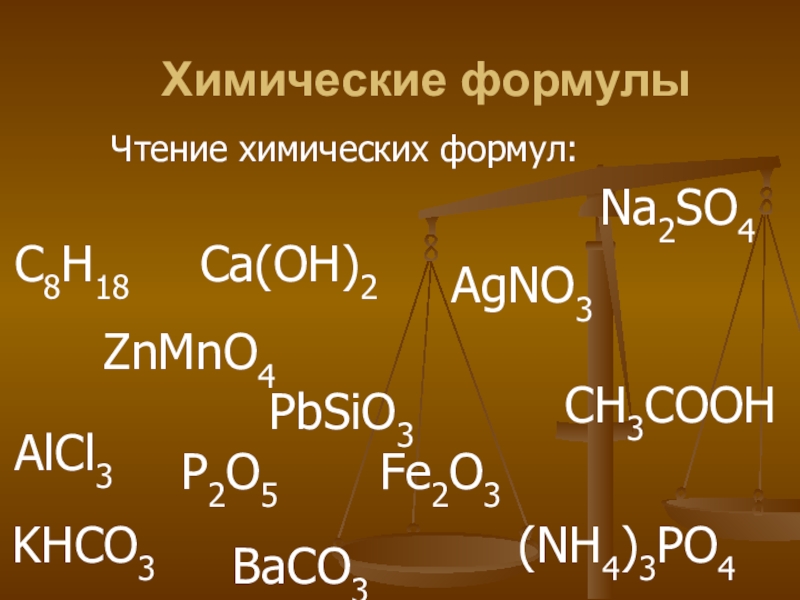
Слайд 14Химические формулы
Чтение химических формул:
P2O5
Fe2O3
BaCO3
Na2SO4
Ca(OH)2
(NH4)3PO4
KHCO3
PbSiO3
AlCl3
CH3COOH
AgNO3
ZnMnO4
C8H18
Слайд 16О какой форме существования химического элемента кислорода говорит каждая из записей?
3Hg O2
4S 5K
3CO2 3H2O
6O2 4P
4S 5K
3CO2 3H2O
6O2 4P
Слайд 17Относительная атомная масса
Относительной атомной массой химического элемента называется величина, показывающая во
сколько раз масса данного атома больше 1/12 массы атома углерода.
Она обозначается буквой Аr.
Она обозначается буквой Аr.
Слайд 18Атомная единица массы
Современные методы исследования позволяют определить чрезвычайно малые массы атомов
с большой точностью. Так, например, масса атома углерода равна 1,993·10-26 кг.
Это очень маленькая величина. Поэтому в химии используются не абсолютные значения атомных масс, а относительные.
За единицу атомной массы принята атомная единица массы, равная 1/12 части массы атома углерода.
Это очень маленькая величина. Поэтому в химии используются не абсолютные значения атомных масс, а относительные.
За единицу атомной массы принята атомная единица массы, равная 1/12 части массы атома углерода.
Слайд 19Относительная атомная масса
Международная единица атомных масс равна 1/12 массы изотопа 12C - основного изотопа природного углерода.
Слайд 20Относительная атомная масса
Относительные атомные массы указаны в периодической таблице.
Например: Аr(Н)=1, Аr(Р)=31.
Атомные массы округляем до целых величин,
исключая атом хлора- Аr(Cl)=35,5.
Атомные массы округляем до целых величин,
исключая атом хлора- Аr(Cl)=35,5.
Слайд 21Hg (ma=201 a.e.m.)
Eu (ma=152 a.e.m.)
N (ma=14 a.e.m.)
K (ma=39 a.e.m.)
Zn (ma=65 a.e.m.)
In
(ma=115 a.e.m.)
Y (ma=89 a.e.m.)
Sn (ma=119 a.e.m.)
Na (ma=23 a.e.m.)
Mg (ma=24 a.e.m.)
Al (ma=27 a.e.m.)
Eu (ma=152 a.e.m.)
B (ma=11 a.e.m.)
Слайд 22Относительная молекулярная масса
Относительной молекулярной массой вещества называется величина, показывающая во сколько
раз масса молекулы больше 1/12 массы атома углерода.
Она обозначается Мr
Она обозначается Мr
Слайд 23Относительная молекулярная масса
Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз
масса молекулы данного вещества больше1/12 массы атома углерода 12C.
Слайд 24Относительная молекулярная масса
Вы знаете, что молекулы состоят из атомов, поэтому относительная
молекулярная масса складывается из суммы атомных масс атомов, составляющих молекулу, с учётом числа атомов.
Например:
Мr(H2SO4)=1·2+32+16·4=98
Например:
Мr(H2SO4)=1·2+32+16·4=98
Слайд 25Относительная молекулярная масса
Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз масса
молекулы данного вещества больше1/12 массы атома углерода C
12
Слайд 27РЕШЕНИЕ ЗАДАЧ
Определение относительной молекулярной массы.
Какова относительная молекулярная
масса Mr (СаО) ?
Решение: Mr = Ar(Cа)+Ar(O)+=40+16=56
Ответ:56
Решение: Mr = Ar(Cа)+Ar(O)+=40+16=56
Ответ:56
Слайд 28Задания
Определить относительные молекулярные массы следующих веществ:
1) MgO
2) SO2
3) HCl
4) AlCl3
5) Zn(NO3)2
6) Ca3(PO4)2