- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Физические и химические свойства металлов
Содержание
- 1. Презентация по химии на тему Физические и химические свойства металлов
- 2. Металлы – химические элементы , образующие в
- 3. Роль металлов в жизни человека и общества.В
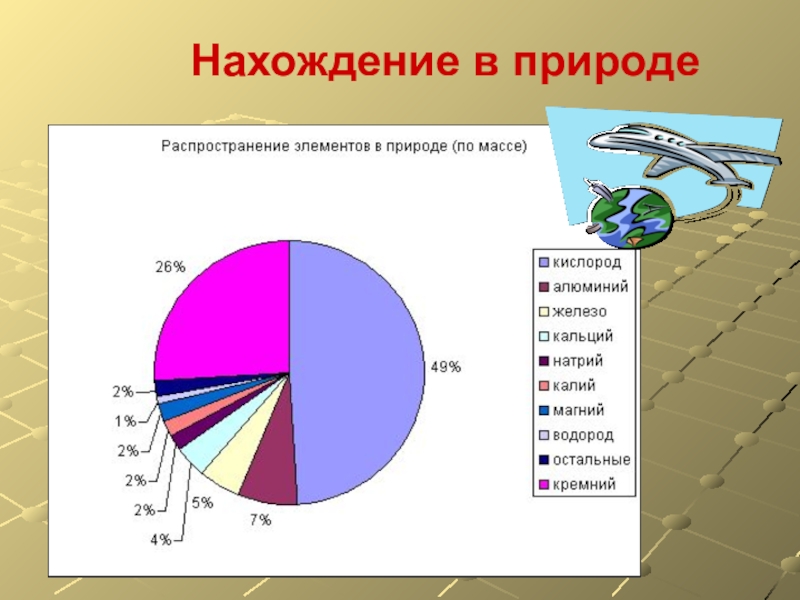
- 4. Нахождение в природе
- 5. Физические свойства металловОчень важным свойством металлов является
- 6. Все металлы имеют характерный металлический блеск.
- 7. Частицы металлов, находящихся в твердом и жидком
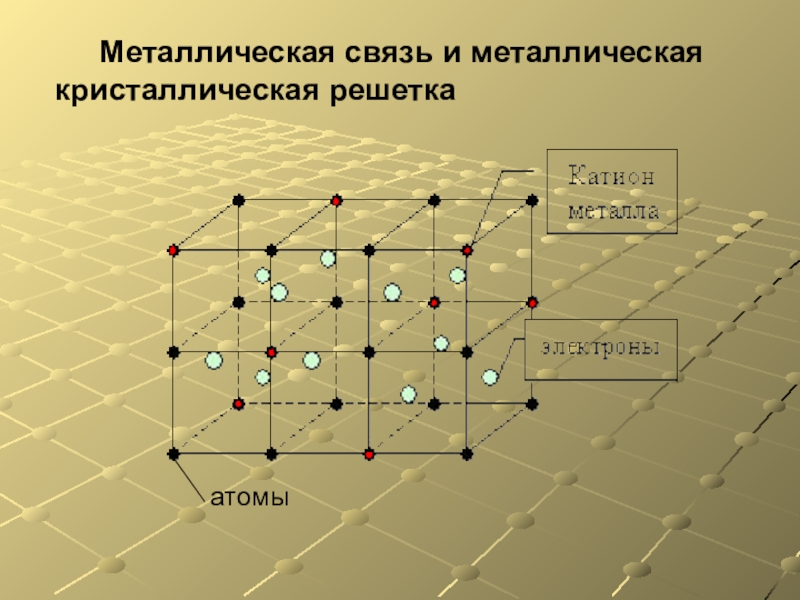
- 8. Металлическая связь и металлическая кристаллическая решеткаатомы
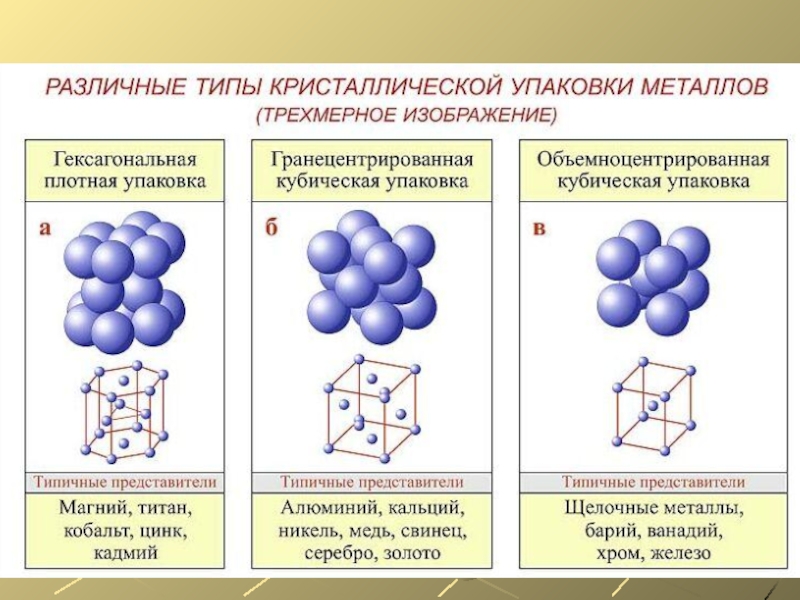
- 9. Слайд 9
- 10. Металлычерныецветные
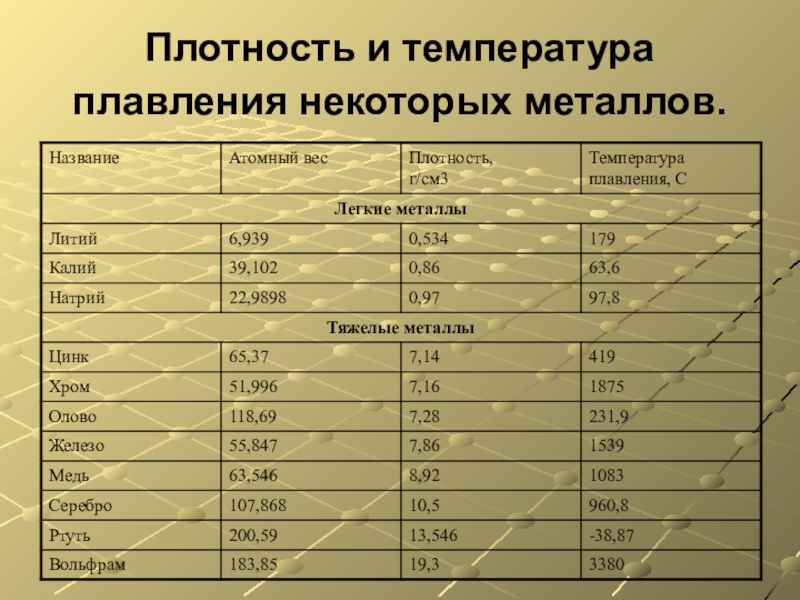
- 11. Плотность и температура плавления некоторых металлов.
- 12. Металлылегкиетяжелые( плотность не более 5 г/см3 )( плотность больше 5 г/см3 )
- 13. Металлымягкиетвердые
- 14. Металлылегкоплавкиетугоплавкие( t пл < 1539 0С )( t пл > 1539 0С )
- 15. Химические свойства металловОсновным химическим свойством металлов является
- 16. 1. Взаимодействие с неметаллами.Закончите уравнения химических реакций.
- 17. Взаимодействие железа с серой Разберите данную реакцию с т. з. окисления-восстановления.
- 18. А).С активными металлами.Ме + Н2О
- 19. 3. Взаимодействие с кислотами. Металлы, стоящие в
- 20. 4. Взаимодействие с солями.Взаимодействие железа с медным
- 21. Выводы:1. Химические свойства металлов определяются строением их
- 22. Применение металловСтанко-строениемедицинаСельское хозяйство получение сплавовВ бытуМеталлургическая промыш-ленность
- 23. Получение металловПирометаллургический способ -восстановление углеродом,
- 24. СПАСИБО ЗА ВНИМАНИЕ
Слайд 2Металлы – химические элементы , образующие в свободном состоянии простые вещества
М.В. Ломоносов - металлы «светлое тело, которое ковать можно»
Что такое металлы
Ba
Cr
K
Li
Слайд 3Роль металлов в жизни человека и общества.
В древности человеку были известны
Сначала человек познакомился с металлами,которые встречаются в самородном виде - это золото,серебро и медь.
Остальные металлы появились после того,как человек научился добывать их из руд с помощью огня.
Каменный век → Медный век → Бронзовый век → Железный век.
Слайд 5Физические свойства металлов
Очень важным свойством металлов является их сравнительно легкая механическая
Слайд 7Частицы металлов, находящихся в твердом и жидком состоянии, связаны особым типом
Слайд 15Химические свойства металлов
Основным химическим свойством металлов является способность их атомов легко
Слайд 161. Взаимодействие с неметаллами.
Закончите уравнения химических реакций. Дайте названия образующимся веществам:
Mg
Al + O2
Cu + S
K + CL2
Ca + P
Взаимодействие алюминия с бромом
Разберите данную реакцию с т. з. окисления-восстановления
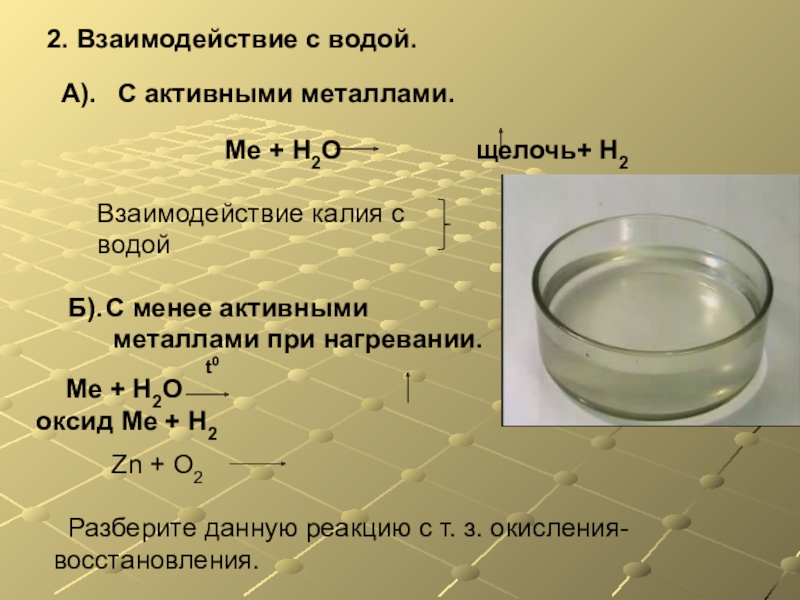
Слайд 18А).
С активными металлами.
Ме + Н2О
Б).
С менее активными
металлами при нагревании.
Ме + Н2О оксид Ме + Н2
t0
2. Взаимодействие с водой.
Взаимодействие калия с водой
Zn + O2
Разберите данную реакцию с т. з. окисления-восстановления.
Слайд 193. Взаимодействие с кислотами.
Металлы, стоящие в ряду активности до водорода,
Взаимодействие железа с разбавленной серной кислотой
Запишите уравнение реакции и разберите её с т. з. окисления-восстановления.
Слайд 204. Взаимодействие с солями.
Взаимодействие железа с медным купоросом.
Взаимодействие меди с нитратом
Запишите уравнения реакций и разберите одну из них с т. з. окисления-восстановления.
Слайд 21Выводы:
1. Химические свойства металлов определяются строением их атомов и строением простого
2. При химических реакциях атомы металлов являются восстановителями, окисляясь при этом.
3. Активность металлов зависит:
А) от числа валентных электронов – чем их меньше, тем металл активнее;
Б) от удаленности валентных электронов от ядра – чем дальше, тем металл активнее.
Слайд 22 Применение металлов
Станко-
строение
медицина
Сельское хозяйство
получение сплавов
В быту
Металлургическая промыш-ленность
Слайд 23 Получение металлов
Пирометаллургический способ -восстановление углеродом, оксидом углерода (II), водородом
Алюминотермический способ – восстановление металлов с помощью алюминия.
Гидрометаллургический способ – получение из руды более активным металлом или из растворов
Электролиз – с помощью электрического тока из расплавов или растворов