- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Азотная кислота
Содержание
- 1. Презентация по химии на тему: Азотная кислота
- 2. Азотная кислотаАзо́тная кислота́ (HNO3), — сильная одноосновная
- 3. СвойстваВысококонцентрированная HNO3 имеет обычно бурую окраску
- 4. СвойстваБольшинство металлов реагируют с азотной кислотой с
- 5. НитратыHNO3 — сильная кислота. Её соли —
- 6. Производство азотной кислотыСовременный способ её производства основан
- 7. Применениев производстве минеральных удобрений;в военной промышленности;в фотографии
- 8. Физические свойстваЧистая азотная кислота представляет собой бесцветную
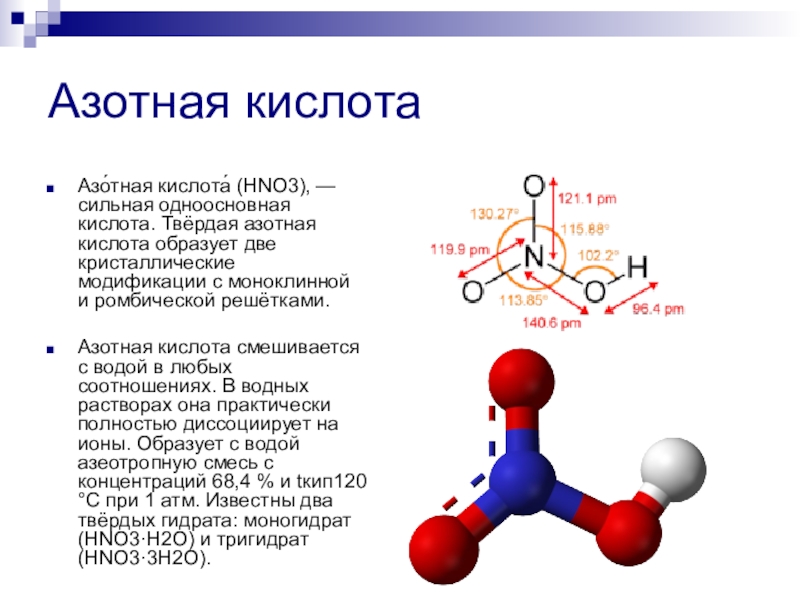
Азотная кислотаАзо́тная кислота́ (HNO3), — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической решётками.Азотная кислота смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы.
Слайд 2Азотная кислота
Азо́тная кислота́ (HNO3), — сильная одноосновная кислота. Твёрдая азотная кислота
образует две кристаллические модификации с моноклинной и ромбической решётками.
Азотная кислота смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы. Образует с водой азеотропную смесь с концентраций 68,4 % и tкип120 °C при 1 атм. Известны два твёрдых гидрата: моногидрат (HNO3·H2O) и тригидрат (HNO3·3H2O).
Азотная кислота смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы. Образует с водой азеотропную смесь с концентраций 68,4 % и tкип120 °C при 1 атм. Известны два твёрдых гидрата: моногидрат (HNO3·H2O) и тригидрат (HNO3·3H2O).
Слайд 3 Свойства
Высококонцентрированная HNO3 имеет обычно бурую окраску вследствие происходящего на свету
процесса разложения:
При нагревании азотная кислота распадается по той же реакции. Азотную кислоту можно перегонять (без разложения) только при пониженном давлении (указанная температура кипения при атмосферном давлении найдена экстраполяцией).
Азотная кислота является сильным окислителем, концентрированная азотная кислота окисляет серу до серной, а фосфор — до фосфорной кислоты, некоторые органические соединения (например амины и гидразин, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Золото, некоторые металлы платиновой группы и тантал инертны к азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется её концентрацией. Так, концентрированная азотная кислота реагирует с медью с образованием диоксида азота, а разбавленная — оксида азота (II):
При нагревании азотная кислота распадается по той же реакции. Азотную кислоту можно перегонять (без разложения) только при пониженном давлении (указанная температура кипения при атмосферном давлении найдена экстраполяцией).
Азотная кислота является сильным окислителем, концентрированная азотная кислота окисляет серу до серной, а фосфор — до фосфорной кислоты, некоторые органические соединения (например амины и гидразин, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Золото, некоторые металлы платиновой группы и тантал инертны к азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется её концентрацией. Так, концентрированная азотная кислота реагирует с медью с образованием диоксида азота, а разбавленная — оксида азота (II):
Свойства
Слайд 4Свойства
Большинство металлов реагируют с азотной кислотой с выделением оксидов азота в
различных степенях окисления или их смесей, разбавленная азотная кислота при реакции с активными металлами может реагировать с выделением водорода и восстановлением нитрат-иона до аммиака.
Некоторые металлы (железо, хром, алюминий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
Смесь азотной и серной кислот носит название «меланж».
Азотная кислота широко используется для получения нитросоединений.
Смесь трех объёмов соляной кислотой и одного объёма азотной называется «царской водкой». Царская водка растворяет большинство металлов, в том числе и золото. Её сильные окислительные способности обусловлены образующимся атомарным хлором и хлоридом нитрозила:
Некоторые металлы (железо, хром, алюминий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
Смесь азотной и серной кислот носит название «меланж».
Азотная кислота широко используется для получения нитросоединений.
Смесь трех объёмов соляной кислотой и одного объёма азотной называется «царской водкой». Царская водка растворяет большинство металлов, в том числе и золото. Её сильные окислительные способности обусловлены образующимся атомарным хлором и хлоридом нитрозила:
Слайд 5Нитраты
HNO3 — сильная кислота. Её соли — нитраты — получают действием
HNO3 на металлы, оксиды, гидроксиды или карбонаты. Все нитраты хорошо растворимы в воде. Их растворы обладают незначительными окислительными свойствами.
При нагревании нитраты разлагаются, нитраты щелочных металлов превращаются в нитриты
Соли других металлов образуют оксиды:
При разложении нитратов металлов, оксиды которых нестабильны, выделяется свободный металл:
Цинк и алюминий в щелочном растворе восстанавливают нитраты до NH3:
Соли азотной кислоты — нитраты — широко используются как удобрения. При этом практически все нитраты хорошо растворимы в воде, поэтому в виде минералов их в природе чрезвычайно мало; исключение составляют чилийская (натриевая) селитра и индийская селитра (нитрат калия). Большинство нитратов получают искусственно.
С азотной кислотой не реагируют стекло, фторопласт-4.
При нагревании нитраты разлагаются, нитраты щелочных металлов превращаются в нитриты
Соли других металлов образуют оксиды:
При разложении нитратов металлов, оксиды которых нестабильны, выделяется свободный металл:
Цинк и алюминий в щелочном растворе восстанавливают нитраты до NH3:
Соли азотной кислоты — нитраты — широко используются как удобрения. При этом практически все нитраты хорошо растворимы в воде, поэтому в виде минералов их в природе чрезвычайно мало; исключение составляют чилийская (натриевая) селитра и индийская селитра (нитрат калия). Большинство нитратов получают искусственно.
С азотной кислотой не реагируют стекло, фторопласт-4.
Слайд 6Производство азотной кислоты
Современный способ её производства основан на каталитическом окислении синтетического
аммиака на платино-родиевых катализаторах (метод Габера) до смеси оксидов азота (нитрозных газов), с дальнейшим поглощением их водой
4NH3 + 5O2 (Pt) → 4NO + 6H2O
2NO + O2 → 2NO2
4NO2 + O2 + 2H2O → 4HNO3.
Концентрация полученной таким методом азотной кислоты колеблется в зависимости от технологического оформления процесса от 45 до 58 %. Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
4KNO3 + 2(FeSO4 · 7H2O) (t°) → Fe2O3 + 2K2SO4 + 2HNO3↑ + NO2↑ + 13H2O
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:
KNO3 + H2SO4(конц.) (t°) → KHSO4 + HNO3↑
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
4NH3 + 5O2 (Pt) → 4NO + 6H2O
2NO + O2 → 2NO2
4NO2 + O2 + 2H2O → 4HNO3.
Концентрация полученной таким методом азотной кислоты колеблется в зависимости от технологического оформления процесса от 45 до 58 %. Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
4KNO3 + 2(FeSO4 · 7H2O) (t°) → Fe2O3 + 2K2SO4 + 2HNO3↑ + NO2↑ + 13H2O
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:
KNO3 + H2SO4(конц.) (t°) → KHSO4 + HNO3↑
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
Слайд 7Применение
в производстве минеральных удобрений;
в военной промышленности;
в фотографии — подкисление некоторых тонирующих
растворов[1];
в станковой графике — для травления печатных форм (офортных досок, цинкографических типографских форм и магниевых клише).
в станковой графике — для травления печатных форм (офортных досок, цинкографических типографских форм и магниевых клише).
Слайд 8Физические свойства
Чистая азотная кислота представляет собой бесцветную жидкость с едким запахом
плотностью 1, 52 г/см3 и кипит при 84°С, а при -41°С затвердевает в бесцветное кристаллическое вещество. Обычно применяемая на практике концентрированная азотная кислота содержит 65 – 70% HNO3 (максимальная плотность 1, 4 г/см3); с водой кислота смешивается в любых соотношениях. Существует также дымящая азотная кислота с концентрацией 97 – 99%.





![Презентация по химии на тему: Азотная кислота Применениев производстве минеральных удобрений;в военной промышленности;в фотографии — подкисление некоторых тонирующих Применениев производстве минеральных удобрений;в военной промышленности;в фотографии — подкисление некоторых тонирующих растворов[1];в станковой графике — для травления](/img/tmb/5/446704/a15cddc8b673ea6e2807a0339393ac72-800x.jpg)






