- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Амины
Содержание
- 1. Презентация по химии на тему Амины
- 2. СтроениеАмины - органические произведения аммиака, в молекуле
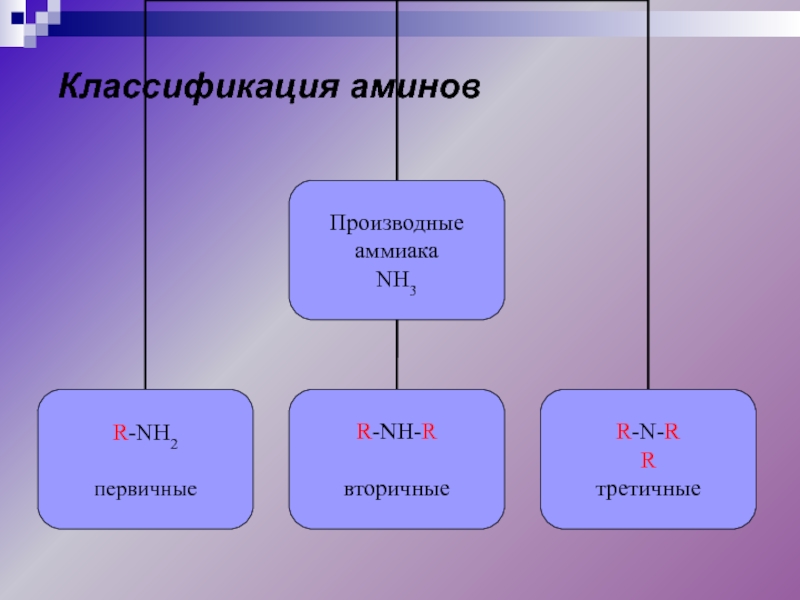
- 3. Классификация аминов
- 4. Типы Аминов.Первичный амин метиламинВторичный амин деэтиламинТретичный амин триэтиламин
- 5. Амины, в которых аминогруппа связана непосредственно с ароматическим кольцом, называются матическими аминами
- 6. ион аммония:
- 7. Изомерия и номенклатура.Изомерия углеродного скелета:бутиламинизобутиламин
- 8. Изомерия положения функциональной группы:пропиламинизопропиламин
- 9. Межклассовая изомерия:Первичный амин прапиламин.Вторичный амин метилэтиламин.
- 10. Получение:В результате этой реакции образуется соль амина
- 11. При взаимодействии полученного первичного амина и галогенопроизводного и последующей обработке щелочью получают вторичный амин (диэтиламин):
- 12. Повторение процедуры приводит к образованию третичного амина:
- 13. Третичный амин может ещё раз вступить в
- 14. Физические свойства.Простейшие амины (метиламин, диметиламин, триметиламин) –
- 15. Химические свойства.Амины как основания.
- 16. Присоединение водорода по донорно-акцепторному механизму.H3N: + H+
- 17. Основное свойство аминов (взаимодействие с кислотами)H3CNH2
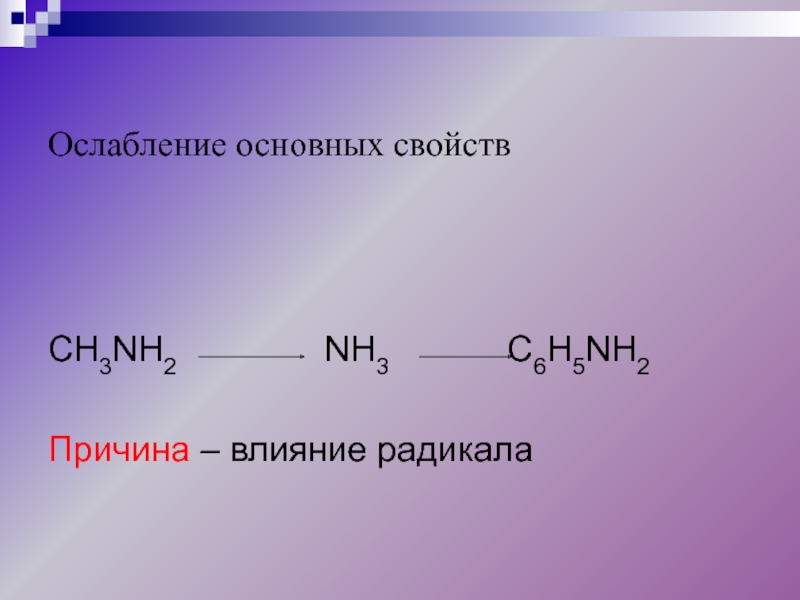
- 18. Ослабление основных свойствCH3NH2
- 19. Амины горят.На воздухе с образованием углекислого газа, воды и азота:
- 20. Амины вступают в реакцию нуклеофильного замещения.Выступая в роли нуклеофилов:
- 21. Амины взаимодействую с производными карбоновых кислот,(сложными эфирами, хлорагидридами, ангидридами).Образуя Амиды – важнейший класс органических соединений:
- 22. Амид – является продуктом замещения гидроксильной группы на остаток амина.
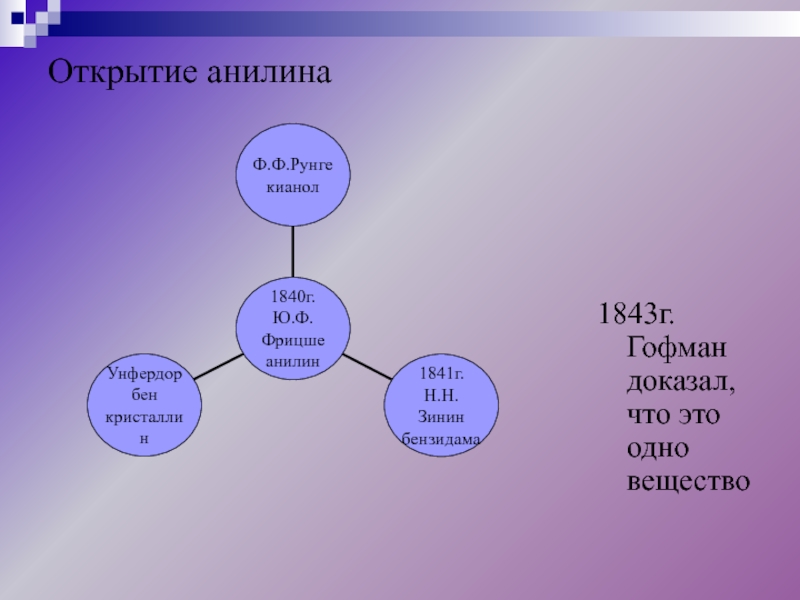
- 23. Открытие анилина1843г. Гофман доказал, что это одно вещество
- 24. Применение аминов.Амины широко применяются для получения лекарств,
- 25. Получение анилинаРеакция ЗининаC6H5NO2 + 6H C6H5NH2 + 2H2O
- 26. Использованные материалы и интернет источникиО. С. Габриелян.
СтроениеАмины - органические произведения аммиака, в молекуле которого один, два или все три атома водорода замещены углеводородным остатком.
Слайд 2Строение
Амины - органические произведения аммиака, в молекуле которого один, два или
все три атома водорода замещены углеводородным остатком.
Слайд 5
Амины, в которых аминогруппа связана непосредственно с ароматическим кольцом, называются матическими
аминами
Слайд 6
ион аммония: ион тетраэтиламмония:
Существуют ионы, которые являются
продуктом формального замещения на углеводородный радикал всех атомов водорода в ионе аммония.
Слайд 9Межклассовая изомерия:
Первичный амин
прапиламин.
Вторичный амин
метилэтиламин.
Третичный амин
триметиламин.
триметиламин.
Слайд 10Получение:
В результате этой реакции образуется соль амина (гидробромид этиламмония), из которой
действием щёлочи можно выделить первичный амин (этиламин):
Получение аминов из галогенопроизводных:
Слайд 11При взаимодействии полученного первичного амина и галогенопроизводного и последующей обработке щелочью
получают вторичный амин (диэтиламин):
Слайд 13Третичный амин может ещё раз вступить в реакцию с бромэтаном. При
этом образуется четвертичная аммонийная соль, образованная бромид-ионом и катионом тетраэтиламмония:
Слайд 14Физические свойства.
Простейшие амины (метиламин, диметиламин, триметиламин) – газообразные вещества. Остальные низшие
амины – жидкости, которые хорошо растворяются в воде. Имеют характерный запах, напоминающий запах аммиака.
Первичные и вторичные амины способны образовывать водородные связи. Это приводит к повышению их температуры.
Первичные и вторичные амины способны образовывать водородные связи. Это приводит к повышению их температуры.
Анилин – маслянистая жидкость, ограниченно растворимая в воде, кипящая при температуре 184
Слайд 15Химические свойства.
Амины как основания.
Атом азота аминогруппы за счет неподеленной пары электронов может образовывать ковалентную связь по донорно – акцепторному механизму, вступая в роли донора. В связи с этим амины способны присоединять катион водорода.
ИОН АММОНИЯ
ИОН ЭТИЛАММОНИЯ
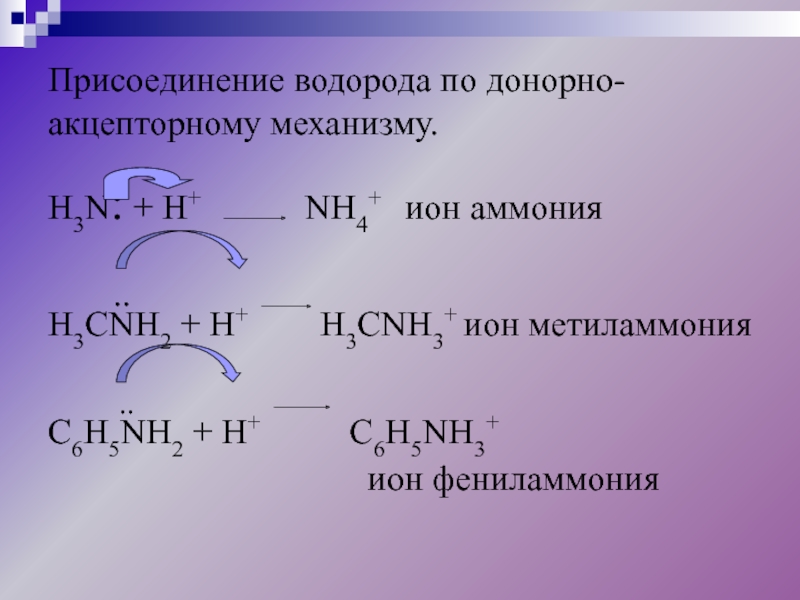
Слайд 16Присоединение водорода по донорно-акцепторному механизму.
H3N: + H+
NH4+ ион аммония
..
H3CNH2 + H+ H3CNH3+ ион метиламмония
..
C6H5NH2 + H+ C6H5NH3+
ион фениламмония
..
H3CNH2 + H+ H3CNH3+ ион метиламмония
..
C6H5NH2 + H+ C6H5NH3+
ион фениламмония
Слайд 17Основное свойство аминов
(взаимодействие с кислотами)
H3CNH2 + HCl
[CH3NH3]+Cl-
хлорид метиламмония
C6H5NH2 + HCl [C6H5NH3]+Cl-
хлорид фениламмония
хлорид метиламмония
C6H5NH2 + HCl [C6H5NH3]+Cl-
хлорид фениламмония
Слайд 21Амины взаимодействую с производными карбоновых кислот,(сложными эфирами, хлорагидридами, ангидридами).
Образуя Амиды –
важнейший класс органических соединений:
Слайд 24Применение аминов.
Амины широко применяются для получения лекарств, полимерных материалов.
Анилин – важнейшее
соединение данного класса, которое используется для производства анилиновых красителей, лекарств (сульфаниламидных препаратов), полимерных материалов (анилиноформальдегидных смол).
Слайд 26Использованные материалы и интернет источники
О. С. Габриелян. Химия.10 класс. Учебник для
общеобразовательных учреждений.
О. С. Габриелян, И.Г. Остроумов. «Химия. 10 класс. Настольная книга учителя»
http://900igr.net
http://ppt4web.ru/khimija
О. С. Габриелян, И.Г. Остроумов. «Химия. 10 класс. Настольная книга учителя»
http://900igr.net
http://ppt4web.ru/khimija














![Презентация по химии на тему Амины Основное свойство аминов (взаимодействие с кислотами)H3CNH2 + HCl [CH3NH3]+Cl- Основное свойство аминов (взаимодействие с кислотами)H3CNH2 + HCl [CH3NH3]+Cl-](/img/tmb/2/142112/74627f54299d744db06ba84cd45b2c8e-800x.jpg)