для себя, а если при труде успеха не будет, неудача – не беда, попробуй ещё.
Д.И. Менделеев
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Алюминий 9 класс
Содержание
- 1. Презентация по химии на тему Алюминий 9 класс
- 2. Император Тиберий
- 3. Тема «Алюминий, его свойства»МБОУСШООЗЗ №2» , учитель химии первой квалификационной категории Иванникова Елена Валентиновна.
- 4. Характеристика алюминия как химического элемента
- 5. Положение в периодической системе
- 6. Алюминий в природе.
- 7. Получение алюминия.1825 год – Г. Эрстед датский
- 8. 1866 год – Ч.Холл (амер.) и
- 9. Цель: 1) исследовать важнейшие физические свойства алюминия
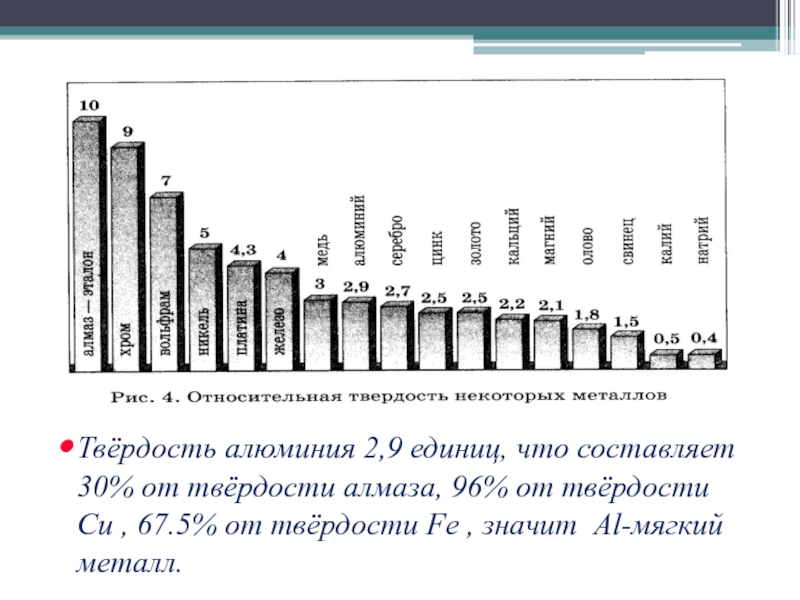
- 10. Твёрдость алюминия 2,9 единиц, что составляет 30%
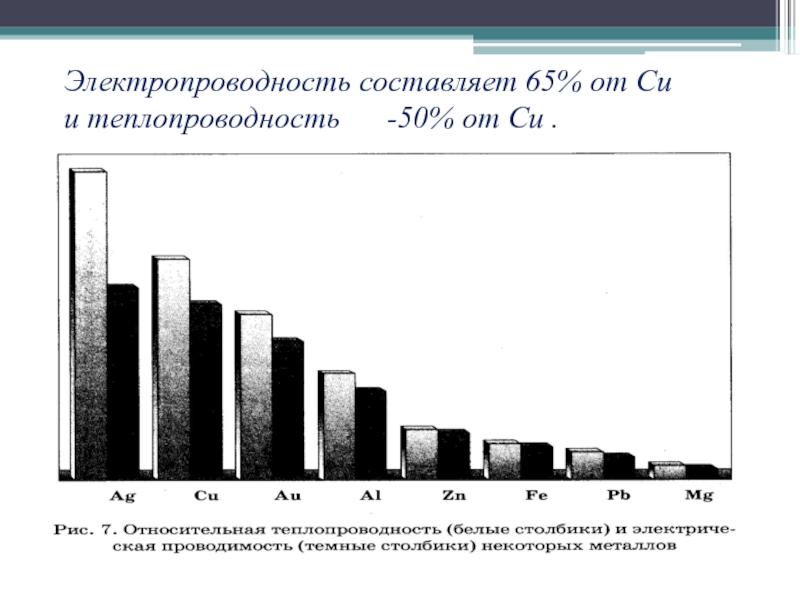
- 11. Электропроводность составляет 65% от Cu и теплопроводность -50% от Cu .
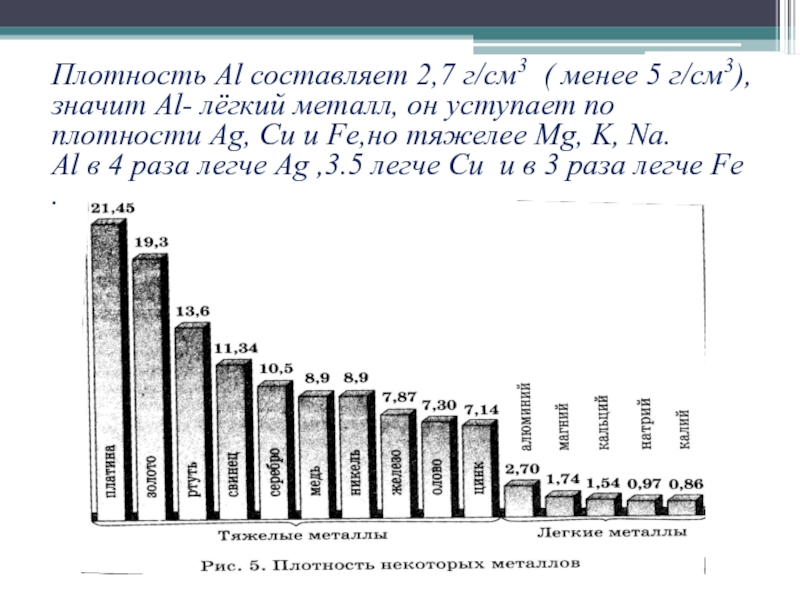
- 12. Плотность Al составляет 2,7 г/см3 ( менее
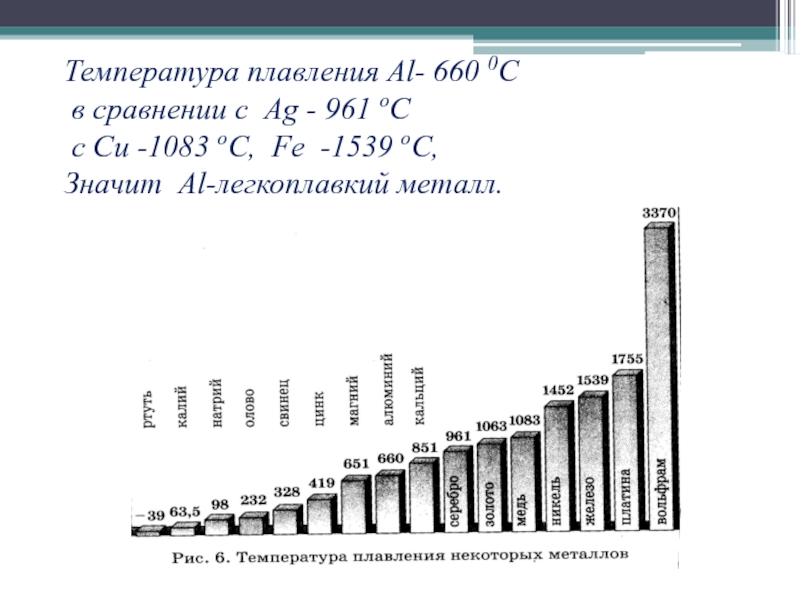
- 13. Температура плавления Al- 660 0С в
- 14. В чём причина таких физических свойств
- 15. Вывод: Характерные физические свойства алюминия находятся
- 16. 2. Химические свойства алюминия. Какова химическая активность
- 17. Составьте уравнения реакций алюминия с
- 18. Составьте уравнения реакций алюминия с кислотой, щёлочью и водой. 1) 2Al +6 HCl=2AlCl3 +3H22) 2Al+2NaOH+2H2O=2NaAlO2+3H23) 2Al+6H2O=2Al(OH)3+3H2
- 19. Вывод:Алюминий –очень активный металл.«Пассивность» алюминия связана с
- 20. Слайд 20
- 21. Применение алюминия
- 22. Слайд 22
- 23. Слайд 23
- 24. Слайд 24
- 25. Домашнее заданиеЗаписи в тетради (выучить).Учебник «Химия –
- 26. Спасибо за внимание!
Император Тиберий
Слайд 3Тема «Алюминий, его свойства»
МБОУСШООЗЗ №2» , учитель химии первой квалификационной категории
Иванникова Елена Валентиновна.
Слайд 5
Положение в периодической системе :
3 период, 3 ряд ,3 группа , главная подгруппа.
№ 13, Ar = 26,981
Строение атома
Z = +13 ) ) )
2 8 3
e- = 13 p+ = 13 n = 14 ZZ)) ))ZZZ. +13 алюминий – переходный металл. ) )
2 8 3
Слайд 7Получение алюминия.
1825 год – Г. Эрстед датский ученый первые получил алюминий
с помощью электролиза
AlCl3+3Na=Al+3NaCl
AlCl3+3Na=Al+3NaCl
Слайд 8 1866 год – Ч.Холл (амер.) и Пол Эру (франц.) разработали промышленный
способ получения алюминия с помощью электролиза, который применяют до настоящего времени.
2Al2O3 = 4Al + 3O2
Слайд 9
Цель: 1) исследовать важнейшие физические свойства алюминия в сравнении со свойствами
других металлов;
2) выявить причины, определяющие эти свойства.
2) выявить причины, определяющие эти свойства.
1.Исследование физических свойств алюминия.
Слайд 10Твёрдость алюминия 2,9 единиц, что составляет 30% от твёрдости алмаза, 96%
от твёрдости Cu , 67.5% от твёрдости Fe , значит Al-мягкий металл.
Слайд 12Плотность Al составляет 2,7 г/см3 ( менее 5 г/см3), значит Al-
лёгкий металл, он уступает по плотности Ag, Cu и Fe,но тяжелее Mg, K, Na.
Al в 4 раза легче Аg ,3.5 легче Cu и в 3 раза легче Fe .
Слайд 13Температура плавления Al- 660 0С в сравнении с Ag - 961
оС
с Cu -1083 оC, Fe -1539 оC,
Значит Al-легкоплавкий металл.
Слайд 14
В чём причина таких физических свойств алюминия?
В строении!
Кристаллическая решётка Al.
Она подобна кубу с плотноупакованными шарами. Это металлическая крисаллическая решётка. В узлах решётки находятся ионы, а в промежутках между ними легкоподвижные электроны. Веществам с металлической кристаллической решёткой присуща металлическая связь.
Слайд 15Вывод:
Характерные физические свойства алюминия находятся в зависимости от его
внутренней структуры. Зная строение, можно прогнозировать свойства металлов.
Слайд 162. Химические свойства алюминия.
Какова химическая активность алюминия ?
Какие свойства проявляет
алюминий , вступая в химические реакции ?
Алюминий- переходный металл.
Алюминий- переходный металл.
Слайд 17
Составьте уравнения реакций алюминия с кислородом, бромом, серой.
1) 4
Al+3O2 =2Al2O3
2) 2Al +3Br2=2AlBr3
3) 2Al+ 3S = Al2S3
2) 2Al +3Br2=2AlBr3
3) 2Al+ 3S = Al2S3
Слайд 18Составьте уравнения реакций алюминия с кислотой, щёлочью и водой.
1) 2Al
+6 HCl=2AlCl3 +3H2
2) 2Al+2NaOH+2H2O=2NaAlO2+3H2
3) 2Al+6H2O=2Al(OH)3+3H2
2) 2Al+2NaOH+2H2O=2NaAlO2+3H2
3) 2Al+6H2O=2Al(OH)3+3H2
Слайд 19Вывод:
Алюминий –очень активный металл.
«Пассивность» алюминия связана с наличием оксидной плёнки.
Алюминий проявляет
переходные свойства.
В реакциях он проявляет восстановительные свойства.
В реакциях он проявляет восстановительные свойства.
Слайд 20 Какие же свойства алюминия позволяют ему найти широкое применение в технике
, быту, промышленности?
Слайд 25Домашнее задание
Записи в тетради (выучить).
Учебник «Химия – 9», стр. 68 -
75 (читать).
Выполнить упр. 6, стр. 75 (письменно).
Выполнить упр. 6, стр. 75 (письменно).