- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Алкены. Этилен (10 класс)
Содержание
- 1. Презентация по химии на тему Алкены. Этилен (10 класс)
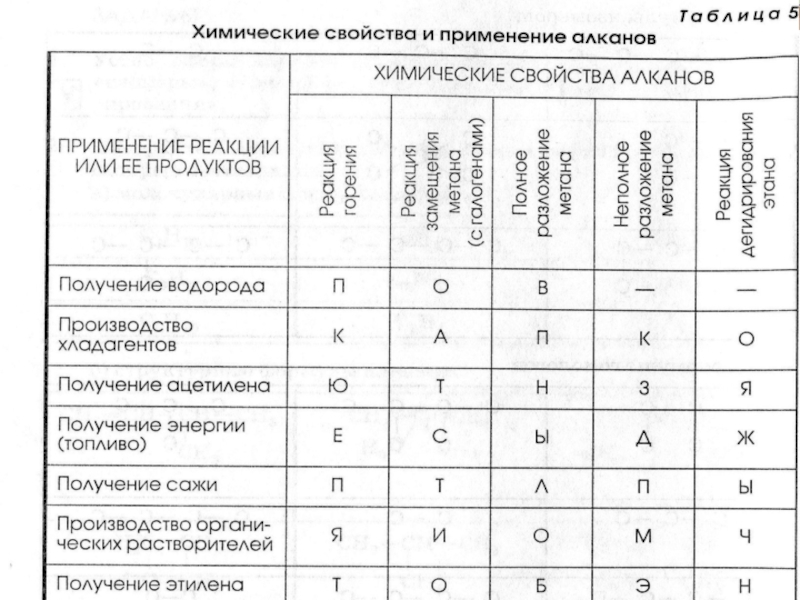
- 2. Из букв, соответствующих правильным ответам, составьте название
- 3. Проверим решение расчётной задачи!задача) Вычислите количество теплоты,
- 4. Слайд 4
- 5. Установите соответствие. Из букв, соответствующих правильным ответам,
- 6. Повторим виды химических реакций алканов!Условия протекания, механизм,
- 7. Слайд 7
- 8. Сегодня на уроке вы…Познакомитесь со способами получения
- 9. Общая схема получения алкенов:Алкан - Н2 алкенПроцесс: дегидрирование
- 10. Гомологический ряд этиленаС2Н4 – этилен, СН2
- 11. ЭтиленБесцветный газ без запаха;В воде плохо растворим;Способен
- 12. Способы получения этиленаВ лаборатории:
- 13. Номенклатура алкеновПример :Составить формулу 2,4-диметилпентен-2Назовите формулы алкенов:
- 14. Изомерия алкеновИзомерия углеродного скелета.Изомерия положения кратной связи;Межклассовая изомерия.Виды изомерии алкенов
- 15. Химические свойства этилена.
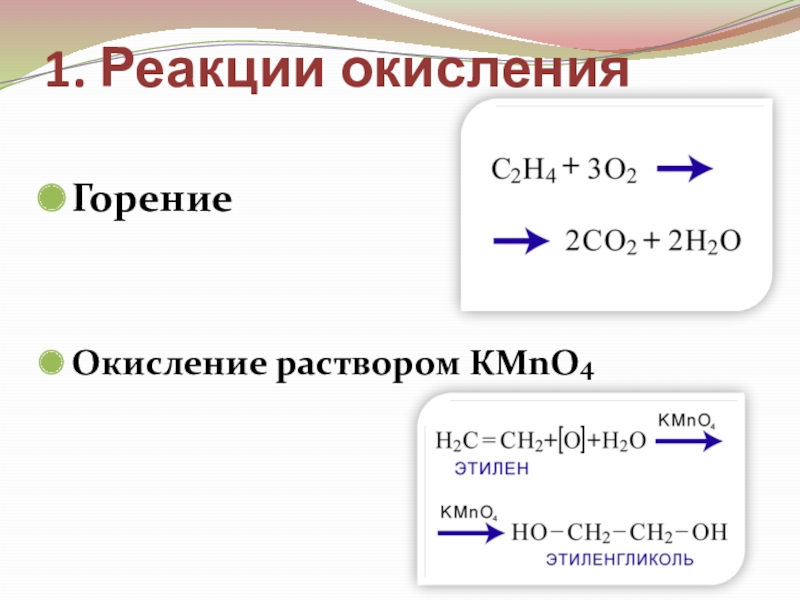
- 16. 1. Реакции окисленияГорениеОкисление раствором КMnO4
- 17. 2. Реакции присоединенияРеакция гидрирования (+ Н2);Гидратация;Галогенирование;Гидрогалогенирование
- 18. При присоединении полярных молекул к алкену атомы водорода присоединяются к более гидрированным углеродам.
- 19. Качественные реакции на алкеныОбесцвечивание бромной воды;Обесцвечивание раствора
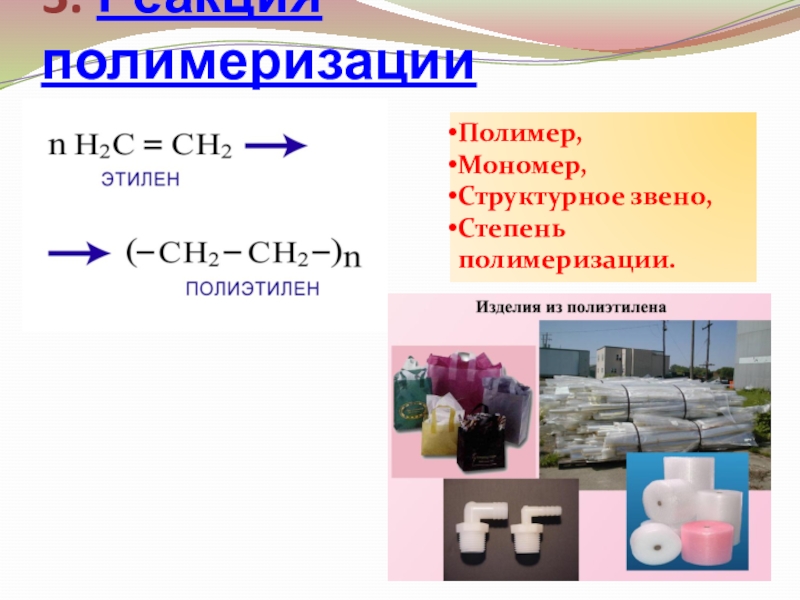
- 20. 3. Реакция полимеризацииПолимер,Мономер,Структурное звено,Степень полимеризации.
- 21. Домашнее заданиеИзучить § 9,10;Упр. 10 – 12, 13*, стр. 43
- 22. Упр. Этилен горит светящим пламенем в отличие
- 23. Упр. Найдите объём этилена (н.у.), полученного реакцией
- 24. Подведение итогов.Благодарю за работу
Слайд 2Из букв, соответствующих правильным ответам, составьте название продукта переработки метана, используемого
Повторение и контроль знаний по теме «Алканы». Задание:
Подчеркните названия смесей, в состав которых входит метан.
Слайд 3Проверим решение расчётной задачи!
задача) Вычислите количество теплоты, которая выделится при сгорании
n=500 моль Х кДж
СН4 +2 О2 = СО2 + 2Н2О + 900 кДж
1 моль 900 кДж
n(CH4) = 11200/22,4 = 500 моль
Х = 500 ˑ 900 /1 = 450000 кДж
3
Слайд 5Установите соответствие. Из букв, соответствующих правильным ответам, составьте название смеси твердых
Слайд 6Повторим виды химических реакций алканов!
Условия протекания, механизм, продукты.
Реакция горения;
Реакция разложения (полное,
Галогенирование (хлорирование, бромирование, фторирование, йодирование);
Реакция изомеризации;
Самостоятельная работа по теме «Химические свойства алканов»
Слайд 8Сегодня на уроке вы…
Познакомитесь со способами получения алкенов;
Выясните общую формулу гомологического
Научитесь составлять изомеры;
Освоите правила номенклатуры;
Познакомитесь с химическими свойствами алкенов.
Слайд 10Гомологический ряд этилена
С2Н4 – этилен, СН2 = СН2
С3Н6 – пропен,
С4Н8 – бутен, СН2= СН – СН2 – СН3
С5Н10 – пентен, СН2 = СН – СН2 – СН2 – СН3
Сформулируйте понятие «алкены»
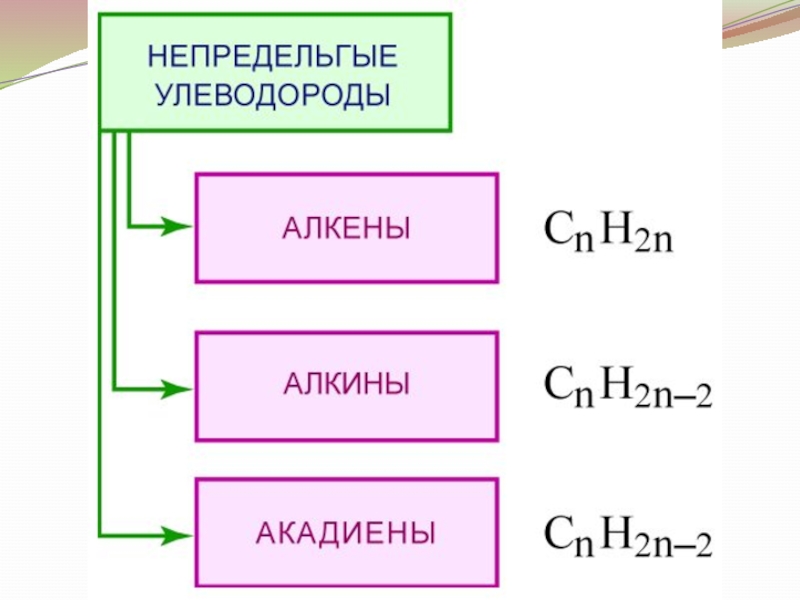
Алкены – непредельные УВ состава СnH2n, содержащие в молекуле, кроме одинарных связей, одну двойную углерод-углеродную связь (-C=C-).
Слайд 11Этилен
Бесцветный газ без запаха;
В воде плохо растворим;
Способен ускорять созревание плодов;
Идёт на
С2Н4
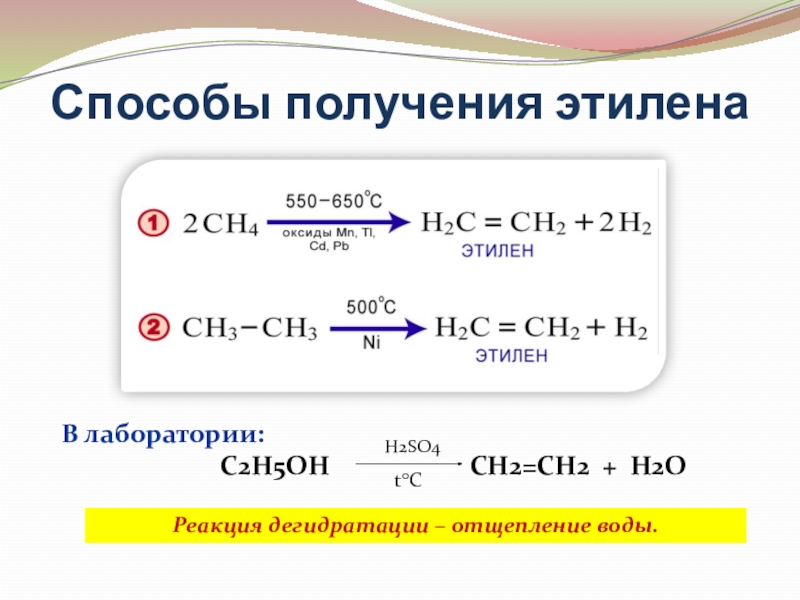
Слайд 12Способы получения этилена
В лаборатории:
H2SO4
t°C
Реакция дегидратации – отщепление воды.
Слайд 14Изомерия алкенов
Изомерия углеродного скелета.
Изомерия положения кратной связи;
Межклассовая изомерия.
Виды изомерии алкенов
Слайд 172. Реакции присоединения
Реакция гидрирования (+ Н2);
Гидратация;
Галогенирование;
Гидрогалогенирование
Слайд 18При присоединении полярных молекул к алкену атомы водорода присоединяются к более
Слайд 19Качественные реакции на алкены
Обесцвечивание бромной воды;
Обесцвечивание раствора перманганата калия.
Качественные реакции –
Слайд 22Упр. Этилен горит светящим пламенем в отличие от бесцветного пламени этана.
ω(С) в С2Н6 = 12ˑ 2/ 30 = 80%
ω(С) в С2Н4 = 12ˑ 2/ 28 = 86%
Слайд 23Упр. Найдите объём этилена (н.у.), полученного реакцией дегидратации 230 мл 95%-го
m(р-ра спирта) = 230 ˑ 0,8 = 184 г
m(спирта) = 184 ˑ 0,95 = 174,8 г
n(спирта) = 174,8 : 46 = 3,8 моль
3,8 моль Х моль
С2Н5ОН С2Н4 + Н2
1 моль 1 моль
n(C2H4) = n(C2H5OH) = 3,8моль
V(C2H2) = 3,8 ˑ 22,4 = 85,12л