- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
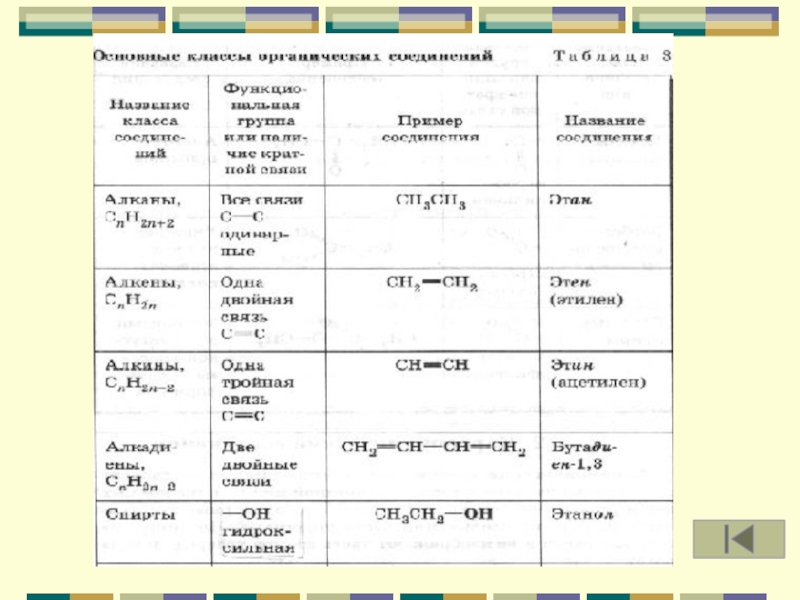
Презентация, доклад по химии на тему: Алканы и алкены
Содержание
- 1. Презентация по химии на тему: Алканы и алкены
- 2. Слайд 2
- 3. Строение.Все атомы углерода находятся в состоянии sp3-гибридизации.Форма
- 4. 1.Выбираем самую длинную углеродную цепь и получаем
- 5. Получение.1.Природные источники- нефть и газ.2.КрекингC10H22
- 6. CH4-C4H10-газы.CH4-газ без цвета,вкуса и запаха.C5H12-C15H32-жидкости (бензин).C16H34 и
- 7. Химические свойства алканов.Взаимодействие с галогенами.CH4+Cl2
- 8. 4.Реакция изомеризации.
- 9. Алкены (олефины).Строение.Атомы углерода находятся в sp2
- 10. Номенклатура алкенов.Выбрать самую длинную углеродную цепь, содержащую
- 11. Изомерия алкенов.Для алкенов характерны:Структурная изомерия:А)изомерия углеродного скелета;Б)изомерия
- 12. Получение алкенов.1.дегидрирование1.дегидрирование алканов(промышленный способ)CnH2n+2
- 13. Физические свойства алкенов.Первые три представителя гомологического ряда
- 14. Химические свойства алкенов.Для алкенов характерны реакции присоединения
Слайд 3Строение.
Все атомы углерода находятся в состоянии sp3-гибридизации.
Форма молекулы – тетраэдр.
Углы между
Длина связи углерод-углерод равна 0,154нм.
Изомерия.
Для алканов характерна структурная изомерия, а именно-изомерия углеродного скелета.
Пример:CH3-CH2-CH2-CH3 бутан, а изомером для него будет
CH3-CH-CH3
CH3
Алканы.
Слайд 41.Выбираем самую длинную углеродную цепь и получаем
основу названия.
2.Пронумеровать цепь так,
3.В названии арабскими цифрами указать положение заместителей, а приставками ди(2), три(3), тетра(4), пента(5),
число одинаковых заместителей.
4.При наличии разных заместителей, их названия перечислить в алфавитном порядке.
Номенклатура алканов.
Слайд 5Получение.
1.Природные источники- нефть и газ.
2.Крекинг
C10H22 С5H12+C5H10
3.Гидрирование3.Гидрирование
CH2=CH2+H2 C2H6
4.Синтез Вюрца.
2CH3-CH2-CH3-Br+2Na CH3-CH2-CH2-CH2-CH2-CH3+2NaBr
5.Получение метана (СН4) в лабораторных условиях.
Al4C3+12HOH 4Al(OH)3+3CH4
t
t
Слайд 6
CH4-C4H10-газы.
CH4-газ без цвета,вкуса и запаха.
C5H12-C15H32-жидкости (бензин).
C16H34 и далее-твердые тела.
Температура кипения и
Все углеводороды плохо растворяются в воде.
Жидкие углеводороды-органические растворители.
Физические свойства алканов.
Слайд 7Химические свойства алканов.
Взаимодействие с галогенами.
CH4+Cl2
2. Нитрование.
CH4+HNO3 CH3NO2+H2O
3. Окисление.
А) полное(горение).
C4H10+13O2 8CO2+10H2O
Б) неполное
C2H5OH
C2H6 CH3-C=О
Н
CH3-C=О
ОН
[О]
[О]
[О]
Слайд 84.Реакция изомеризации.
CH3-CH2-CH2-CH2-CH3 CH3-C-CH3
5.Разложение.
СН4 С+2Н2
СН4 СН СН+3Н2
СН3
СН3
t,кат.
10000
15000
Слайд 9
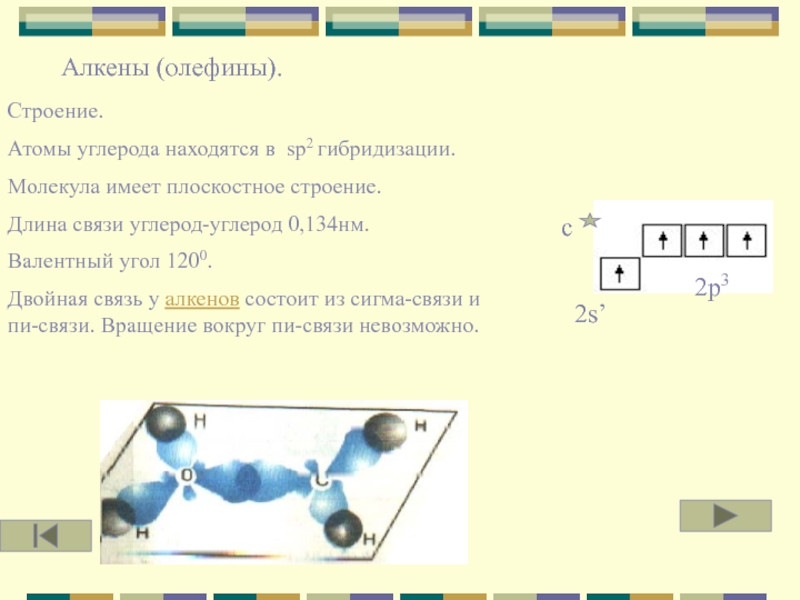
Алкены (олефины).
Строение.
Атомы углерода находятся в sp2 гибридизации.
Молекула имеет плоскостное
Длина связи углерод-углерод 0,134нм.
Валентный угол 1200.
Двойная связь у алкенов состоит из сигма-связи и пи-связи. Вращение вокруг пи-связи невозможно.
с
2s’
2p3
Слайд 10Номенклатура алкенов.
Выбрать самую длинную углеродную цепь, содержащую двойную связь.
2. Нумерация атомов
Пр.:
CH3-CH-CH2-CH=CH-CH3
CH3 5-МЕТИЛГЕКСЕН-2
3. Если по расположению двойной связи нельзя определить начало нумерации атомов в цепи, то нумерацию определяет положение заместителей.
4. Названия алкенов4. Названия алкенов формулируются так же, как и названия алканов. 4. Названия алкенов формулируются так же, как и названия алканов. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс, обозначающий принадлежность соединения к классу алкенов,-ен.
6 5 4 3 2 1
Слайд 11Изомерия алкенов.
Для алкенов характерны:
Структурная изомерия:
А)изомерия углеродного скелета;
Б)изомерия положения двойной связи.
Пр.: CH2=CH-CH2-CH3
В)изомерия углеводородов разных гомологических рядов.
СН2=СН-СН2-СН3 изомер – СН2-СН2 циклобутан.
СН2-СН2
Пространственная изомерия:
А)цис-изомерия;
Б)транс-изомерия.
Слайд 12Получение алкенов.
1.дегидрирование1.дегидрирование алканов(промышленный способ)
CnH2n+2 CnH2n+H2
2.дегидротация2.дегидротация спиртов
CH2-CH3
OH
3.дегидрогалогенирование
CnH2n+1Cl CnH2n+HCl
КОН
Н2SO4
t
Слайд 13Физические свойства алкенов.
Первые три представителя гомологического ряда алкенов в обычных условиях-
Слайд 14Химические свойства алкенов.
Для алкенов характерны реакции присоединения по месту разрыва пи-связи.
АлкеныАлкены
1.гидрирование
CnH2n+H2 CnH2n+2
2.галогенирование
CnH2n+Br2 CnH2nBr2
3.гидратация
CnH2n+H2O CnH2n+1OH
4.гидрогалогенирование
CnH2n+HCl CnH2n+1Cl
5.полимеризация
nCH2=CH2 (-CH2-CH2-)n
Уф.свет