- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Количество вещества (8 класс)
Содержание
- 1. Презентация по химии Количество вещества (8 класс)
- 2. Химия - наука о веществах …Что изучает химия?
- 3. Как и в каких единицах можно измерить вещество?
- 4. Для измерения вещества выбрана особая единица, которая
- 5. В порции вещества количеством 1 МОЛЬ содержится
- 6. Примеры:1) Аr (Н)=1, => 1
- 7. ОпределениеКоличество вещества - это физическая величина, которая
- 8. Определение Моль - это единица измерения количества
- 9. Постоянная Авогадро - это физическая величина, которая
- 10. Формула для определения числа частиц веществаN-число структурных
- 11. Определите число молекул, содержащихся в 2 моль
- 12. 3 моль водорода - 5 моль
- 13. Моль – порция веществаМоль – единица измерения
- 14. Молярная массаЭто физическая величина, которая показывает массу
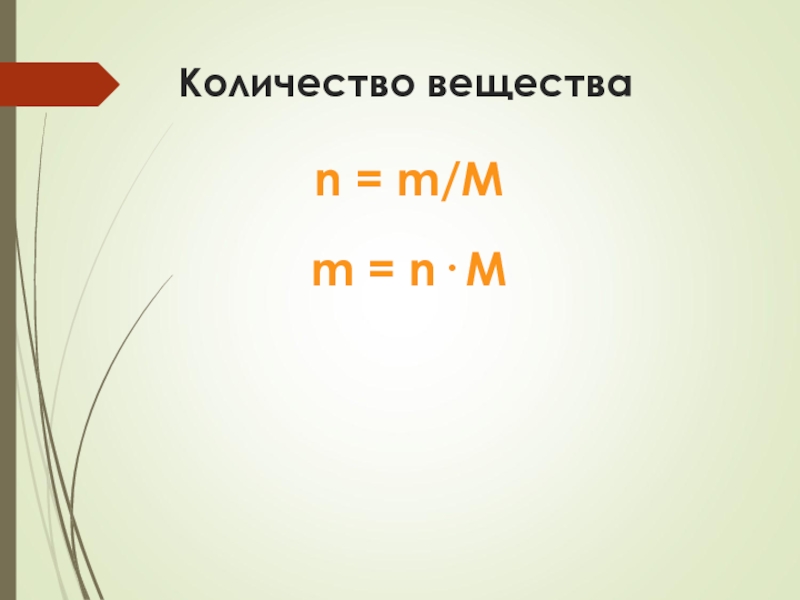
- 15. Количество веществаn = m/Mm = n· M
- 16. Заполняем таблицы 6 и 7, стр. 49Решаем задачи№ 8, стр. 49№ 10, стр. 50
- 17. Домашнее задание § 15В тетради на печатной основе Задание 9,11,12, стр. 50
- 18. Слайд 18
Химия - наука о веществах …Что изучает химия?
Слайд 4Для измерения вещества выбрана особая единица, которая соединяет в себе число
молекул и массу
Это единица измерения вещества - МОЛЬ
Это единица измерения вещества - МОЛЬ
Слайд 5В порции вещества количеством 1 МОЛЬ содержится 6· 1023 молекул (атомов)
данного вещества.
При этом масса порции вещества 1 моль численно равна относительной молекулярной массе этого вещества.
При этом масса порции вещества 1 моль численно равна относительной молекулярной массе этого вещества.
Слайд 6Примеры:
1) Аr (Н)=1, => 1 г элементарного водорода содержит
6 ·1023 атомов водорода
3) Mr (Н2)=2, => 2 г водорода содержат 6 ·1023 молекул водорода
2) Аr (Na)=23, => 23 г натрия содержат 6 ·1023 атомов натрия
3) Mr (N2)=28, => 28 г молекулярного азота содержат
6 ·1023 молекул азота
3) Mr (Н2)=2, => 2 г водорода содержат 6 ·1023 молекул водорода
2) Аr (Na)=23, => 23 г натрия содержат 6 ·1023 атомов натрия
3) Mr (N2)=28, => 28 г молекулярного азота содержат
6 ·1023 молекул азота
Слайд 7Определение
Количество вещества - это физическая величина, которая определяется числом структурных единиц
этого вещества (молекул, атомов, ионов);
обозначается n или ;
измеряется в моль.
обозначается n или ;
измеряется в моль.
Слайд 8Определение
Моль - это единица измерения количества вещества, то есть такая порция
вещества, которая содержит 6 ·1023 структурных частиц (молекул, атомов ) этого вещества.
Слайд 9Постоянная Авогадро
- это физическая величина, которая показывает содержание структурных частиц
(молекул, атомов ) в
1 моль вещества;
обозначается NA;
численно равна 6 ·1023
1 моль вещества;
обозначается NA;
численно равна 6 ·1023
Слайд 10Формула для определения числа частиц вещества
N-число структурных частиц (молекул, атомов и
др.)
N=NA · n
n= N/NA
N=NA · n
n= N/NA
Слайд 11Определите число молекул, содержащихся в 2 моль водорода.
N (H2)= 6
·1023 · 2 =
=12 ·1023 молекул
=12 ·1023 молекул
Слайд 123 моль водорода - 5 моль кислорода - 1 моль оксида углерода
-
2 моль азота -
1 моль хлора -
4 моль воды -
Определите число молекул, содержащихся в
24 ·1023
18 ·1023
30 ·1023
6 ·1023
12 ·1023
6 ·1023
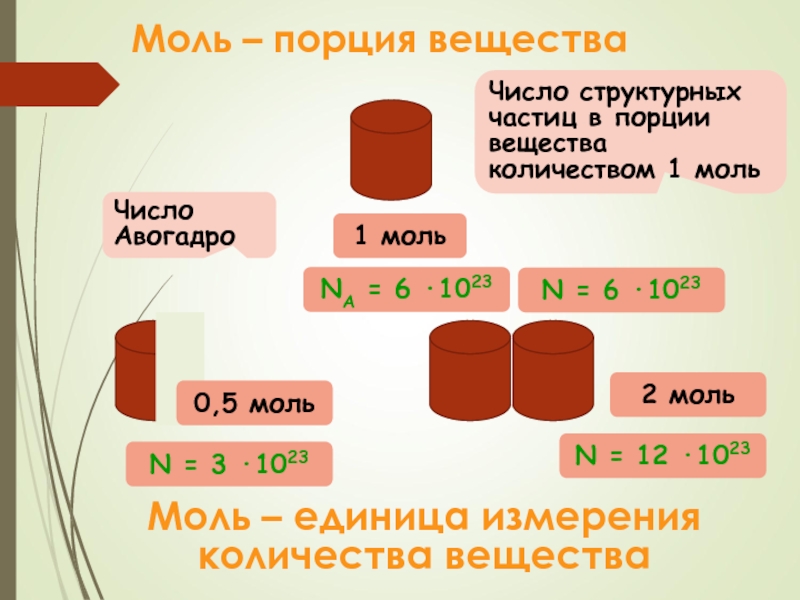
Слайд 13Моль – порция вещества
Моль – единица измерения количества вещества
Число структурных частиц
в порции вещества количеством 1 моль
Число Авогадро
1 моль
NA = 6 ·1023
2 моль
0,5 моль
N = 3 ·1023
N = 12 ·1023
N = 6 ·1023
Слайд 14Молярная масса
Это физическая величина, которая показывает массу 1 моль вещества.
Обозначается М
Численно
равна относительной молекулярной массе, Мr
Измеряется в г/моль
Измеряется в г/моль