- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии для 8 класса по теме Обзор неметаллов
Содержание
- 1. Презентация по химии для 8 класса по теме Обзор неметаллов
- 2. Положение неметаллов в периодической системе д. и.
- 3. Вещества - неметаллы могут быть жидкими, твердыми и газообразными
- 4. Для неметаллов характерно явление: аллотропия. Оно проявляется
- 5. Аллотропные модификации кислородаОзон (от греческого оzon —
- 6. Аллотропные модификации серы
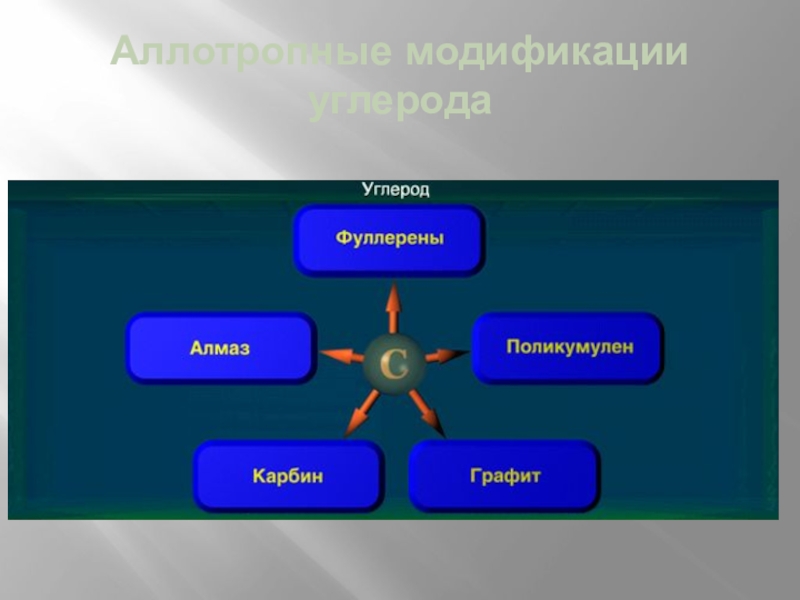
- 7. Аллотропные модификации углерода
- 8. Алмаз. Решетка алмаза очень прочная: атомы
- 9. Слайд 9
- 10. Белый фосфор. На воздухе он очень
- 11. Слайд 11
- 12. благородные газыБлагородные, а по-другому инертные газы, какими
- 13. Газообразный гелий используют как легкий газ для
- 14. Слайд 14
- 15. Картинка неметаллы- http://aleks-7zklass.narod.ru/p162aa1.html Схемы –таблицы http://ximijakatja.ucoz.ru/index/nemetally/0-77
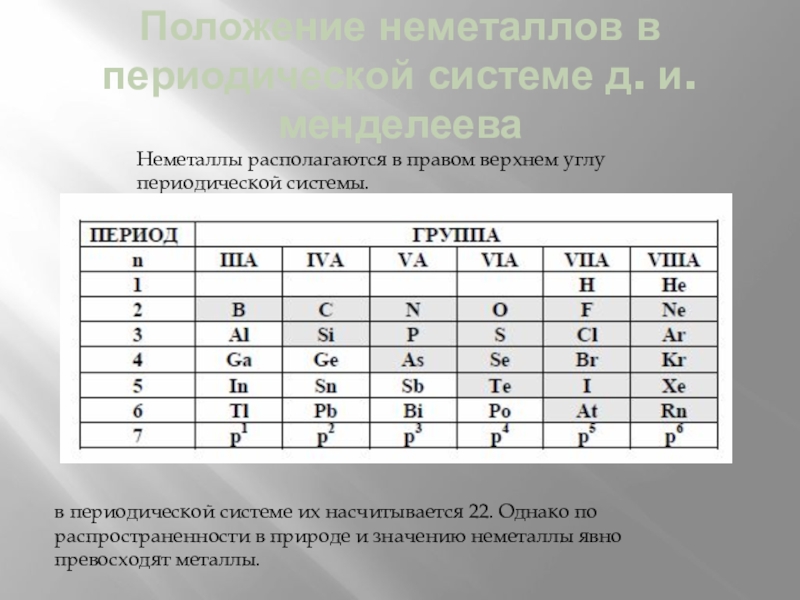
Слайд 2Положение неметаллов в периодической системе д. и. менделеева
Неметаллы располагаются в правом
в периодической системе их насчитывается 22. Однако по распространенности в природе и значению неметаллы явно превосходят металлы.
Слайд 4Для неметаллов характерно явление: аллотропия.
Оно проявляется в том, что один
Такие простые вещества, имеющие одинаковый качественный состав, но различающиеся по числу атомов в молекуле, имеют различные свойства.
Слайд 5Аллотропные модификации кислорода
Озон (от греческого оzon — пахнущий) — газ голубого
Кислород (О2)
Озон (О3)
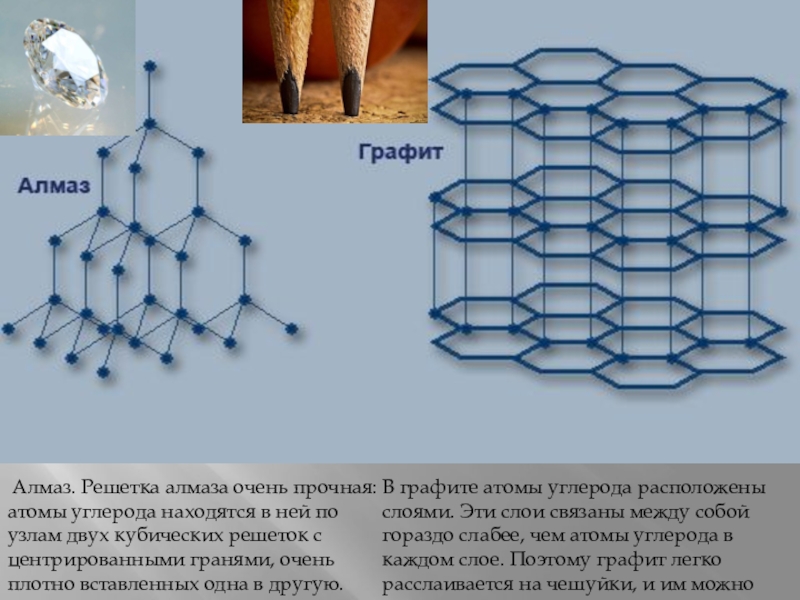
Слайд 8 Алмаз. Решетка алмаза очень прочная: атомы углерода находятся в ней
В графите атомы углерода расположены слоями. Эти слои связаны между собой гораздо слабее, чем атомы углерода в каждом слое. Поэтому графит легко расслаивается на чешуйки, и им можно писать
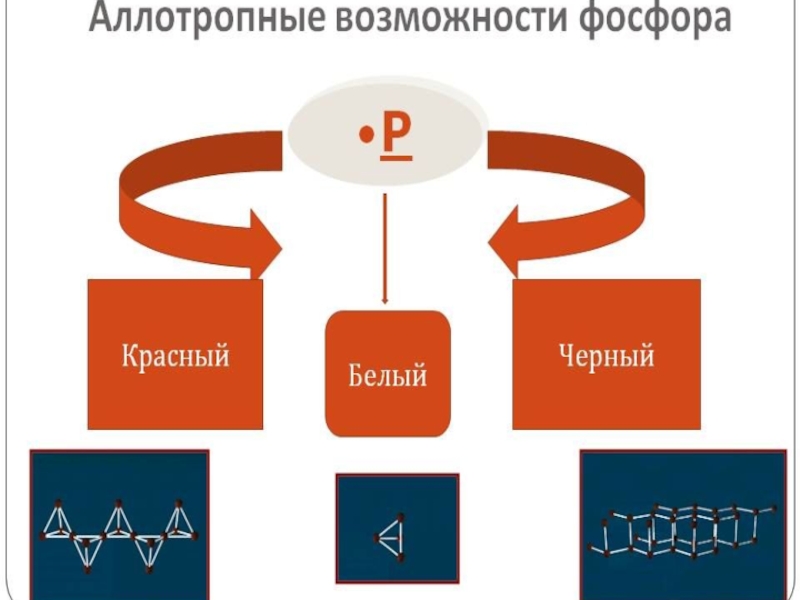
Слайд 10 Белый фосфор. На воздухе он очень быстро окисляется (начинает гореть)
Красный фосфор – это твердое вещество темно-красного цвета. Окисляется на воздухе он очень медленно, в темноте не светится, загорается только при нагревании, и он не является ядовитым. При сильном нагревании, при котором отсутствует доступ воздуха, он, не плавясь, превращается в пар, из которого при охлаждении и получается белый фосфор.
Черный фосфор получают из белого при 200 градусах Цельсия под высоким давлением. Он имеет слоистую структуру, металлический блеск и внешне похож на графит. Из всех твердых видов данного вещества он наименее активный
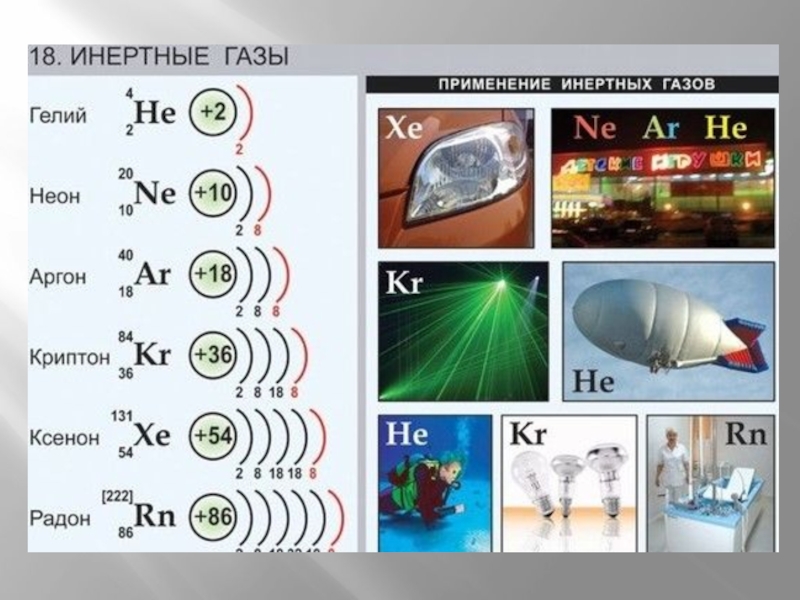
Слайд 12благородные газы
Благородные, а по-другому инертные газы, какими являются аргон, криптон, радон,
Благородные газы – бесцветные одноатомные газ без цвета и запаха, обладают более высокой электропроводностью по сравнению с другими газами и при прохождении через них тока ярко светятся: гелий ярко-жёлтым светом; неон огненно красным светом.
Слайд 13Газообразный гелий используют как легкий газ для наполнения воздушных шаров, применяют
Области применения ксенона. В светотехнике, им пользуются и медики—при рентгеноскопических обследованиях головного мозга
Продувкой аргона через жидкую сталь из нее удаляют газовые включения. Это улучшает свойства металла.Все шире применяется дуговая электросварка в среде
Вдыхание высших инертных газов (конечно в смеси с кислородом) приводит человека в состояние, сходное с опьянением алкоголем.
Слайд 15Картинка неметаллы- http://aleks-7zklass.narod.ru/p162aa1.html
Схемы –таблицы http://ximijakatja.ucoz.ru/index/nemetally/0-77
Аллотропия кислорода http://900igr.net/kartinki/khimija/Prostye-veschestva-nemetally/038-Allotropija-kisloroda.html
Озон
Алмаз и графит http://www.uraldiamond.ru/index.asp?ID=41
Аллотропия фосфора http://fb.ru/article/41646/belyiy-fosfor-krasnyiy-i-chernyiy---harakteristiki-i-primenenie и
( яндекс – картинки)
Благородные газы - http://zablugdeniyam-net.ru/priroda/blagorodnye-gazy/ http://www.spishy.ru/referats/7/1950