- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии для 11 класса на тему: Ферменты
Содержание
- 1. Презентация по химии для 11 класса на тему: Ферменты
- 2. Оглавление 1.Притча о верблюдах.2.Создание проблемной ситуации:А) Демонсрационный
- 3. Оглавление8.Результаты исследовательских работ:а.Действие ферментов желудочного сока на белкиб.Специфичность действия ферментов:лактаза, уреаза.амилаза и сахараза9.Каталитическая активность ферментов
- 4. ОпределениеФерменты – биологические катализаторы белковой природы, ускоряющие
- 5. Строение ферментов1.двухкомпонентными - сложными белками Характерной особенностью
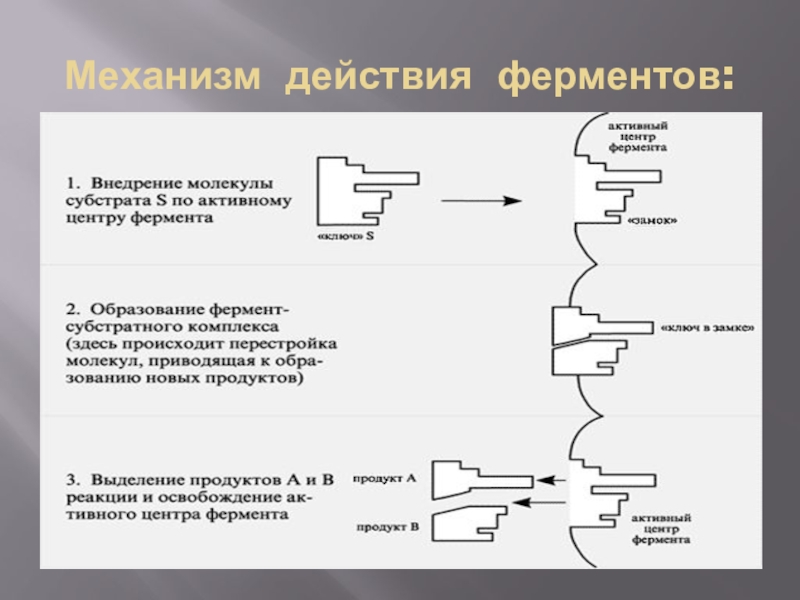
- 6. Механизм действия ферментов:
- 7. Механизм действия ферментаЕ + S → Е
- 8. Исчезновение каталитической активности фермента:При денатурации фермента его каталитическая активность исчезает, т.к. нарушается структура активного центра.
- 9. Центры в молекуле фермента:1.Активный центр:-присоединяет субстрат;2.Аллостерическийцентр:присоединяет низкомолекулярныевещества-активаторы или ингибиторы
- 10. Свойства ферментов:Термолабильность - изменчивость фермента под влиянием температуры.При
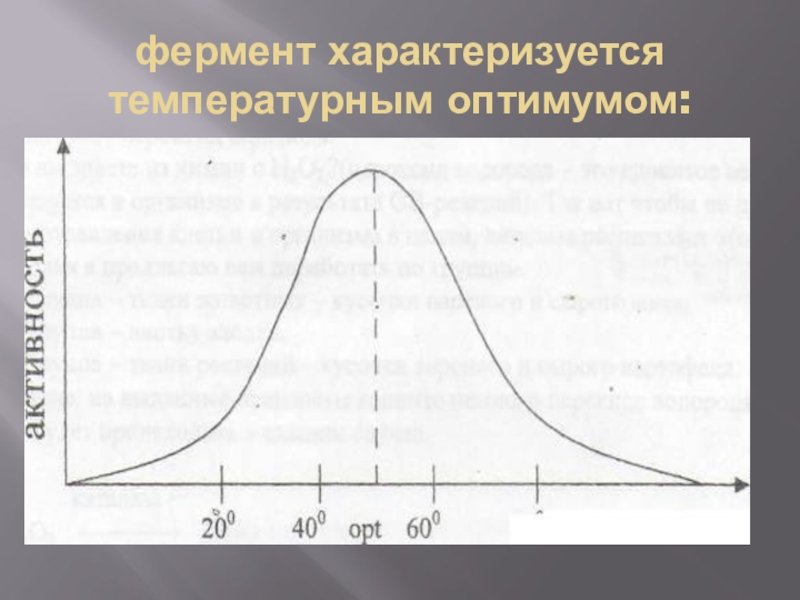
- 11. фермент характеризуется температурным оптимумом:
- 12. Температурные оптимумы:1.Для ферментов животного происхождения topt = 40-502. для ферментов растительного происхождения -50-60°3. для человека ~ 37°.
- 13. Влияние РН на активность ферментов:1) амилаза слюны:
- 14. Лактаза- молочный сахар(лактозу)---глюкоза + галактозаУреаза—мочевину---Аммиак + углекислый газ
- 15. Скорость расщепления уреазы:За 1 секунду 1 молекула
- 16. Номенклатура ферментовСейчас используется новая номенклатура ферментов, принятая
- 17. Свойства ферментовФерменты обладают такими общими для всех
- 18. Денатурация белка -- это разрушение вторичной и
- 19. Свойства ферментовФерменты обладают также уникальными свойствами:Необычно высокая
- 20. Свойства ферментовВысокая специфичность ферментов. Благодаря данному свойству
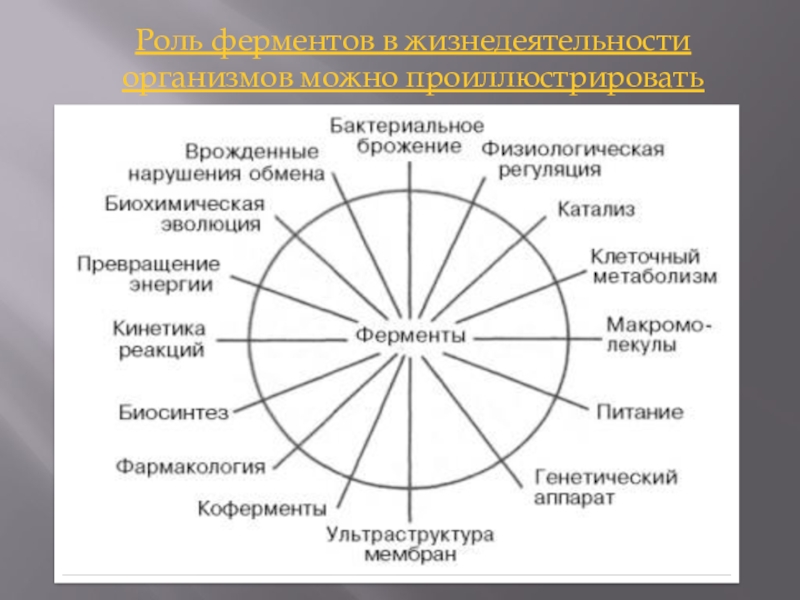
- 21. Роль ферментов в жизнедеятельности организмов можно проиллюстрировать схемой:
- 22. Особенности ферментовМногие ферменты наиболее эффективны при температуре
- 23. Особенности ферментовФерменты наиболее эффективно действуют при строго
- 24. ПрименениеФерменты используются в производстве:Пищи и напитков(вино, хлеб, сыр)Медикаментов («Пепсин», «Мезим», «Фестал»)Моющих средствТекстиляБумаги
- 25. Классификация ферментов:Названия ферментов происходятот: типа катализируемой данным
- 26. Классификация ферментов:--Оксидоредуктазы.--Трансферазы.--Гидролазы.--Лиазы.--Изомеразы.--Лигазы (Синтетазы)
- 27. Применение ферментов:--. в животноводстве --при изготовлении фотоматериалов--при
- 28. Применение ферментов:ферменты применяются более чем в 25 отраслях промышленности
- 29. Обобщение знаний:1.Что такое ферменты? 2. Какими свойствами
- 30. Вывод по изученной теме:Как вы понимаете выражение:
- 31. Проверь себя: ТЕСТ
- 32. Тест1.(3 балла). Класс соединений, к которому относятся ферменты:А. БелкиБ. ЖирыВ. Углеводы.Г. Нуклеиновые кислоты.
- 33. Тест1.(3 балла). Класс соединений, к которому относятся ферменты:А. БелкиБ. ЖирыВ. Углеводы.Г. Нуклеиновые кислоты.
- 34. Тест2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:А. АминокислотыБ. Углеводороды.В. Углеводы.Г. Высшие (жирные) кислоты.
- 35. Тест2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:А. АминокислотыБ. Углеводороды.В. Углеводы.Г. Высшие (жирные) кислоты.
- 36. Тест3.(3 балла). Продуктами гидролиза белков являются:А. Глюкоза.Б. Аминокислоты.В. Глицерин и жирные кислоты.Г. Нуклеотиды.
- 37. Тест3.(3 балла). Продуктами гидролиза белков являются:А. Глюкоза.Б. Аминокислоты.В. Глицерин и жирные кислоты.Г. Нуклеотиды.
- 38. Тест4. (3 балла). Температура, при которой ферменты
- 39. Тест4. (3 балла). Температура, при которой ферменты
- 40. Тест5.(3 балла). Селективностью (избирательностью) действия ферментов называется:А.
- 41. Тест5.(3 балла). Селективностью (избирательностью) действия ферментов называется:А.
- 42. Тест6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее активен:А. 1,5—2,0. Б. 3,0—4,0. В. 5,0—6,0.Г. 7,0—8,0.
- 43. Тест6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее активен:А. 1,5—2,0. Б. 3,0—4,0. В. 5,0—6,0.Г. 7,0—8,0.
- 44. Тест7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:А. Амилаза. Б. Пепсин.В. Каталаза.Г. Фицин
- 45. Тест7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:А. Амилаза. Б. Пепсин.В. Каталаза.Г. Фицин
- 46. Тест8.(3 балла). Фермент трипсин расщепляет:А. Углеводы. Б. Белки. В. Жиры.Г. Нуклеиновые кислоты.
- 47. Тест8.(3 балла). Фермент трипсин расщепляет:А. Углеводы. Б. Белки. В. Жиры.Г. Нуклеиновые кислоты.
- 48. Тест9.(3 балла). Высокая эффективность ферментов объясняется:А. Быстрым
- 49. Тест9.(3 балла). Высокая эффективность ферментов объясняется:А. Быстрым
- 50. Тест10.(3 балла). Отдел желудка жвачных животных, в
- 51. Тест10.(3 балла). Отдел желудка жвачных животных, в
- 52. Домашнее задание.§ 19 учебника. Ответить на вопросы
- 53. Список литературы1. Габриелян О.С.,А.В.Яшукова Методическое пособие. Химия.
- 54. Интернет -ресурсыhttp://files.school-collection.edu.ru/dlrstore/d7794640-8cff-11db-b606-0800200c9a66/ch10_30_02.swfhttp://files.school-collection.edu.ru/dlrstore/d7791f54-8cff-11db-b606-0800200c9a66/ch10_30_01.swf
Слайд 2Оглавление
1.Притча о верблюдах.
2.Создание проблемной ситуации:
А) Демонсрационный опыт с пероксидом водорода;
1.Определение-
2.История вопроса о ферментах
3.Строение ферментов
4.Механизм действия ферментов
5.Свойства ферментов .
6.Многообразие ферментов
7.Классификация ферментов
Слайд 3Оглавление
8.Результаты исследовательских работ:
а.Действие ферментов желудочного сока на белки
б.Специфичность действия ферментов:
лактаза,
амилаза и сахараза
9.Каталитическая активность ферментов
Слайд 4Определение
Ферменты – биологические катализаторы белковой природы, ускоряющие химические реакции в живых
На данный момент химикам известно более 2000 ферментов
Слайд 5Строение ферментов
1.двухкомпонентными - сложными белками
Характерной особенностью двухкомпонентного фермента
является то, что
отдельности не обладают заменой каталитической активностью.
Только их комплекс проявляет ферментативные свойства.
2.однокомпонентными -простыми белками;
Иначе обстоит дело у однокомпонентных ферментов, не имеющих
добавочной группы, которая могла бы входить в
непосредственный контакт с преобразуемым соединением. Эту
функцию выполняет часть белковой молекулы, называемая
каталитическим центром.
По строению ферменты могут быть:
Слайд 7Механизм действия фермента
Е + S → Е S → Е S
фермент субстрат фермент- преобразованный фермент- фермент продукт
субстратный фермент- продуктивный
комплекс субстратный комплекс
комплекс
Слайд 8Исчезновение каталитической активности фермента:
При денатурации фермента его каталитическая активность исчезает,
т.к.
Слайд 9Центры в молекуле фермента:
1.Активный центр:
-присоединяет субстрат;
2.Аллостерический
центр:
присоединяет низкомолекулярные
вещества-активаторы или ингибиторы
Слайд 10Свойства ферментов:
Термолабильность - изменчивость фермента под влиянием температуры.
При возрастании температуры активность фермента
определенной температуры, начинает снижаться.
Слайд 12Температурные оптимумы:
1.Для ферментов животного происхождения topt = 40-50
2. для ферментов растительного происхождения -50-60°
3.
Слайд 13Влияние РН на активность ферментов:
1) амилаза слюны: РН = 7 (нейтральная
2) пепсин желудочного сока действует в кислой среде (РН=1,5-2,5),
3) трипсин кишечного сока имеет РН = 8-9 (щелочная среда).
Слайд 14Лактаза- молочный сахар
(лактозу)---
глюкоза + галактоза
Уреаза—мочевину---
Аммиак + углекислый газ
Слайд 15Скорость расщепления уреазы:
За 1 секунду 1 молекула уреазы расщепляет 30.000 молекул
Слайд 16Номенклатура ферментов
Сейчас используется новая номенклатура ферментов, принятая в 1961 году. В
Слайд 17Свойства ферментов
Ферменты обладают такими общими для всех белков свойствами, как:
Способность к
Амфотерность (способность проявлять в зависимости от условий как кислотные, так и основные свойства)
Способность к денатурации и гидролизу
Протекание цветных реакций (биуретовой и ксантопротеиновой)
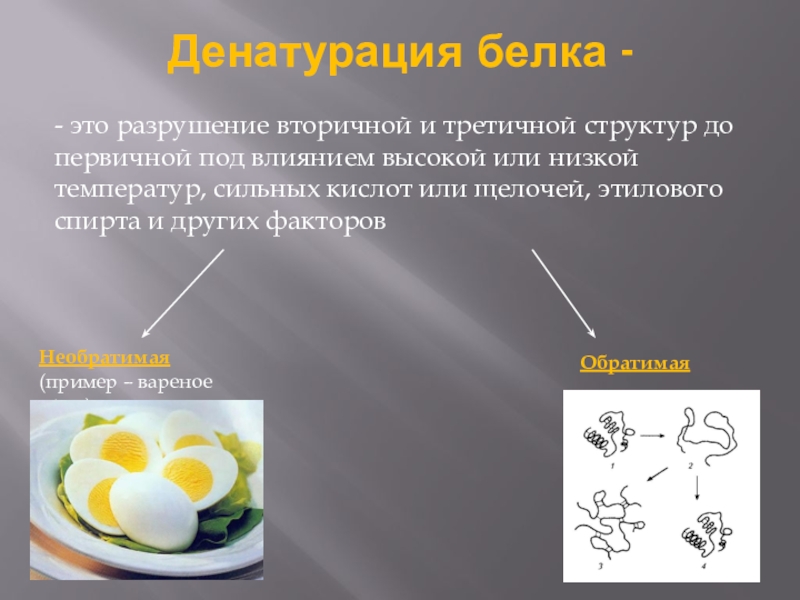
Слайд 18Денатурация белка -
- это разрушение вторичной и третичной структур до первичной
Необратимая
(пример – вареное яйцо)
Обратимая
Слайд 19Свойства ферментов
Ферменты обладают также уникальными свойствами:
Необычно высокая каталитическая активность. Так, добавка
Селективность (избирательность) действия – определяется их способностью превращать только данный тип субстратов в определенных реакциях и условиях
-9
-7
8
12
Слайд 20Свойства ферментов
Высокая специфичность ферментов. Благодаря данному свойству в организме не воцаряется
Стабильность – способность сохранять каталитическую активность при определенных условиях
Эффективность – скорость некоторых ферментативный реакций может быть в 10 раз больше скорости реакций, протекающих в их отсутствие
15
Слайд 22Особенности ферментов
Многие ферменты наиболее эффективны при температуре человеческого тела (35-42 С).
Слайд 23Особенности ферментов
Ферменты наиболее эффективно действуют при строго определенной среде раствора, при
Например, пепсин наиболее активен при pH от 1,5 до 2,0; каталаза крови – при pH, равном 7,0
Слайд 24Применение
Ферменты используются в производстве:
Пищи и напитков(вино, хлеб, сыр)
Медикаментов («Пепсин», «Мезим», «Фестал»)
Моющих
Текстиля
Бумаги
Слайд 25Классификация ферментов:
Названия ферментов происходят
от:
типа катализируемой данным ферментом реакции + название
Окончание -аза служит для обозначения ферментной природы
Слайд 26 Классификация ферментов:
--Оксидоредуктазы.
--Трансферазы.
--Гидролазы.
--Лиазы.
--Изомеразы.
--Лигазы (Синтетазы)
Слайд 27Применение ферментов:
--. в животноводстве
--при изготовлении фотоматериалов
--при обработке овса и конопли.
--для
--в состав стиральных порошков, зубных паст.
-- медицине ( диагностическое значение )
--для превращения химической энергии в электрическую.
Слайд 29Обобщение знаний:
1.Что такое ферменты?
2. Какими свойствами они обладают?
3.Чем объяснить
Слайд 30Вывод по изученной теме:
Как вы понимаете выражение:
«Все ферменты - белки,
но не все белки - ферменты»?
Слайд 32Тест
1.(3 балла). Класс соединений, к которому относятся ферменты:
А. Белки
Б. Жиры
В. Углеводы.
Г.
Слайд 33Тест
1.(3 балла). Класс соединений, к которому относятся ферменты:
А. Белки
Б. Жиры
В. Углеводы.
Г.
Слайд 34Тест
2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:
А. Аминокислоты
Б. Углеводороды.
В. Углеводы.
Г.
Слайд 35Тест
2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:
А. Аминокислоты
Б. Углеводороды.
В. Углеводы.
Г.
Слайд 36Тест
3.(3 балла). Продуктами гидролиза белков являются:
А. Глюкоза.
Б. Аминокислоты.
В. Глицерин и жирные
Г. Нуклеотиды.
Слайд 37Тест
3.(3 балла). Продуктами гидролиза белков являются:
А. Глюкоза.
Б. Аминокислоты.
В. Глицерин и жирные
Г. Нуклеотиды.
Слайд 38Тест
4. (3 балла). Температура, при которой ферменты в организме человека наиболее
А. 10 °С.
Б. 30 °С.
В. 37 °С.
Г. 40 °С.
Слайд 39Тест
4. (3 балла). Температура, при которой ферменты в организме человека наиболее
А. 10 °С.
Б. 30 °С.
В. 37 °С.
Г. 40 °С.
Слайд 40Тест
5.(3 балла). Селективностью (избирательностью) действия ферментов называется:
А. Способность фермента ускорять одну
Б. Способность фермента ускорять любые реакции.
В. Способность фермента замедлять любые реакции.
Г. Способность фермента замедлять одну или группу однотипных реакций.
Слайд 41Тест
5.(3 балла). Селективностью (избирательностью) действия ферментов называется:
А. Способность фермента ускорять одну
Б. Способность фермента ускорять любые реакции.
В. Способность фермента замедлять любые реакции.
Г. Способность фермента замедлять одну или группу однотипных реакций.
Слайд 42Тест
6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее
А. 1,5—2,0.
Б. 3,0—4,0.
В. 5,0—6,0.
Г. 7,0—8,0.
Слайд 43Тест
6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее
А. 1,5—2,0.
Б. 3,0—4,0.
В. 5,0—6,0.
Г. 7,0—8,0.
Слайд 44Тест
7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:
А.
Б. Пепсин.
В. Каталаза.
Г. Фицин
Слайд 45Тест
7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:
А.
Б. Пепсин.
В. Каталаза.
Г. Фицин
Слайд 46Тест
8.(3 балла). Фермент трипсин расщепляет:
А. Углеводы.
Б. Белки.
В. Жиры.
Г. Нуклеиновые кислоты.
Слайд 47Тест
8.(3 балла). Фермент трипсин расщепляет:
А. Углеводы.
Б. Белки.
В. Жиры.
Г. Нуклеиновые кислоты.
Слайд 48Тест
9.(3 балла). Высокая эффективность ферментов объясняется:
А. Быстрым восстановлением их молекул в
Б. Многообразием ферментов.
В. Высокой активностью молекул ферментов.
Г. Все предыдущие ответы верны.
Слайд 49Тест
9.(3 балла). Высокая эффективность ферментов объясняется:
А. Быстрым восстановлением их молекул в
Б. Многообразием ферментов.
В. Высокой активностью молекул ферментов.
Г. Все предыдущие ответы верны.
Слайд 50Тест
10.(3 балла). Отдел желудка жвачных животных, в котором вырабатывается фермент реннин,
А. Сетка.
Б. Книжка.
В. Сычуг.
Г. Рубец.
Слайд 51Тест
10.(3 балла). Отдел желудка жвачных животных, в котором вырабатывается фермент реннин,
А. Сетка.
Б. Книжка.
В. Сычуг.
Г. Рубец.
Слайд 52Домашнее задание.
§ 19 учебника. Ответить на вопросы и выполнить задания после
Подготовить презентацию «Витамины»
10-12 слайдов.
Слайд 53Список литературы
1. Габриелян О.С.,А.В.Яшукова Методическое пособие. Химия. 10 класс.(базовый уровень) ,
2. Габриелян О.С.Химия.10 класс: контрольные и проверочные работы-М. Дрофа,2011
3. Власова З. А. Биология. Справочник школьника. Всероссийское слово, 1995 г.
4. Хомченко Г. Л. Химия для поступающих в ВУЗЫ. Высшая школа,1993 г.
5. Биологический энциклопедический словарь. Советская энциклопедия, 1987г.