Практическая работа № 6
«Решение экспериментальных задач по теме
«Металлы и их соединения»
Учитель Ивлева Е.Н.
Орлов
2018
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 9 класс Практическая работа № 6 Решение экспериментальных задач по теме Металлы и их соединения
Содержание
- 1. Презентация по химии 9 класс Практическая работа № 6 Решение экспериментальных задач по теме Металлы и их соединения
- 2. Практическая работа № 6
- 3. Иду на мелкую монету,В колоколах люблю звенеть,Мне ставят памятник за этоИ знают: имя мое - ...
- 4. Правила техники безопасности1. Проводите опыты лишь с
- 5. Решение уравнений2Cu+O2 = 2CuO – реакция соединенияCuO+
- 6. Слайд 6
- 7. Cu→CuO →CuSO4→Cu(OH)2 →CuCl2Вывод: В ходе практической работы
- 8. СПАСИБО ЗА УРОК
Практическая работа № 6 ТЕМА: Решение экспериментальных задач по теме «Металлы и их соединения» Цель: Показать связь между металлами и их соединениямиОборудование: пробирки, штатив, сухое горючее, держатель для пробирок, медная проволока, реактивы: оксид
Слайд 1ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «ОРЛОВСКОЕ СПЕЦИАЛЬНОЕ УЧЕБНО – ВОСПИТАТЕЛЬНОЕ
УЧРЕЖДЕНИЕ ЗАКРЫТОГО ТИПА»
Слайд 2 Практическая работа № 6 ТЕМА: Решение экспериментальных задач по теме
«Металлы и их соединения»
Цель: Показать связь между металлами и их соединениями
Оборудование: пробирки, штатив, сухое горючее, держатель для пробирок, медная проволока, реактивы: оксид меди (CuO), щелочь (NaOH), соляная кислота (HCl), серная кислота (H2SO4)
Слайд 3Иду на мелкую монету,
В колоколах люблю звенеть,
Мне ставят памятник за это
И
знают: имя мое - ...
Слайд 4Правила техники безопасности
1. Проводите опыты лишь с теми веществами, которые указаны
учителем.
2. Не пробуйте вещества на вкус.
3. При выяснении запаха не подносите сосуд близко к лицу. Для выяснения запаха нужно ладонью руки сделать движение от отверстия сосуда к носу.
4. Нагревая пробирку с жидкостью, держите ее так, чтобы открытый конец ее был направлен в сторону от себя и от соседа.
5. Опыты производите только над столом.
6. Нельзя переносить спиртовку во время работы в зажжённом виде с одного стола на другой. Тушить только колпачком – не дуть!
7. В случае пореза, ожога немедленно
обращайтесь к учителю.
8. Обращайтесь бережно с посудой,
веществами и лабораторным
оборудованием.
9. Закончив работу, приведите
рабочее место в порядок.
2. Не пробуйте вещества на вкус.
3. При выяснении запаха не подносите сосуд близко к лицу. Для выяснения запаха нужно ладонью руки сделать движение от отверстия сосуда к носу.
4. Нагревая пробирку с жидкостью, держите ее так, чтобы открытый конец ее был направлен в сторону от себя и от соседа.
5. Опыты производите только над столом.
6. Нельзя переносить спиртовку во время работы в зажжённом виде с одного стола на другой. Тушить только колпачком – не дуть!
7. В случае пореза, ожога немедленно
обращайтесь к учителю.
8. Обращайтесь бережно с посудой,
веществами и лабораторным
оборудованием.
9. Закончив работу, приведите
рабочее место в порядок.
Слайд 5Решение уравнений
2Cu+O2 = 2CuO – реакция соединения
CuO+ H2SO4= CuSO4+ H2O реакция
обмена
CuO+ 2H++SO2-4= Cu2++SO4+ H+2O2-
CuO+ 2H+= Cu2++ H+2O2-
Cu2+SO2-4+2Nа+ОН-=Cu2+(ОН)-2+Nа+2SO2-4 реакция обмена
Cu2++SO2-4+2Nа++2ОН-=Cu(ОН)2+ 2Nа++SO42-
Cu2++2ОН-=Cu(ОН)2нерастворимое основание
CuO+ 2H++SO2-4= Cu2++SO4+ H+2O2-
CuO+ 2H+= Cu2++ H+2O2-
Cu2+SO2-4+2Nа+ОН-=Cu2+(ОН)-2+Nа+2SO2-4 реакция обмена
Cu2++SO2-4+2Nа++2ОН-=Cu(ОН)2+ 2Nа++SO42-
Cu2++2ОН-=Cu(ОН)2нерастворимое основание
Cu(ОН)2+ 2H+Cl- = Cu2+Cl-2 + 2H+2O2- реакция обмена
Cu(ОН)2+2H++2Cl-= Cu2++2Cl- + 2H2O
Cu(ОН)2+ 2H+= Cu2++ 2H+2O2-
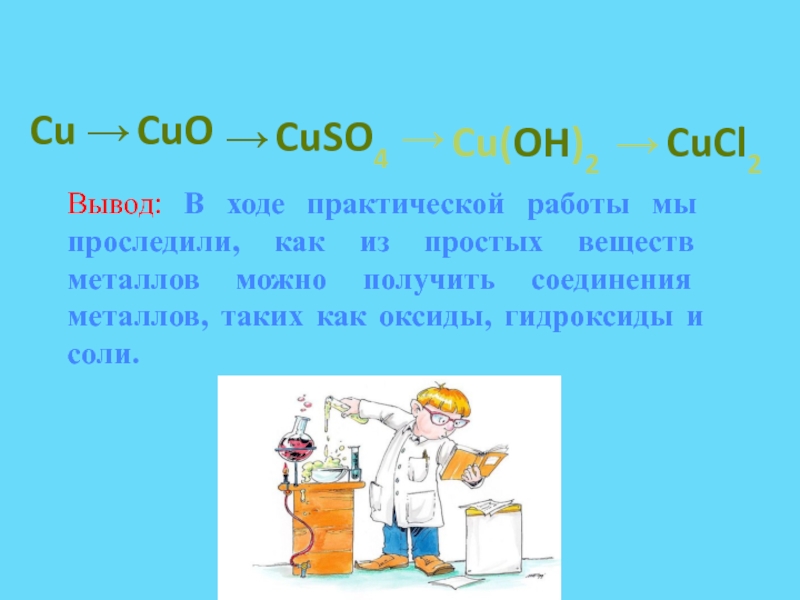
Слайд 7Cu
→
CuO
→
CuSO4
→
Cu(OH)2
→
CuCl2
Вывод: В ходе практической работы мы проследили, как из
простых веществ металлов можно получить соединения металлов, таких как оксиды, гидроксиды и соли.