- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 9 класс Азотная кислота
Содержание
- 1. Презентация по химии 9 класс Азотная кислота
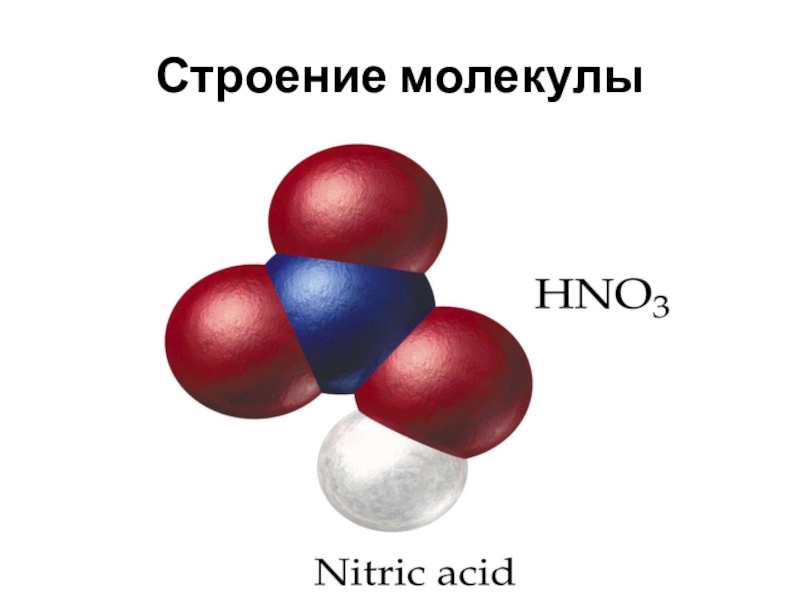
- 2. Строение молекулы
- 3. ПолучениеРазличают производство слабой (разбавленной) азотной кислоты и
- 4. ПолучениеРисунок1.1 –Технологическая схема производства азотной кислоты АК-72:
- 5. Физические свойства Бесцветная, концентрированная азотная кислота на
- 6. Химические свойстваТермическое разложение:
- 7. Взаимодействие с металламиЗолото, некоторые металлы платиновой группы
- 8. Взаимодействие с металламиа) с металлами, стоящими в
- 9. Взаимодействие с металламиЕдинственная общая закономерность при взаимодействии
- 10. Взаимодействие с металлами С золотом и платиной азотная
- 11. Слайд 11
- 12. Взаимодействие с неметалламиАзотная кислота окисляет неметаллы, при этом азот обычно восстанавливается до NO или NO2:
- 13. HNO3 как сильная одноосновная кислота взаимодействует: а)
- 14. Смесь трех объёмов соляной кислоты и одного
- 15. Применениев производстве минеральных удобрений;в военной промышленности (дымящая —
- 16. Действие на организм Азотная кислота
Строение молекулы
Слайд 3Получение
Различают производство слабой (разбавленной) азотной кислоты и производство концентрированной азотной кислоты.
Процесс
производства разбавленной азотной кислоты складывается из трех стадий:
1) конверсии аммиака с целью получения оксида азота 4NH3 + 5О2 → 4NO + 6Н2О
2) окисления оксида азота до диоксида азота 2NO + О2 → 2NO2
3) абсорбции оксидов азота водой 4NO2 + О2 + 2Н2О → 4HNO3
Суммарная реакция образования азотной кислоты выражается NH3 + 2О2 → HNO3 + Н2О
1) конверсии аммиака с целью получения оксида азота 4NH3 + 5О2 → 4NO + 6Н2О
2) окисления оксида азота до диоксида азота 2NO + О2 → 2NO2
3) абсорбции оксидов азота водой 4NO2 + О2 + 2Н2О → 4HNO3
Суммарная реакция образования азотной кислоты выражается NH3 + 2О2 → HNO3 + Н2О
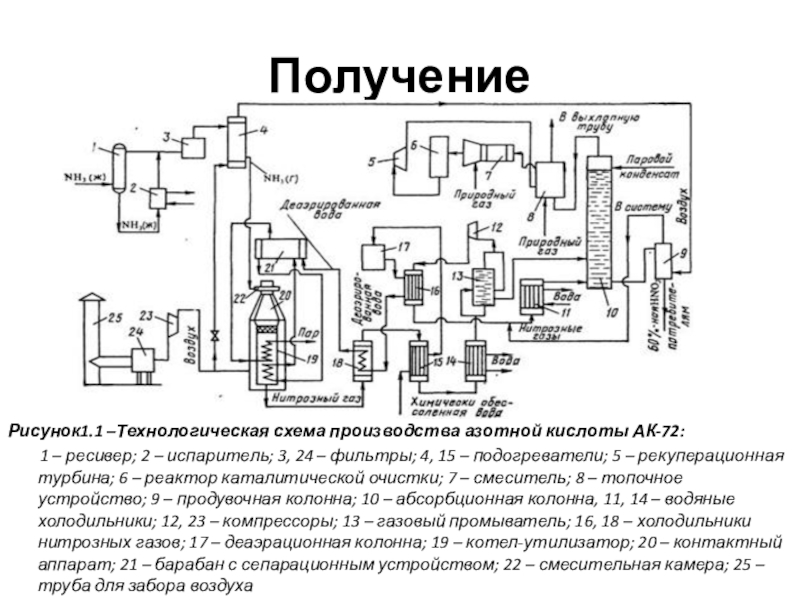
Слайд 4Получение
Рисунок1.1 –Технологическая схема производства азотной кислоты АК-72:
1
– ресивер; 2 – испаритель; 3, 24 – фильтры; 4, 15 – подогреватели; 5 – рекуперационная турбина; 6 – реактор каталитической очистки; 7 – смеситель; 8 – топочное устройство; 9 – продувочная колонна; 10 – абсорбционная колонна, 11, 14 – водяные холодильники; 12, 23 – компрессоры; 13 – газовый промыватель; 16, 18 – холодильники нитрозных газов; 17 – деаэрационная колонна; 19 – котел-утилизатор; 20 – контактный аппарат; 21 – барабан с сепарационным устройством; 22 – смесительная камера; 25 – труба для забора воздуха
Слайд 5Физические свойства
Бесцветная, концентрированная азотная кислота на воздухе дымит. Очень
быстро становится коричневого (бурого) цвета из-за реакции разложения:
4HNO3 = 4NO2 + 2H2O + O2
4HNO3 = 4NO2 + 2H2O + O2
Слайд 7Взаимодействие с металлами
Золото, некоторые металлы платиновой группы и тантал инертны к
азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется её концентрацией.
Некоторые металлы (железо, хром, алюминий, кобальт, никель, марганец, бериллий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
Некоторые металлы (железо, хром, алюминий, кобальт, никель, марганец, бериллий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
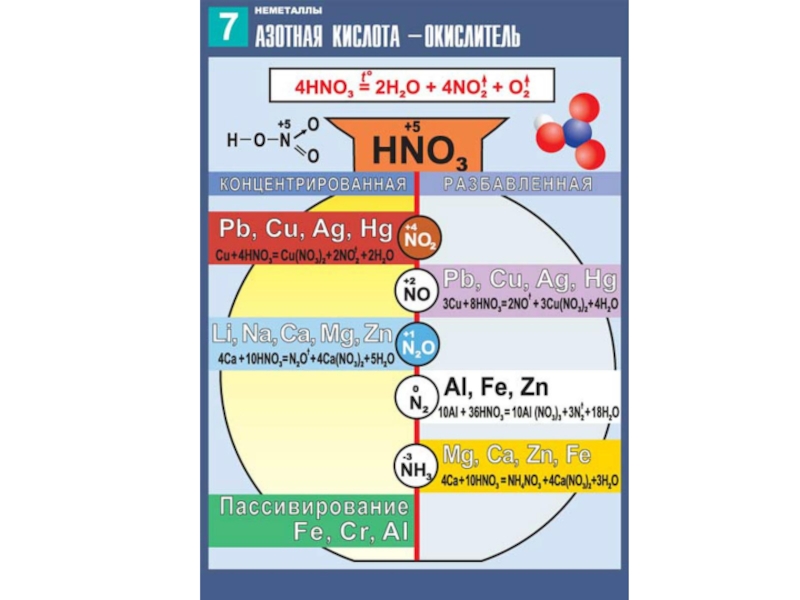
Слайд 8Взаимодействие с металлами
а) с металлами, стоящими в ряду напряжений правее водорода:
Концентрированная
HNO3
Разбавленная HNO3
б) с металлами, стоящими в ряду напряжений левее водорода:
Разбавленная HNO3
б) с металлами, стоящими в ряду напряжений левее водорода:
Слайд 9Взаимодействие с металлами
Единственная общая закономерность при взаимодействии азотной кислоты с металлами:
чем более разбавленная кислота и чем активнее металл, тем глубже восстанавливается азот:
увеличение концентрации кислоты увеличение активности металла
увеличение концентрации кислоты увеличение активности металла
Слайд 10Взаимодействие с металлами
С золотом и платиной азотная кислота, даже концентрированная не
взаимодействует. Железо, алюминий, хром холодной концентрированной азотной кислотой пассивируются. С разбавленной азотной кислотой железо взаимодействует, причем в зависимости от концентрации кислоты образуются не только различные продукты восстановления азота, но и различные продукты окисления железа:
Слайд 12Взаимодействие с неметаллами
Азотная кислота окисляет неметаллы, при этом азот обычно восстанавливается
до NO или NO2:
Слайд 13HNO3 как сильная одноосновная кислота взаимодействует:
а) с основными и амфотерными оксидами:
б)
с основаниями:
в) вытесняет слабые кислоты из их солей:
в) вытесняет слабые кислоты из их солей:
Слайд 14Смесь трех объёмов соляной кислоты и одного объёма азотной называется «царской
водкой».
Царская водка растворяет большинство металлов, в том числе золото и платину.
Царская водка растворяет большинство металлов, в том числе золото и платину.
Слайд 15Применение
в производстве минеральных удобрений;
в военной промышленности (дымящая — в производстве взрывчатых веществ,
как окислитель ракетного топлива, разбавленная — в синтезе различных веществ, в том числе отравляющих);
крайне редко в фотографии — разбавленная — подкисление некоторых тонирующих растворов;
в станковой графике — для травления печатных форм (офортных досок, цинкографических типографских форм и магниевых клише).
в производстве красителей и лекарств (нитроглицерин)
в ювелирном деле — основной способ определения золота в золотом сплаве;
в основном органическом синтезе (нитроалканы, анилин, нитроцеллюлоза, тротил...)
крайне редко в фотографии — разбавленная — подкисление некоторых тонирующих растворов;
в станковой графике — для травления печатных форм (офортных досок, цинкографических типографских форм и магниевых клише).
в производстве красителей и лекарств (нитроглицерин)
в ювелирном деле — основной способ определения золота в золотом сплаве;
в основном органическом синтезе (нитроалканы, анилин, нитроцеллюлоза, тротил...)
Слайд 16Действие на организм
Азотная кислота по степени воздействия на
организм относится к веществам 3-го класса опасности.
Её пары очень вредны: пары вызывают раздражение дыхательных путей, а сама кислота оставляет на коже долгозаживающие язвы.
При действии на кожу возникает характерное жёлтое окрашивание кожи, обусловленное ксантопротеиновой реакцией.
При нагреве или под действием света кислота разлагается с образованием высокотоксичного диоксида азота NO2 (газа бурого цвета).
ПДК для азотной кислоты в воздухе рабочей зоны по NO2 2 мг/м
Её пары очень вредны: пары вызывают раздражение дыхательных путей, а сама кислота оставляет на коже долгозаживающие язвы.
При действии на кожу возникает характерное жёлтое окрашивание кожи, обусловленное ксантопротеиновой реакцией.
При нагреве или под действием света кислота разлагается с образованием высокотоксичного диоксида азота NO2 (газа бурого цвета).
ПДК для азотной кислоты в воздухе рабочей зоны по NO2 2 мг/м