- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 8 класс. Растворы, растворимость
Содержание
- 1. Презентация по химии 8 класс. Растворы, растворимость
- 2. Физическая теория.Сторонники физической теории растворов Вант-Гофф, Оствальд
- 3. Признаки химического взаимодействия при растворенииТепловые явленияИзменение окраскиХимическая
- 4. Опыты1)Растворение серной кислоты в воде сопровождается настолько
- 5. РастворениеФизический процесс –заключающийся в перемешивании молекул растворенного
- 6. Растворение? Современная теория– это
- 7. Растворимость -Способность вещества образовывать с другими веществами
- 8. По растворимости выделяютХорошо растворимые вещества (в 100г
- 9. Классификация растворов по содержанию растворенного веществаНенасыщенный раствор:
- 10. Вода
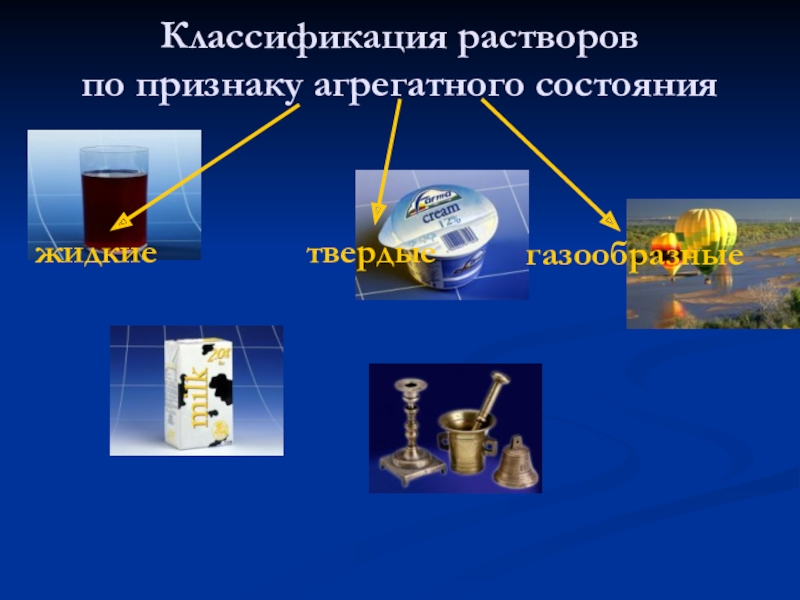
- 11. Классификация растворов по признаку агрегатного состояния
- 12. Растворы и растворениеРАСТВОРЫоднородная устойчивая система, состоящая из
- 13. Применение растворов в промышленности
- 14. Применение растворов в сельском хозяйстве
- 15. Применение растворов в быту и медицине
- 16. Вопросы1)Расскажите физическую теорию о растворе.2)Расскажите химическую теорию
- 17. Уравнения1) Fe2O3 + HCl → FeCl3 +
- 18. Задачи1) Рассчитайте количество вещества спирта C2H6O, который
- 19. Слайд 19
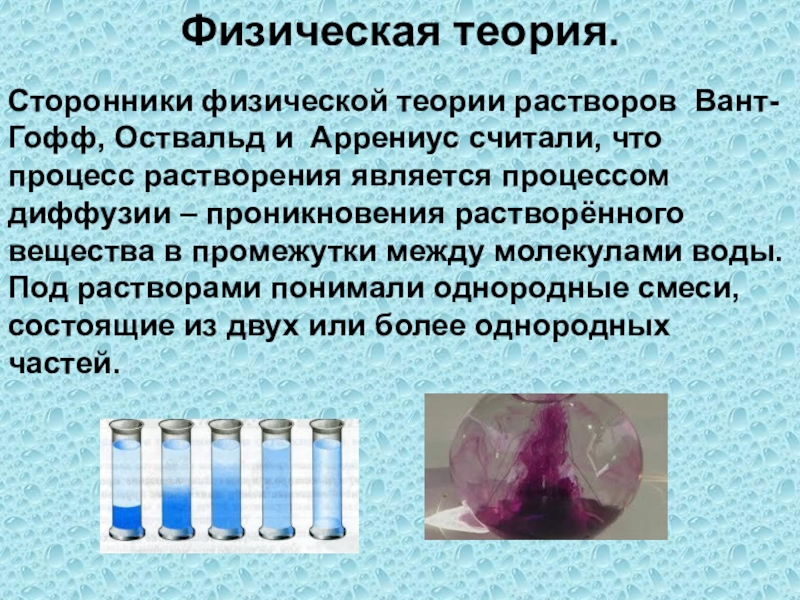
Слайд 2Физическая теория.
Сторонники физической теории растворов Вант-Гофф, Оствальд и Аррениус считали, что
Слайд 3Признаки химического взаимодействия при растворении
Тепловые явления
Изменение окраски
Химическая теория.
Менделеев, Каблуков и Кистяковский
Гидраты – это соединения, которые образуются в результате химического взаимодействия растворённого вещества с молекулами воды.
Кристаллогидраты – соли, в состав которых входит вода. В этом случае её называют кристаллизационной. Например, к кристаллогидратам относится хорошо известная всем соль голубого цвета – медный купорос. Безводный сульфат меди (II) – кристаллы белого цвета.
Слайд 4Опыты
1)Растворение серной кислоты в воде сопровождается настолько сильным выделением теплоты, что
2)Растворение хлорида натрия и нитрата аммония сопровождается выделением теплоты.
3)М. В. Ломоносов установил, что растворы замерзают при более низкой температуре, чем растворитель .
Слайд 5Растворение
Физический процесс –заключающийся в перемешивании молекул растворенного вещества и растворителя, результат
Химический процесс –заключающийся во взаимодействии молекул растворенного вещества и растворителя, а также образования гидратов.
Слайд 6Растворение?
Современная теория
– это физико-химический процесс, включающий в себя
Слайд 7Растворимость -
Способность вещества образовывать с другими веществами (растворителями) однородные системы –
- величина, которая показывает максимальную массу растворённого вещества в 100г воды
Слайд 8По растворимости выделяют
Хорошо растворимые вещества (в 100г воды растворяется > 1г
Малорастворимые (в 100г воды растворяется < 1г вещества)
Нерастворимые (в 100г воды растворяется < 0,01г вещества).
Слайд 9Классификация растворов по содержанию растворенного вещества
Ненасыщенный раствор: при данной температуре находится
Насыщенный раствор: при данной температуре вещество больше не растворяется
Пересыщенный раствор: в растворенном состоянии больше вещества, чем его в насыщенном растворе
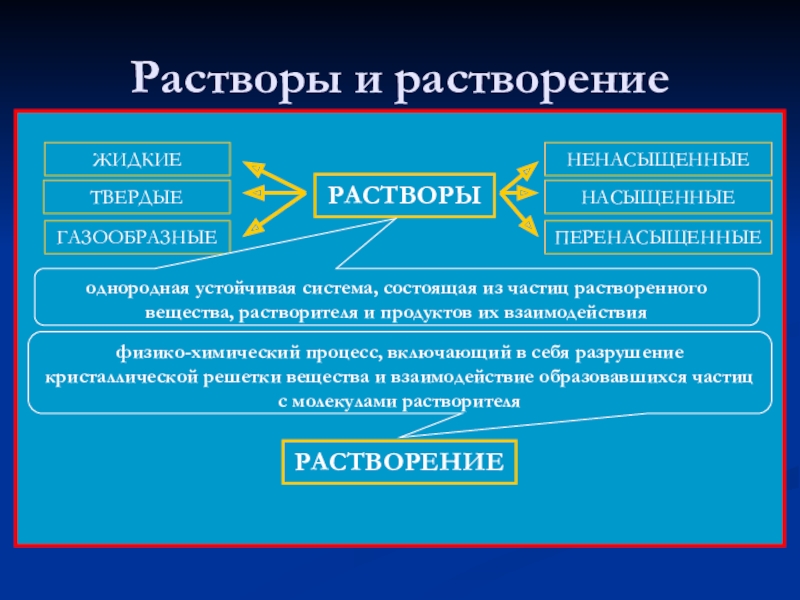
Слайд 12Растворы и растворение
РАСТВОРЫ
однородная устойчивая система, состоящая из частиц растворенного вещества, растворителя
РАСТВОРЕНИЕ
физико-химический процесс, включающий в себя разрушение кристаллической решетки вещества и взаимодействие образовавшихся частиц с молекулами растворителя
Слайд 16Вопросы
1)Расскажите физическую теорию о растворе.
2)Расскажите химическую теорию о растворе.
3)Что такое раствор?
4)Гидраты
5)Что такое растворимость и что она показывает?
6)Дайте характеристику растворам.
7)Что такое кристаллогидраты?
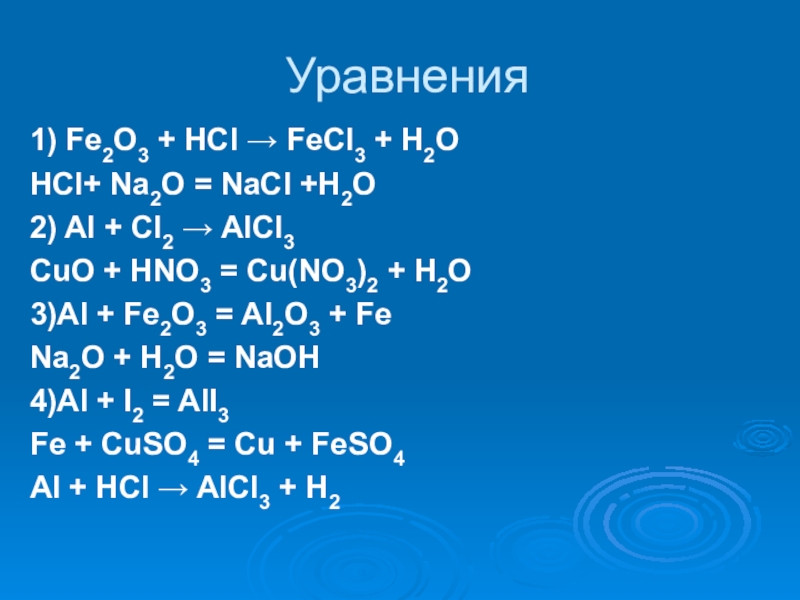
Слайд 17Уравнения
1) Fe2O3 + HCl → FeCl3 + H2O
HCl+ Na2O =
2) Al + Cl2 → AlCl3
CuO + HNO3 = Cu(NO3)2 + H2O
3)Al + Fe2O3 = Al2O3 + Fe
Na2O + H2O = NaOH
4)Al + I2 = AlI3
Fe + CuSO4 = Cu + FeSO4
Al + HCl → AlCl3 + H2
Слайд 18Задачи
1) Рассчитайте количество вещества спирта C2H6O, который содержится в 500 г
2) Для борьбы с болезнями растений, особенно плодовых деревьев и виноградников, применяют раствор сульфата меди(II). Обычно растворяют 100 г соли на ведро воды (8л). Какова массовая доля соли в полученном растворе? Сколько воды и соли содержится в 500 г этого раствора?
3) Найдите массу азота, полученного из 280 л воздуха (н. у.), если известно, что объёмная доля азота в воздухе составляет 78%.
4) Из 150 г воды растворили 50 г фосфорной кислоты. Найдите массовую долю кислоты в полученном растворе.