- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 8 класс по теме Кислоты
Содержание
- 1. Презентация по химии 8 класс по теме Кислоты
- 2. Вопрос 3.Перед вами ряд формул неорганических соединений: H2SO4,
- 3. Проверьте свою работу:3. Остались формулы:H2SO4, HNO3, HCl,
- 4. «Просто знать – еще не все, знания нужно уметь использовать»
- 5. Филиал МБОУ СОШ с. Каменка в селе ЕловаткаУрок на тему «Кислоты»Учитель биологии, химии Васильева Л.Н.
- 6. Цели:1. Рассмотреть понятие о кислотах;2. Познакомить учащихся
- 7. На уроке нам потребуется: кристаллические лимонная и
- 8. Пример: кислый → кислота
- 9. HCI соляная HNO3
- 10. Состав кислот HCl
- 11. 1 уровень. Перепишите формулы кислот: HCL, H2SO4,
- 12. НСl
- 13. По числу атомов водорода(по основности).HCI, HNO3H3PO4, H3BO3H2S, H2SO4, H2SiO3ОдноосновныеДвухосновныеТрехосновные
- 14. Нахождение кислот в природе (органические)ЛимоннаяМолочнаяЯблочнаяЩавелеваяИботеновая
- 15. Классификация кислотПо нахождению в природе 2. По
- 16. Физические свойства.HCI, H2SO4, HNO3 - жидкостиВсе кислоты,
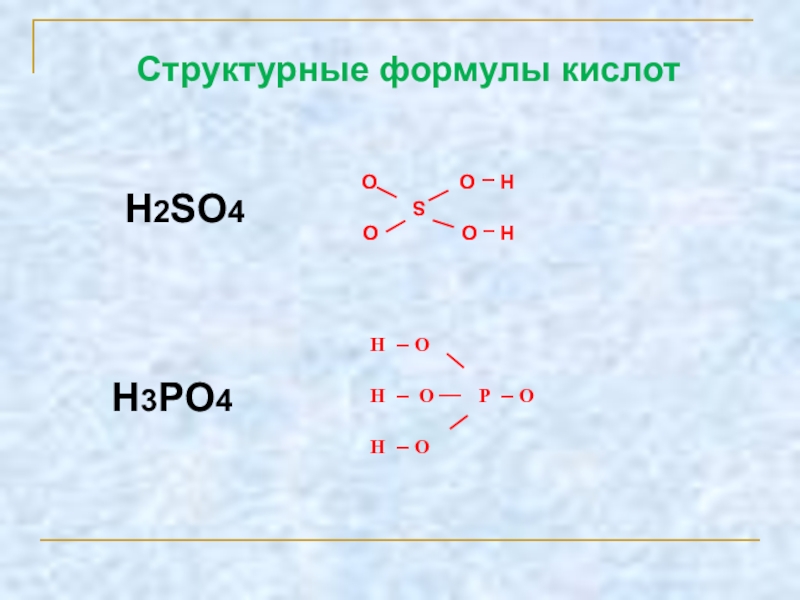
- 17. H – O H – O
- 18. Действие кислот на индикаторыКислота - КрасныйКак запомнить изменение окраски и не спутать кислую и щелочную среду?
- 19. Важнейшие кислоты.По объёмам производства серной кислоты судят
- 20. Другой важнейшей кислотой является соляная кислота. Она
- 21. 3. На все возникшие вопросы я получил
- 22. 5. Задание на дом:§ 32, стр. 100-102
- 23. Гниение листьевIПолучение пластмассОкраска листьевПроизводство красителейЗамерзание водыCl
Слайд 1Ответьте на вопросы
1. Назовите следующие вещества: СО2; СаО; NaOH; KOH (3
2. Напишите уравнения реакций с помощью которых можно осуществить превращения
Ca CaO Ca(OH)2 (4 балла)
3.Рассчитайте массу и объем углекислого газа СО2 количеством вещества 4,4 моль. (5 баллов)
Слайд 2Вопрос 3.
Перед вами ряд формул неорганических соединений:
H2SO4, K2O, Ca(OH)2, NaOH, HCI,
1. Выпишите формулы оксидов
2. Выпишите формулы оснований
3.Какие формулы остались не выписанные?
Слайд 3Проверьте свою работу:
3. Остались формулы:
H2SO4, HNO3, HCl, HF, HCI,
K2O, AI2O3, Na2O,
1. Формулы оксидов:
Ca(OH)2, NaOH, Cu(OH)2
2. Формулы оснований:
Слайд 5Филиал МБОУ СОШ с. Каменка в селе Еловатка
Урок на тему «Кислоты»
Учитель
Слайд 6Цели:
1. Рассмотреть понятие о кислотах;
2. Познакомить учащихся с важнейшими неорганическими кислотами;
3.
4. Развивать умение обобщать факты, строить аналогии и делать выводы;
5. Развивать способность учащихся к химическому прогнозированию;
6.Способствовать развитию интереса к химии, умений применять новый материал на практике и в жизни;
7. Продолжить воспитание навыков самостоятельной работы.
Слайд 7На уроке нам потребуется: кристаллические лимонная и аскорбиновая кислоты, HCI,
химическая посуда: стаканы, пробирки.
Слайд 8
Пример: кислый → кислота (эти слова имеют один
Запомните!
Кислоты пробовать на вкус нельзя. Это смертельно опасно.
Кислоты разрушают живые ткани и вызывают ожоги.
Поэтому надо быть очень осторожными и никогда не пробовать на вкус те веществ, которые вам не известны
Слайд 9HCI соляная
HNO3 азотная
H2SO4 серная
H2SO3
H2S сероводородная
H3PO4 ортофосфорная
H2CO3 угольная
H2SiO3 кремниевая
HBr бромная
Что общего у всех этих веществ?
Вся остальная часть называется
кислотным остатком.
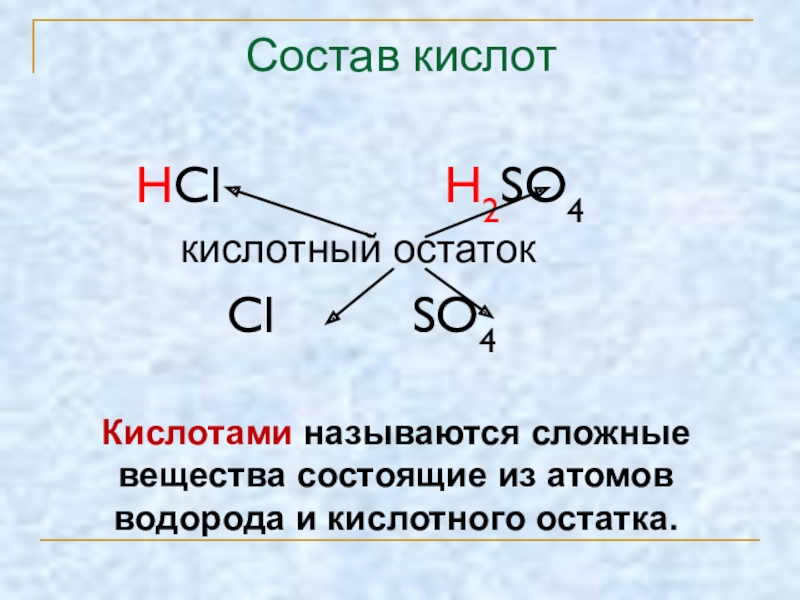
Слайд 10Состав кислот
HCl H2SO4
Cl SO4
Кислотами называются сложные вещества состоящие из атомов водорода и кислотного остатка.
Слайд 111 уровень. Перепишите формулы кислот: HCL, H2SO4, H3PO4. Назовите кислоты.
2 уровень. Перепишите формулы кислот: H2S, HNO3, H2CO3, HBr. Назовите кислоты. В формулах подчеркните кислотные остатки и определите их валентность
3 уровень. Перепишите формулы кислот: HNO2, H2SO3, HI, H2SiO3. Назовите кислоты. В формулах подчеркните кислотные остатки и определите их валентность
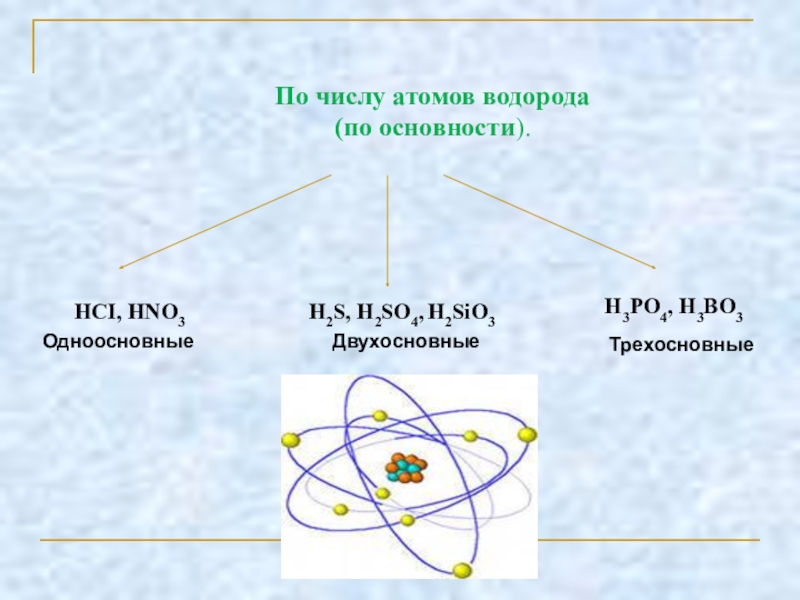
Слайд 13По числу атомов водорода
(по основности).
HCI, HNO3
H3PO4, H3BO3
H2S, H2SO4, H2SiO3
Одноосновные
Двухосновные
Трехосновные
Слайд 15Классификация кислот
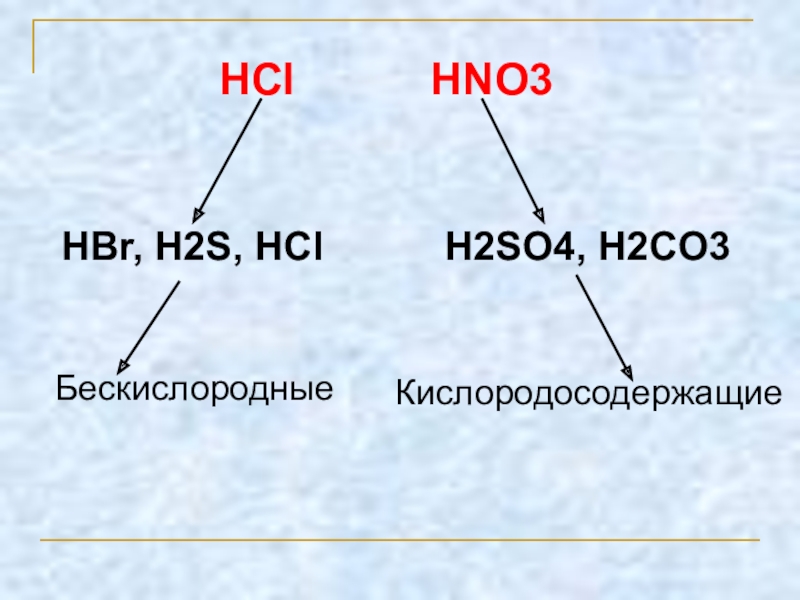
По нахождению в природе
2. По наличию кислорода в кислотном
3. По основности кислотного остатка
4. По растворимости в воде
Слайд 16Физические свойства.
HCI, H2SO4, HNO3 - жидкости
Все кислоты, кроме кремниевой, растворимы в
H3PO4, HBO3 – твёрдые вещества
Угольная и сернистые кислоты в свободном виде не существуют
H2CO3 = CO2 + H2O H2SO3 = SO2 + H2O
Слайд 18
Действие кислот на индикаторы
Кислота - Красный
Как запомнить изменение окраски
и не
Слайд 19Важнейшие кислоты.
По объёмам производства серной кислоты судят о развитии химической промышленности,
Необходимо знать правила безопасности при работе с серной кислотой: При проведении опытов в пробирки сначала наливают воду, а за тем при постоянном помешивании добавляют серную кислоту тонкой струйкой.
Сначала вода,
Потом кислота,
Иначе случится беда.
Запомните!
Слайд 20Другой важнейшей кислотой является соляная кислота.
Она входит в состав желудочного
Соляная кислота дезинфицирует большую часть микробов попадающих в организм с пищей и способствует перевариванию пищи.
Наглядным примером является жевание жвачной резинки на голодный желудок, вследствие чего выделяется желудочный сок содержащий соляную кислоту, которая в свою очередь разъедает стенки желудка и вызывает различные желудочно- кишечные заболевания.
Н CL
Слайд 213. На все возникшие вопросы я получил ответы
Ответьте на следующие
2. Почему они имеют такое название?
1. С каким классом неорганической химии вы сегодня познакомились?
3. Как можно определить кислоту не зная что находится в пробирке?
Рефлексивный тест
1. Я узнал много нового
2. Мне это пригодится в жизни
4.На уроке поработал добросовестно
Слайд 225. Задание на дом:
§ 32, стр. 100-102 упражнение № 1, 2
стр. 104.
В домашних условиях исследуйте действие раствора лимонной кислоты на лист любого комнатного растения. Напишите мини-отчет и сделайте выводы.