- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 8 класс на тему Растворение. Растворы.
Содержание
- 1. Презентация по химии 8 класс на тему Растворение. Растворы.
- 2. Цель урока:Познакомиться с растворением как физико-химическим процессом
- 3. Растворами называют гомогенную систему, состоящую из двух
- 4. Теории растворов.
- 5. Физическая теория.Основоположники теории: Вант Гофф, Оствальд, Аррениус.Растворение– процесс диффузии.Растворы– однородные смеси.Сванте Аррениус
- 6. Химическая теория.Основоположники: Менделеев, Каблуков, Кистяковский.Растворение – это
- 7. Современная теория.Растворение – это физико-химический процесс.Растворы –
- 8. РастворениеФизический процесс –результат диффузии веществХимический процесс –взаимодействие
- 9. ГидратыНе постоянный состав (в кристаллогидратах)Медный купорос –
- 10. Признаки химического взаимодействия при растворении.
- 11. 1. Тепловые явленияэндотермические2. Изменение цветаБелые кристаллы CuSO4
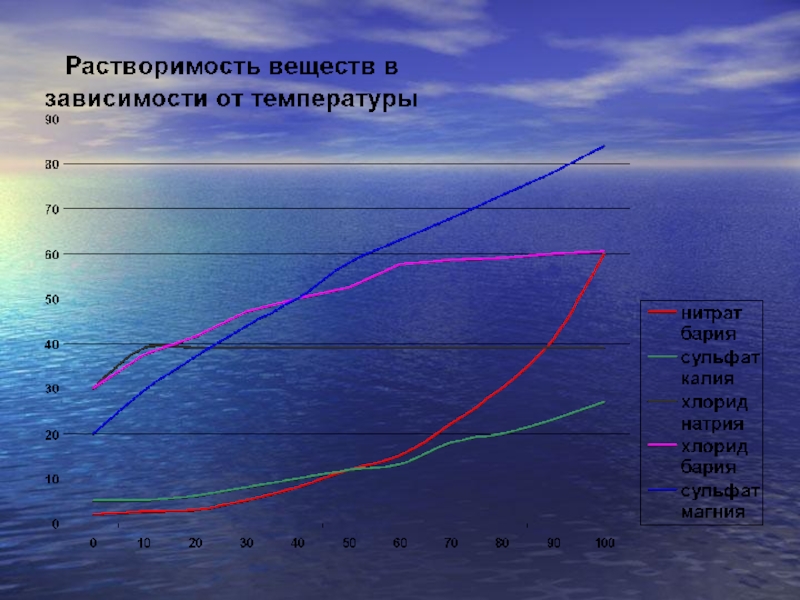
- 12. Растворимость - ?От чего зависит растворимость веществ?
- 13. Факторы влияющие на растворимость веществ1. Природа растворенного вещества2. Природа растворителя3. Температура4. Масса растворенного вещества
- 14. Природа растворенного веществаВеществахорошо растворимые (в 100г H2O
- 15. Зависимость растворимости веществ от природы растворителяРастворение медного купороса в водеРастворение медного купороса в спиртеСпиртовой раствор йода
- 16. Слайд 16
- 17. Классификация растворов по признаку растворимостиНенасыщенный раствор: при
- 18. Типы растворов по содержанию растворенного веществаНенасыщенные –
- 19. Ответьте на вопросы :1. От чего не
- 20. Применение растворов в промышленности
- 21. Применение растворов в сельском хозяйстве
- 22. Применение растворов в быту и медицине
Слайд 2Цель урока:
Познакомиться с растворением как физико-химическим процессом и растворами как физико-химическими
Выявить зависимость растворимости твердых веществ от температуры.
Рассмотреть классификацию растворов по признаку растворимости.
Слайд 3Растворами называют гомогенную систему, состоящую из двух или большего числа составных
Главный признак растворов- непрерывное изменение состава при сохранении однородности
К растворам относят:
гомогенные смеси
соединения переменного состава
Компоненты раствора
Растворитель
растворенное
вещество
Важная особенность – простыми физическими приемами можно выделить чистые исходные компоненты.
Слайд 5Физическая теория.
Основоположники теории: Вант Гофф, Оствальд, Аррениус.
Растворение– процесс диффузии.
Растворы– однородные смеси.
Сванте
Слайд 6Химическая теория.
Основоположники: Менделеев, Каблуков, Кистяковский.
Растворение – это процесс химического взаимодействия растворяемого
Растворы – это соединения-гидраты.
Иван Алексеевич Каблуков
Слайд 7Современная теория.
Растворение – это физико-химический процесс.
Растворы – это однородные (гомогенные) системы,
Слайд 8Растворение
Физический процесс –
результат диффузии веществ
Химический процесс –взаимодействие вещества с водой и
Состав раствора
Растворенное вещество
Растворитель
Гидраты растворенных веществ
Слайд 9Гидраты
Не постоянный состав (в кристаллогидратах)
Медный купорос – CuSO4 · 5H2O
Глауберова соль
Постоянный состав
(в растворах)
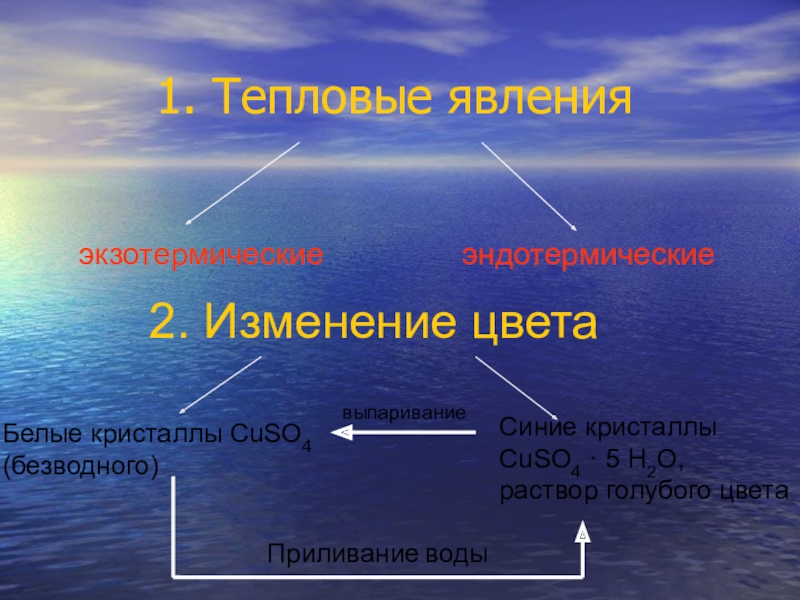
Слайд 111. Тепловые явления
эндотермические
2. Изменение цвета
Белые кристаллы CuSO4
(безводного)
Синие кристаллы
CuSO4 ·
раствор голубого цвета
Приливание воды
выпаривание
экзотермические
Слайд 13Факторы влияющие на растворимость веществ
1. Природа растворенного вещества
2. Природа растворителя
3. Температура
4.
Слайд 14Природа растворенного вещества
Вещества
хорошо растворимые (в 100г H2O
нерастворимые (в 100г H2O меньше 0,01г вещества)
малорастворимые (в 100г H2O меньше 1г вещества)
РАСТВОРИМОСТЬ НЕКОТОРЫХ СОЛЕЙ В 100 г ВОДЫ ПРИ 20 °С
Карбонат кальция CaCO3
Гидроксид кальция Ca(OH)2
Хлорид кальция CaCl2
Слайд 15Зависимость растворимости веществ от природы растворителя
Растворение медного купороса в воде
Растворение медного
Спиртовой раствор йода
Слайд 17Классификация растворов по признаку растворимости
Ненасыщенный раствор: при данной температуре находится меньше
Насыщенный раствор: при данной температуре вещество больше не растворяется
Пересыщенный раствор: в растворенном состоянии больше вещества, чем его в насыщенном растворе
Слайд 18Типы растворов по содержанию растворенного вещества
Ненасыщенные – если содержание в растворе
Насыщенный – такой раствор, в котором содержание растворенного вещества отвечает установлению при данной температуре равновесия между этим веществом и раствором.
Перенасыщенный – такой раствор , где содержание вещества больше, чем насыщенном растворе.
Слайд 19Ответьте на вопросы :
1. От чего не зависит растворимость твердых веществ?
А)
2. Как меняется растворимость гидроксида кальция в воде при понижении температуры?
А) понижается Б) остается постоянной В) увеличивается Г) не знаю
3. Какое из веществ является практически нерастворимым?
А) нитрат серебра Б) сульфат бария В) гидроксид кальция Г) не знаю
4. К 100мл H2O добавили 10г карбоната кальция. Какова массовая доля вещества в полученном растворе?
А) 10% Б) 9,1% В) 5% Г) 0%