- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 10 класс Электронные эффекты
Содержание
- 1. Презентация по химии 10 класс Электронные эффекты
- 2. Слайд 2
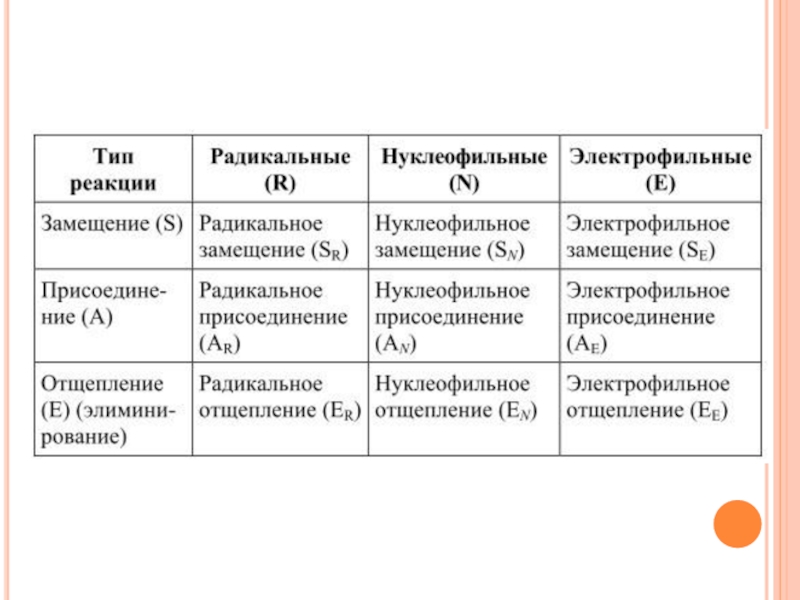
- 3. Слайд 3
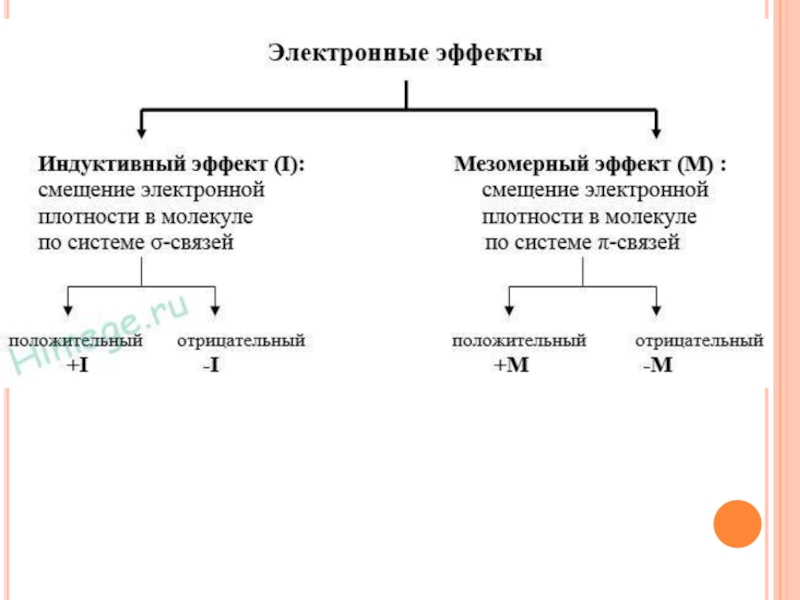
- 4. Электронные эффекты - смещение электронной плотности в
- 5. Индуктивный эффект (I-эффект)Индуктивный эффект — смещение электронной
- 6. Слайд 6
- 7. Из-за слабой поляризуемости σ-связей I-эффект быстрозатухает
- 8. Индуктивный эффект называют отрицательным (–I),если заместитель уменьшает электронную плотность
- 9. Отрицательный индуктивный эффект проявляют элементы, более электроотрицательные,
- 10. –I-эффект проявляют заместители, которые содержат более электроотрицательные атомы,
- 11. В случае заместителей с полным зарядом отрицательный
- 12. sp3 < sp2 < sp В
- 13. Индуктивный эффект называется положительным (+I), если заместитель увеличивает электронную плотность
- 14. (СН3)3С- > (CH3)2CH- > CH3-CH2- > CH3-
- 15. Слайд 15
- 16. Слайд 16
- 17. Индуктивный эффект проявляется всегда при наличии в
- 18. Мезомерный эффект (М- эффект) или эффект сопряжнияСмещение
- 19. Слайд 19
- 20. Слайд 20
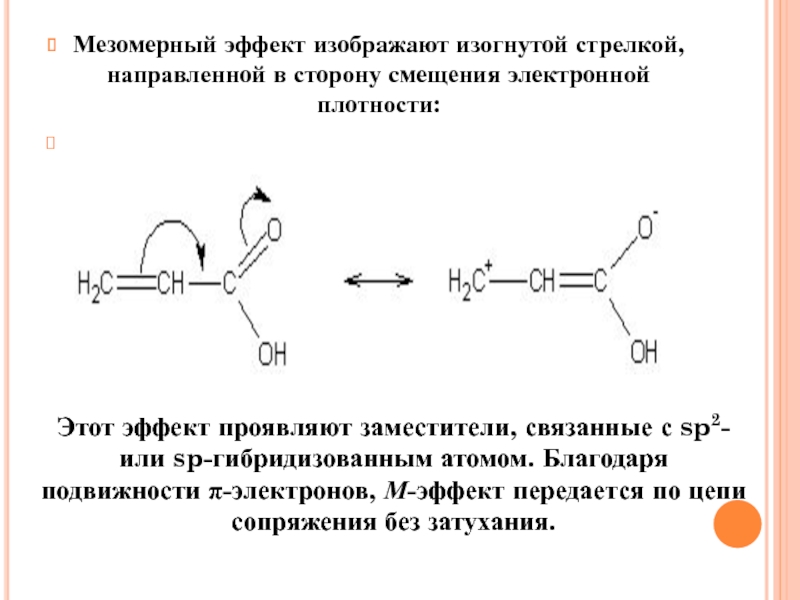
- 21. Мезомерный эффект изображают изогнутой стрелкой, направленной в
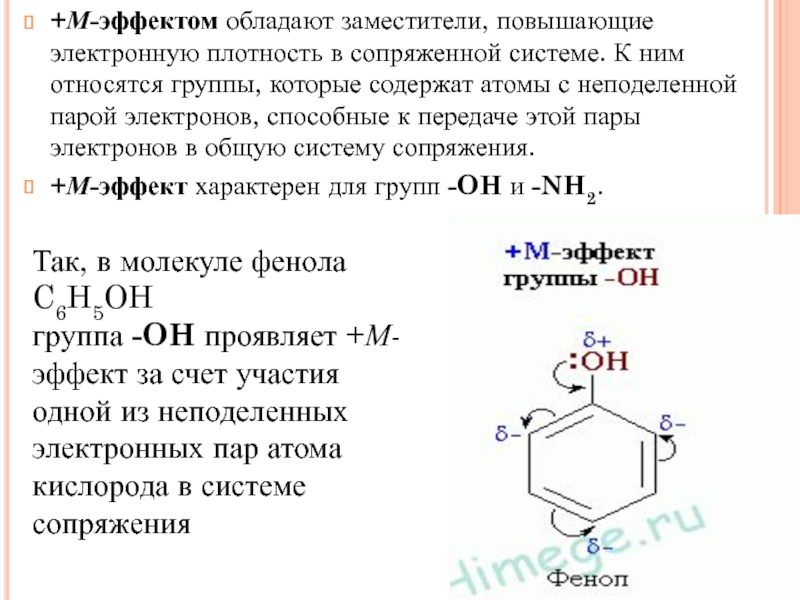
- 22. +М-эффектом обладают заместители, повышающие электронную плотность в сопряженной
- 23. Слайд 23
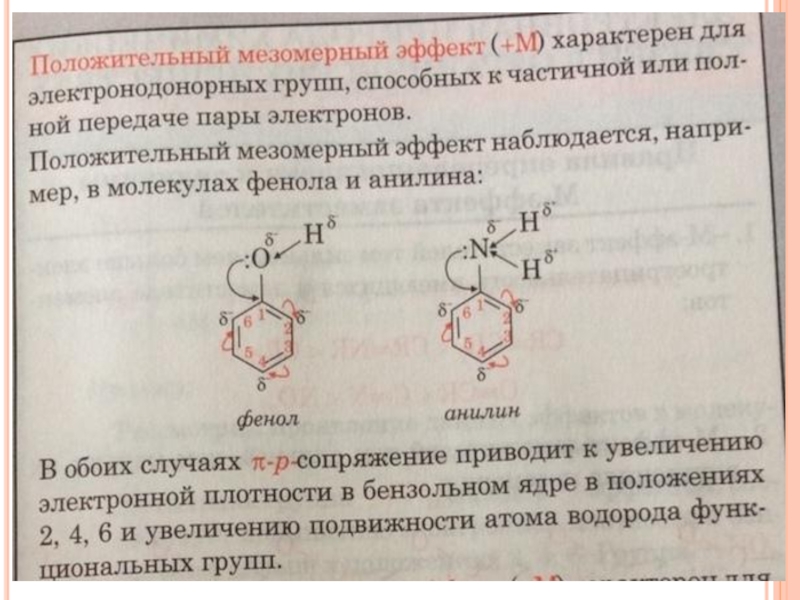
- 24. Положительный мезомерный эффект (+М) уменьшается при увеличении
- 25. Положительным мезомерным эффектом обладают группировки с неподеленными
- 26. Положительный мезомерный эффект уменьшается в том случае, если атом связан с группой-акцептором электронов: -NH2 > -NH-CO-CH3
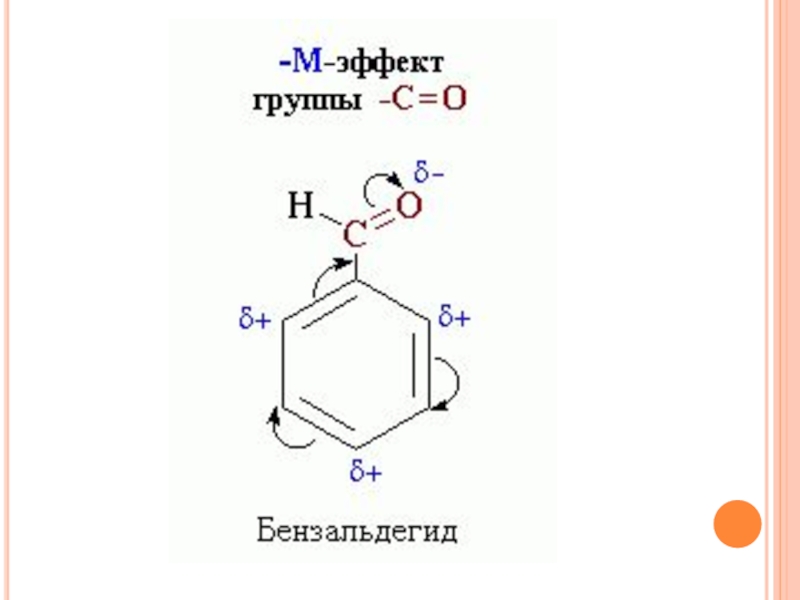
- 27. –М-эффект проявляют заместители с электроотрицательными атомами и смещающие
- 28. Слайд 28
- 29. Слайд 29
- 30. Отрицательный мезомерный эффект возрастает с увеличением электроотрицательности
- 31. Уменьшение отрицательного мезомерного эффекта наблюдается в случае, если группа- акцептор сопряжена с донорной группой: -CO-O-
- 32. Слайд 32
- 33. Слайд 33
- 34. Слайд 34
- 35. Слайд 35
- 36. Слайд 36
- 37. Слайд 37
- 38. Заместители А, вызывающие отрицательный мезомерный эффект:-NO2, -CN, -COOH,
- 39. Слайд 39
Слайд 4Электронные эффекты - смещение электронной плотности в молекуле, ионе или радикале
Заместителем считается любой атом (кроме водорода) или группа атомов, связанные с атомом углерода.
Слайд 5Индуктивный эффект (I-эффект)
Индуктивный эффект — смещение электронной плотности по цепи σ-связей,
Изображается стрелкой в направлении смещения электронной плотности.
Направление (знак) I-эффекта заместителя качественно оценивается путем сравнения со стандартом — атомом водорода, индуктивный эффект которого принят за 0.
Слайд 7
Из-за слабой поляризуемости σ-связей I-эффект быстро
затухает с удалением от заместителя
Слайд 8Индуктивный эффект называют отрицательным (–I),
если заместитель уменьшает электронную плотность на атоме углерода, с
Слайд 9Отрицательный индуктивный эффект проявляют элементы, более электроотрицательные, чем углерод, т.е. галогены,
F > O > N,
F > Cl > Br > I
Слайд 10–I-эффект проявляют заместители, которые содержат более электроотрицательные атомы, чем атом углерода:
-F, -Cl,
Заместители А, вызывающие отрицательный индуктивный эффект, являются
электроноакцепторами: -NO2, -CN, -COOH, -F, — Cl, -Br, -I, -COOR, -COR, -OR, -OH, -NH2, -Ar
Слайд 11В случае заместителей с полным зарядом отрицательный индуктивный эффект увеличивается с
>O+- >> N+<
Слайд 12sp3 < sp2 < sp
В случае сложных заместителей отрицательный индуктивный эффект
Слайд 13Индуктивный эффект называется положительным (+I),
если заместитель увеличивает электронную плотность на атоме углерода, индуцируя
Слайд 14(СН3)3С- > (CH3)2CH- > CH3-CH2- > CH3- > H-
Положительный индуктивный эффект
Заместители B, вызывающие положительный индуктивный эффект, являются электронодонорами: — CR3, -CHR2, -CH2R, -CH3
Слайд 17Индуктивный эффект проявляется всегда при наличии в молекуле атомов с различной
Индуктивный эффект распространяется только через σ-связи и всегда в одном направлении.
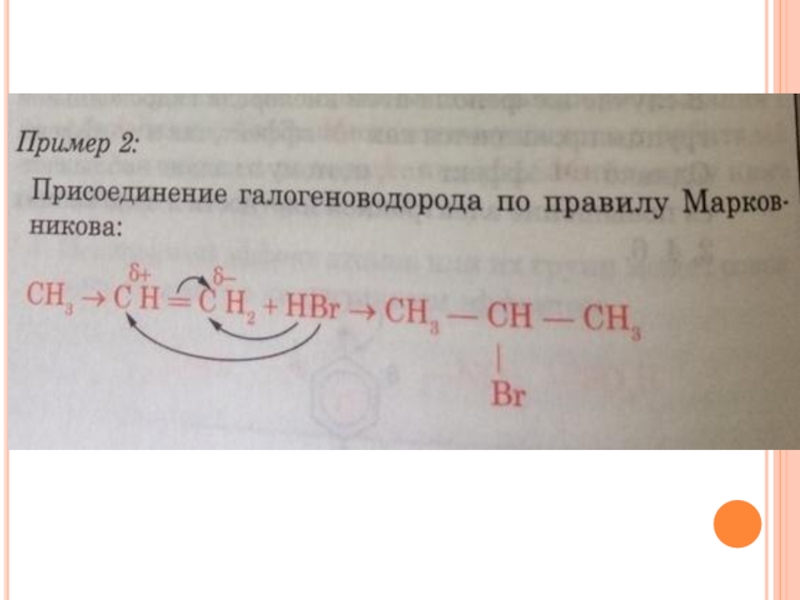
Индуктивный эффект затухает в цепи через 3 – 4 σ-связи.Пример влияния индуктивного эффекта на направление химической реакции — присоединение галогенводородов к алкенам по правилу Марковникова и против правила Марковникова.
Слайд 18Мезомерный эффект (М- эффект) или эффект сопряжния
Смещение электронной плотности по цепи
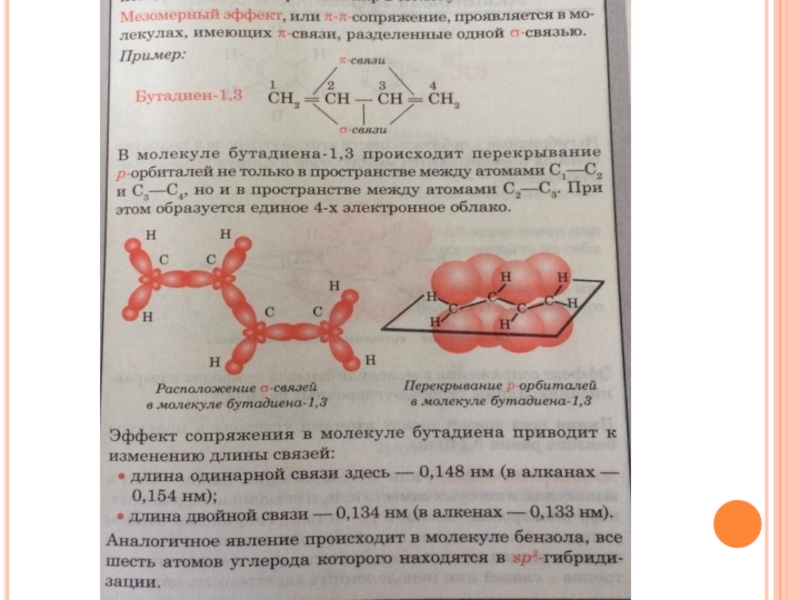
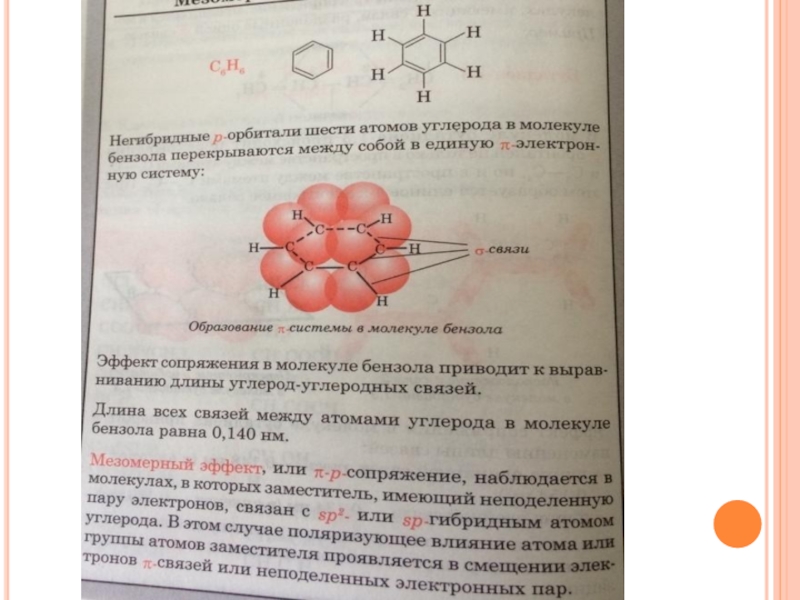
Сопряженная система состоит из чередующихся простых и кратных связей. В сопряжение также может вступать атом с неподеленной парой р-электронов или атом с вакантной р-орбиталью.
Мезомерный эффект проявляется лишь в том случае, когда заместитель включен в сопряженную систему молекулы.
Слайд 21Мезомерный эффект изображают изогнутой стрелкой, направленной в сторону смещения электронной плотности:
Этот
Слайд 22+М-эффектом обладают заместители, повышающие электронную плотность в сопряженной системе. К ним относятся
+М-эффект характерен для групп -OH и -NH2.
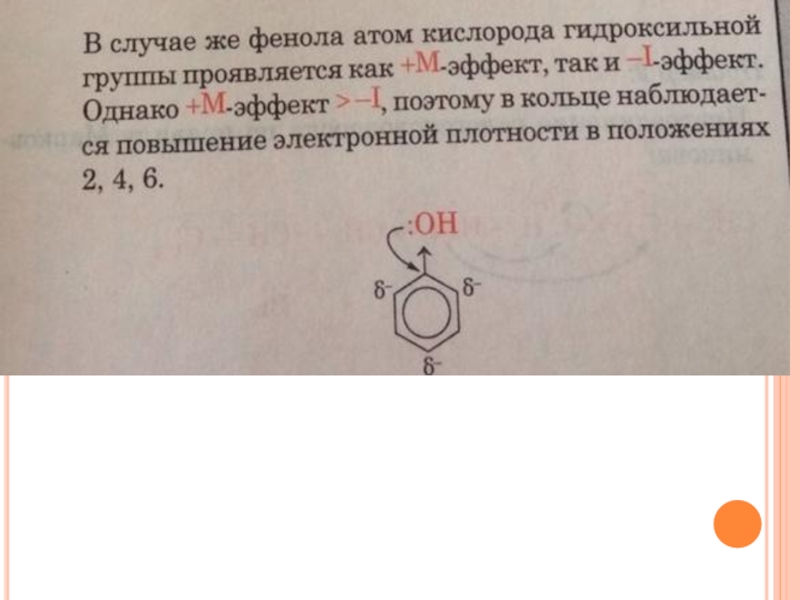
Так, в молекуле фенола C6H5OH группа -OH проявляет +М-эффект за счет участия одной из неподеленных электронных пар атома кислорода в системе сопряжения
Слайд 24Положительный мезомерный эффект (+М) уменьшается при увеличении электроотрицательности атома, несущего неподеленную
F > Cl > Br > I (+M-эффект)
Слайд 25Положительным мезомерным эффектом обладают группировки с неподеленными парами электронов на атоме,
-NH2 (NHR, NR2) > OH (OR) > X (галоген) (+М-эффект)
Слайд 26Положительный мезомерный эффект уменьшается в том случае, если атом связан с
-NH2 > -NH-CO-CH3
Слайд 27–М-эффект проявляют заместители с электроотрицательными атомами и смещающие электронную плотность на себя.
Слайд 30Отрицательный мезомерный эффект возрастает с увеличением электроотрицательности атома и достигает максимальных
>C=O+H >> >C=O
Слайд 31Уменьшение отрицательного мезомерного эффекта наблюдается в случае, если группа- акцептор сопряжена
-CO-O- << -СО-NH2 < -CO-OR < -CO-H(R) << -CO-CO- < -CO-X (галоген) (–М-эффект).
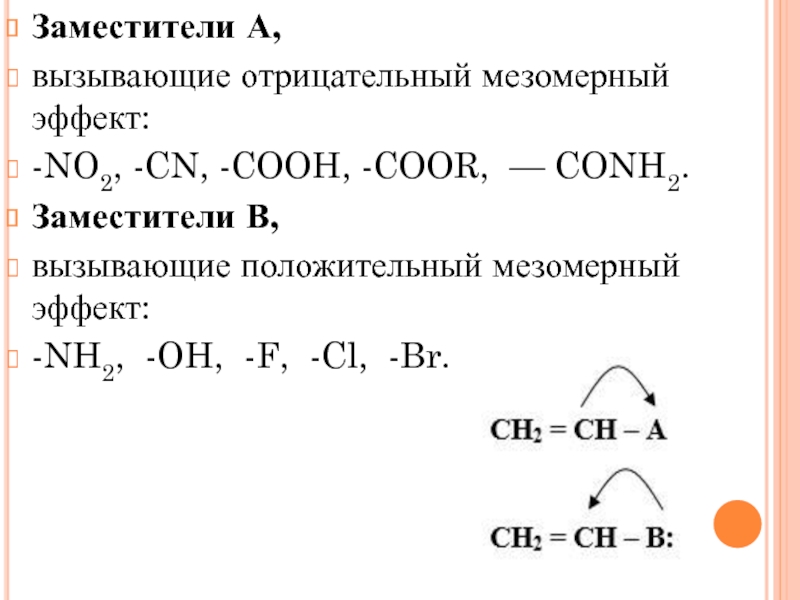
Слайд 38Заместители А,
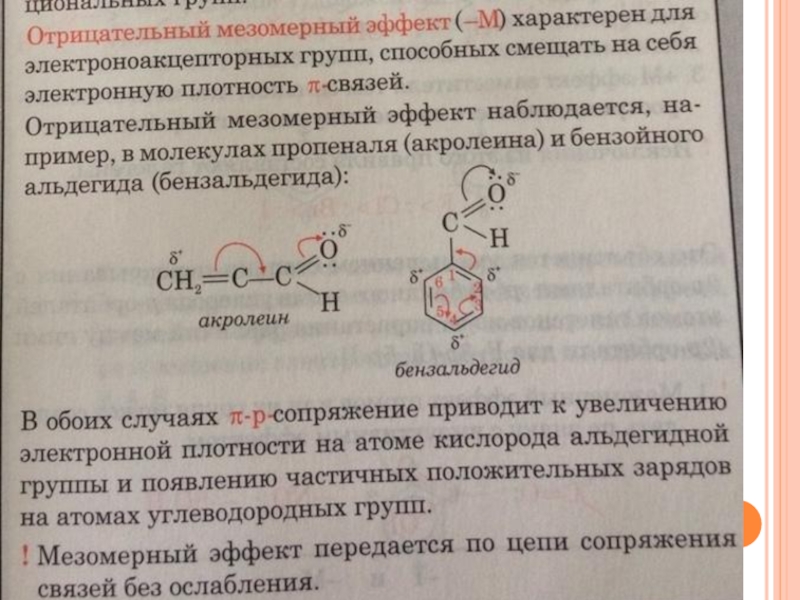
вызывающие отрицательный мезомерный эффект:
-NO2, -CN, -COOH, -COOR, — CONH2.
Заместители В,
вызывающие
-NH2, -OH, -F, -Cl, -Br.