- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
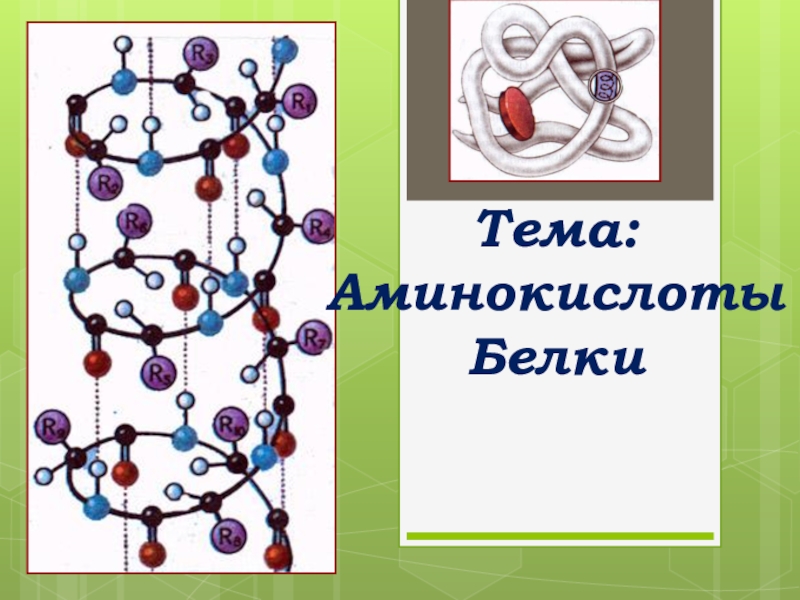
Презентация, доклад лекции по химии: Аминокислоты и белки
Содержание
- 1. Презентация лекции по химии: Аминокислоты и белки
- 2. ХИМИЯ
- 3. Рождение химии белка… Впервые белок был
- 4. Жерар Мульдер"Во всех растениях и животных
- 5. Белки, или протеины что происходит от греч. protos — первый,
- 6. Проблемный вопрос:Можно ли утверждать что: «Нет белка
- 7. Содержание учебного материала:Аминокислоты: строение молекулы, номенклатура и
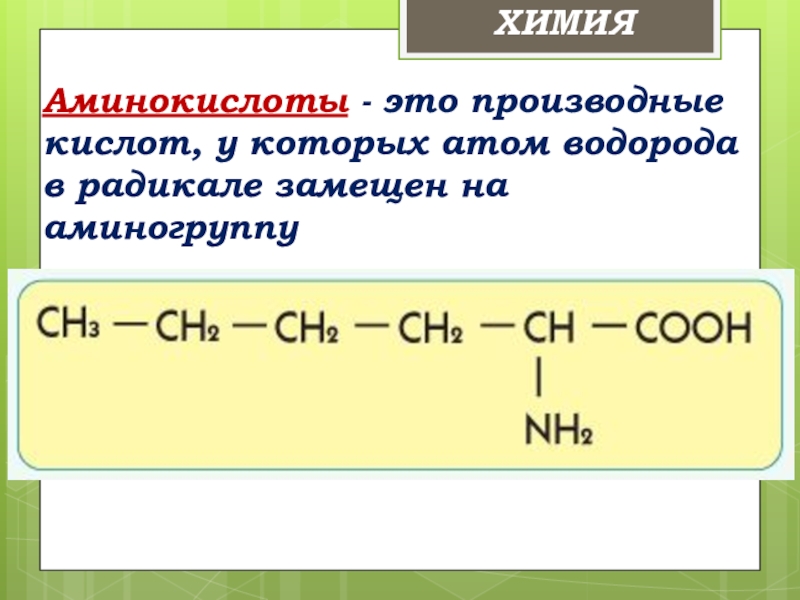
- 8. Аминокислоты - это производные кислот, у
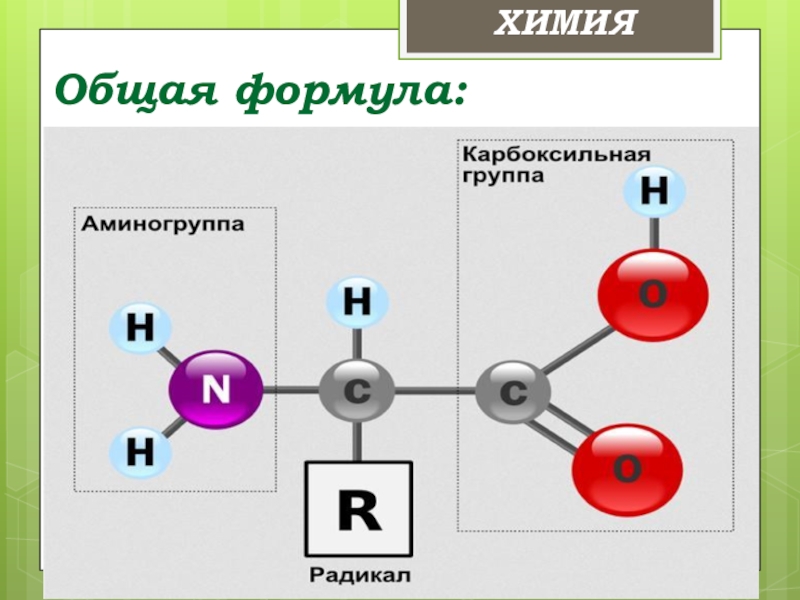
- 9. Общая формула:ХИМИЯ
- 10. Слайд 10
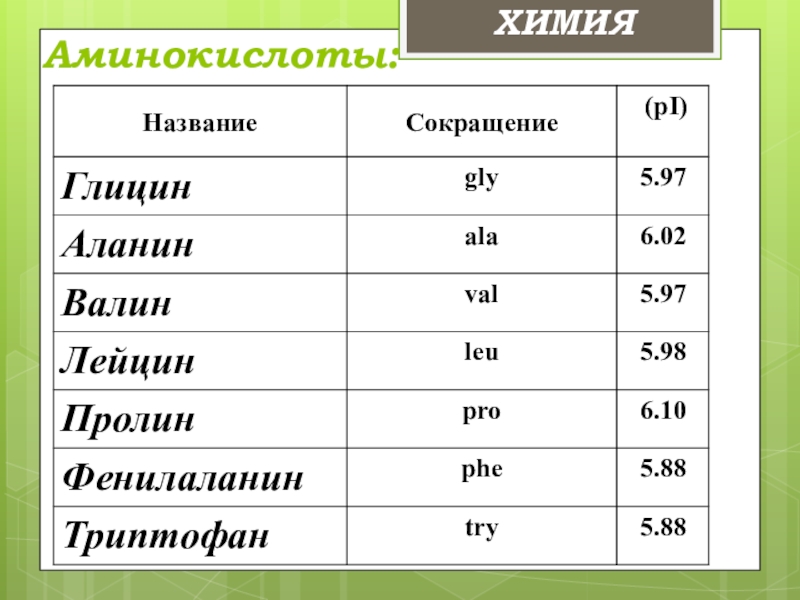
- 11. Аминокислоты: ХИМИЯ
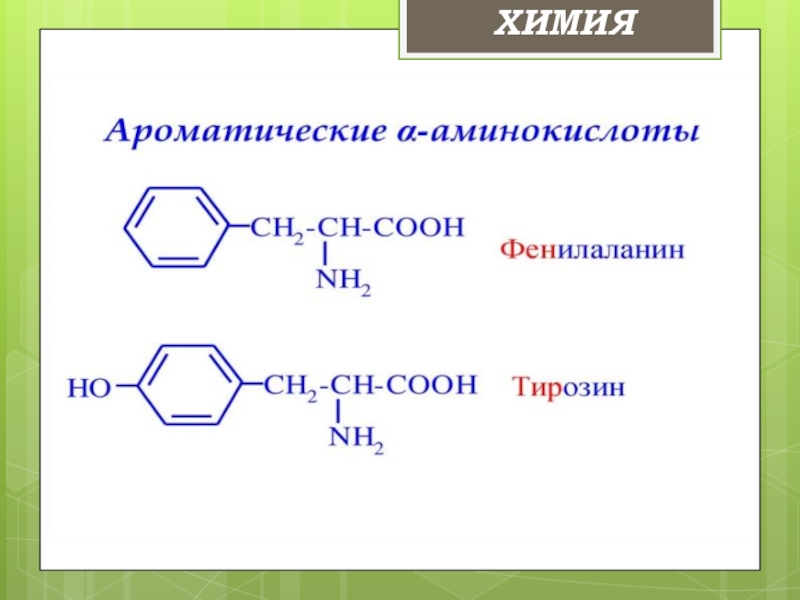
- 12. Классификация аминокислот: 1.По природе радикала : ХИМИЯ
- 13. ХИМИЯ
- 14. 2. По взаимному расположению функциональных групп выделяют α-, ß-, γ- и т.д. аминокислоты. ХИМИЯ
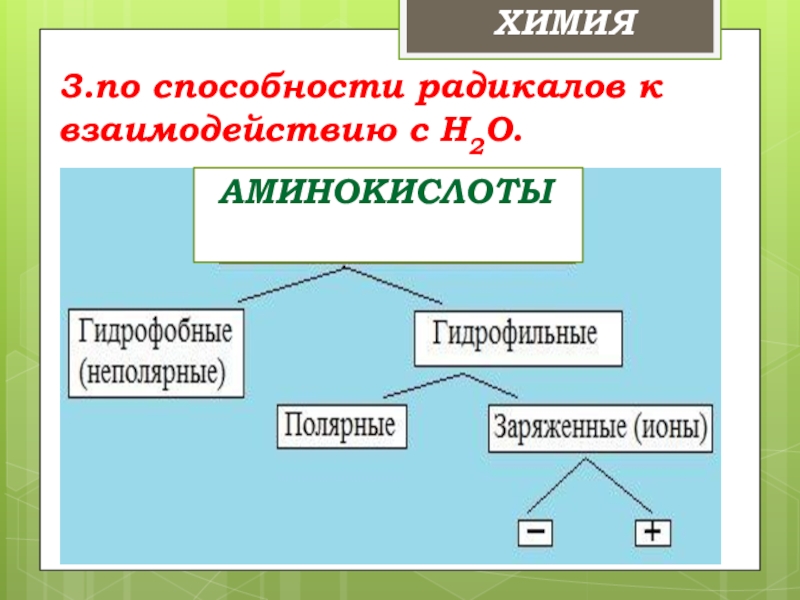
- 15. 3.по способности радикалов к взаимодействию с Н2О. ХИМИЯ АМИНОКИСЛОТЫАМИНОКИСЛОТЫ
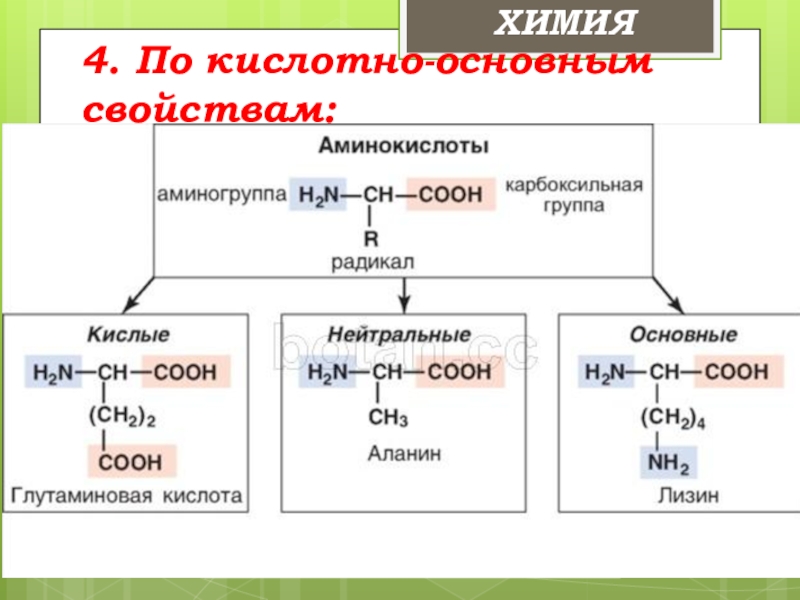
- 16. 4. По кислотно-основным свойствам:ХИМИЯ
- 17. Незаменимые (8) не синте-зируются организмом из других
- 18. ХИМИЯ Изомерия аминокислотСтруктурная изомерия:
- 19. Оптическая изомерия ХИМИЯ «Зеркало Венеры», 1898
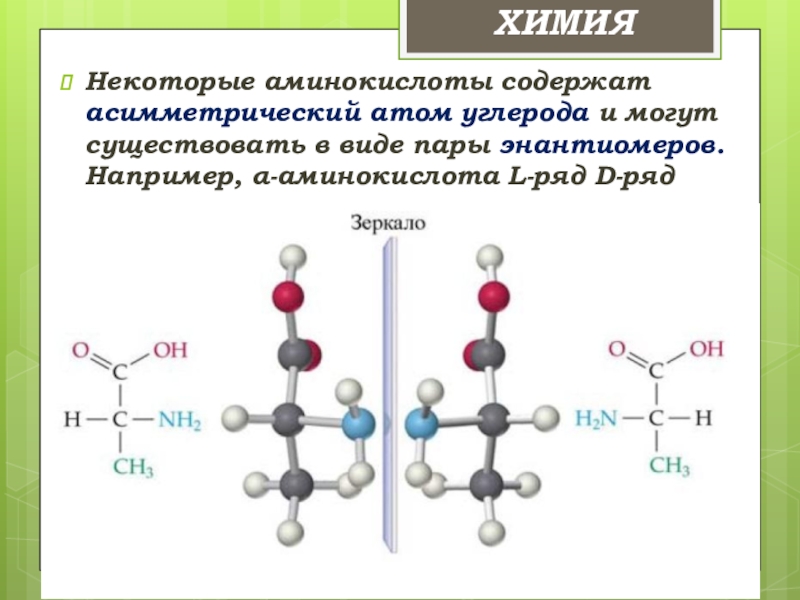
- 20. Некоторые аминокислоты содержат асимметрический атом углерода и
- 21. ХИМИЯ
- 22. нелетучие кристаллические вещества высокие температуры плавлениянерастворимы в
- 23. В кристаллическом состоянии существуют в виде внутренних
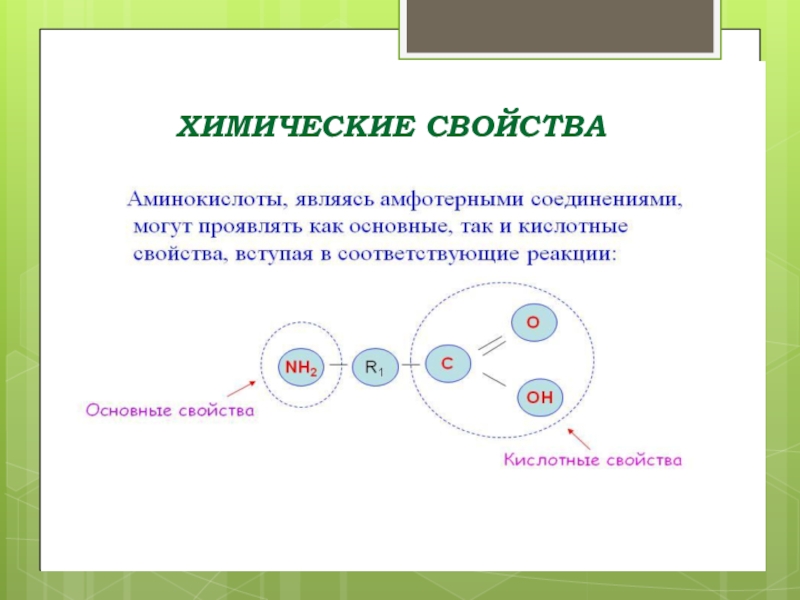
- 24. ХИМИЧЕСКИЕ СВОЙСТВА
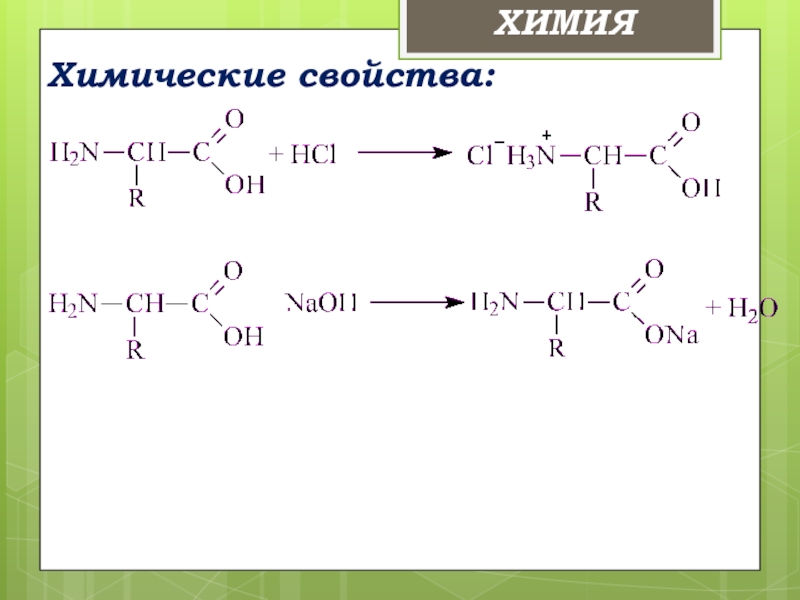
- 25. Химические свойства:ХИМИЯ
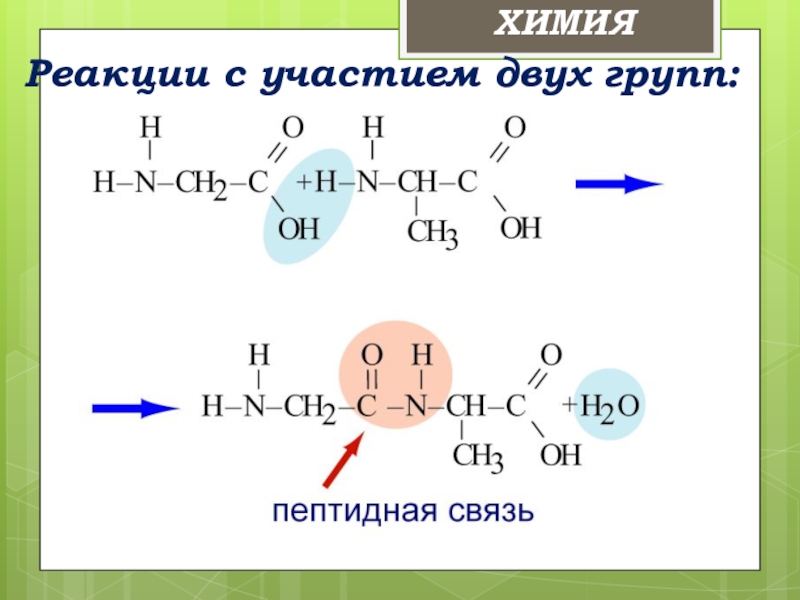
- 26. Реакции с участием двух групп:ХИМИЯ
- 27. Пептиды :- продукты поликонденсации, построенные из α-аминокислот.
- 28. Слайд 28
- 29. Белки - сложные высокомолекулярные природные соединения, построенные
- 30. Свойства живого, связанные с белками:Способность к воспроизведению себе подобных.Сократимость и движение.Обмен веществ. ХИМИЯ
- 31. Задание к видеофрагменту: Сколько белков должен употреблять ежедневно человек?Какая пища является источником белка?Почему белки разные?ХИМИЯ
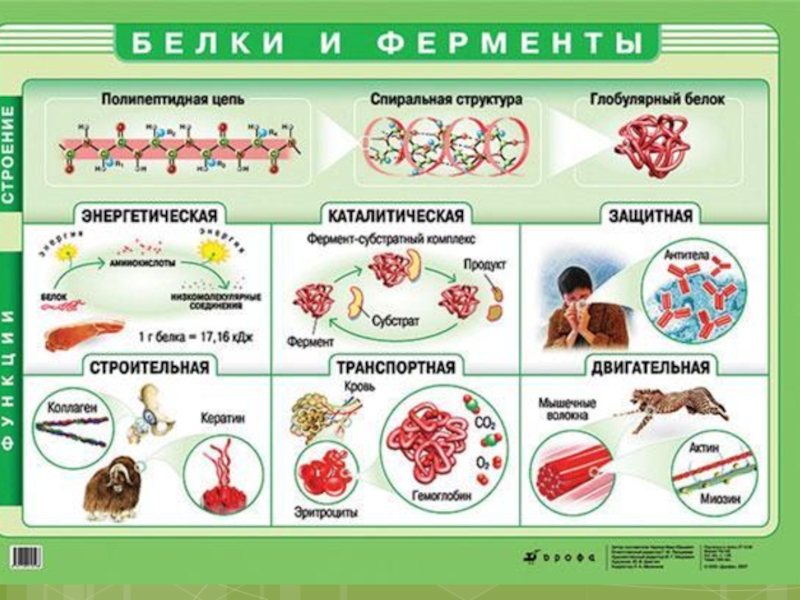
- 32. Функции белков: СтроительнаяБелки участвуют в образовании всехмембран и органоидов клетки.белоккератинХИМИЯ
- 33. КаталитическаяВ каждой клетке имеются сотни ферментов. Они
- 34. ТранспортнаяБелки связывают и переносят
- 35. Регуляторная Белки - гормоны регулируют различные
- 36. ЗащитнаяНапример, фибриноген и протромбинобеспечивают свертываемость кровиАнтитела блокируют
- 37. СократительнаяБелки - участвуют в сокращении мышечных волоконАктин и миозин – белки мышцХИМИЯ
- 38. Энергетическая1г белка - 17.6 кДжПри недостатке углеводов
- 39. Физико-химические свойства белков Белки имеют высокий молекулярный
- 40. Химические свойства :Поддаются гидролизу с образованием аминокислот.Денатурируются:
- 41. Для обнаружения белков в растворе применяются цветные
- 42. Структурная организация белков.
- 43. Первичная структура белка – это последовательность аминокислот в полипептидной цепи.пептидная связь
- 44. Слайд 44
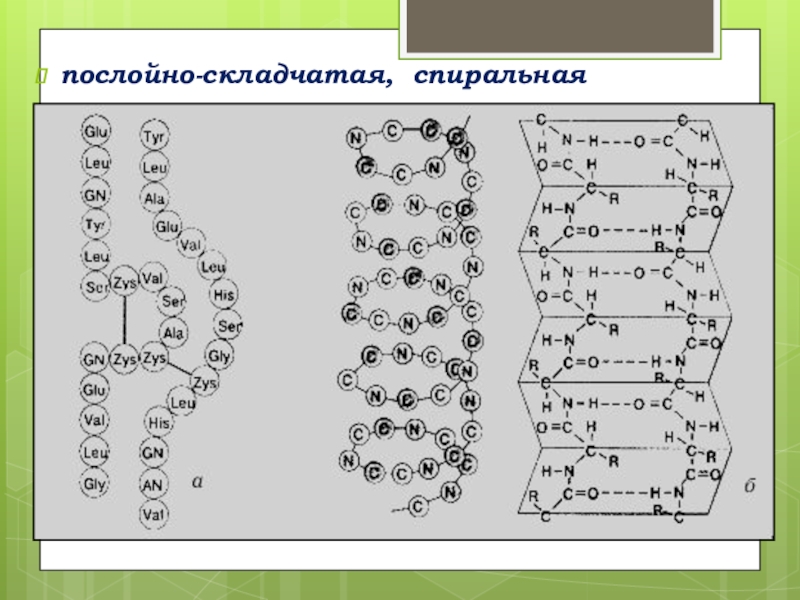
- 45. Вторичная структура - спираль, удерживаемая водородными связями.
- 46. послойно-складчатая, спиральная
- 47. Третичная структура – имеет вид клубка, удерживаемого взаимодействием различных остатков аминокислот. (дисульфидные связи)
- 48. Четвертичная структура агрегаты нескольких
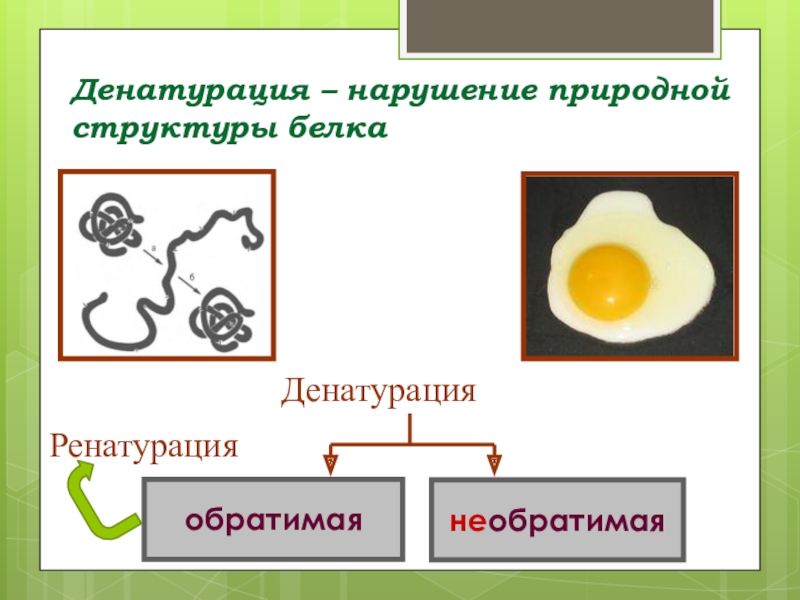
- 49. Денатурация – нарушение природной структуры белка.ДенатурациянеобратимаяобратимаяРенатурация
- 50. Слайд 50
- 51. Проблемный вопрос:Можно ли утверждать что: «Нет белка
- 52. Ситуационные задачи Почему яйца или молоко применяют в качестве противоядия при отравлении солями тяжелых металлов?
- 53. Токсическое воздействие алкоголя на головной мозг воспринимается
- 54. Ситуационные задачи Почему ученые называют белки биологическими «бусами»?
- 55. Домашнее задание:1. Изучить тему: «Аминокислоты, пептиды, белки»2.
- 56. Слайд 56
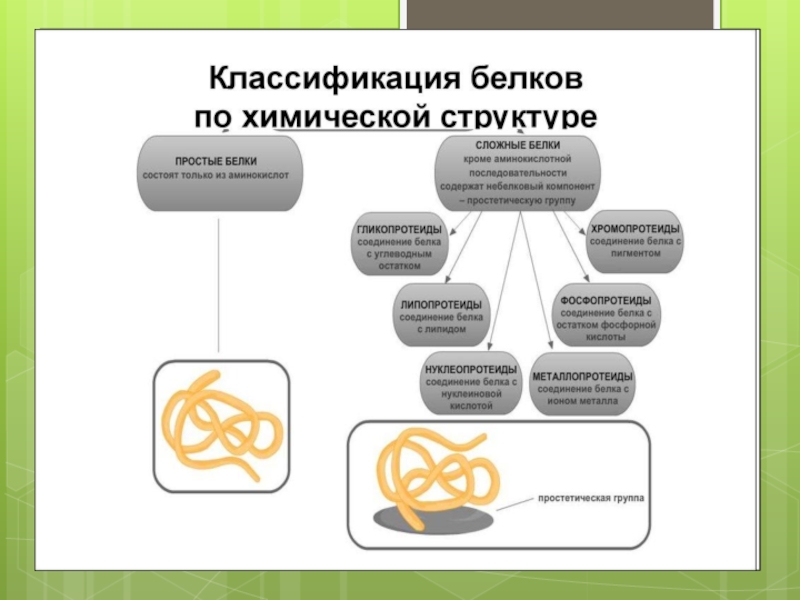
- 57. Сложные белки: 1. Гликопротеины (содержат углеводы). 2.
- 58. Слайд 58
Слайд 3Рождение химии белка…
Впервые белок был выделен (в виде клейковины) в
ХИМИЯ
Слайд 4
Жерар Мульдер
"Во всех растениях и животных присутствует некое вещество, которое без
ХИМИЯ
Слайд 5Белки, или протеины
что происходит от греч.
protos — первый, первичный.
Одновременно с Мульдером
Анри Браконно в результате длительного нагревания кожи, сухожилий получил первую аминокислоту, сладкую на вкус - гликоколл (глицин).
ХИМИЯ
Слайд 6Проблемный вопрос:
Можно ли утверждать что: «Нет белка – нет органической жизни
ХИМИЯ
Слайд 7Содержание учебного материала:
Аминокислоты: строение молекулы, номенклатура и изомерия, кислотно-основные свойства, значение.
Белки: строение молекулы, свойства, роль в организме.
ХИМИЯ
Слайд 8
Аминокислоты - это производные кислот, у которых атом водорода в
ХИМИЯ
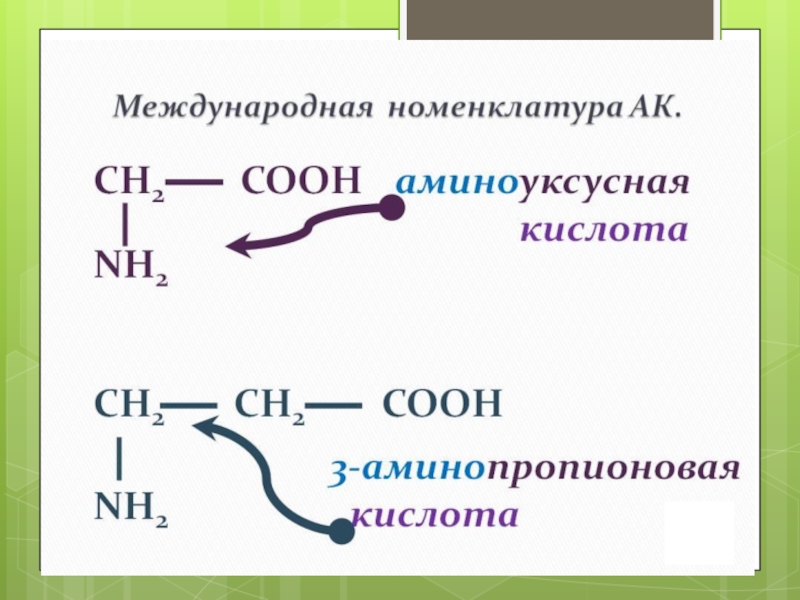
Слайд 142. По взаимному расположению функциональных групп
выделяют α-, ß-, γ- и
ХИМИЯ
Слайд 17Незаменимые (8) не синте-зируются организмом из других соединений, поэтому должны поступать
Полузамени-мые – (2) частично должны поступать с пищей.
Заменимые
(10)- синтези-руются в организме из незаменимых или других соединений.
ХИМИЯ
АМИНОКИСЛОТЫ
4.По биологическому значению:
Слайд 20Некоторые аминокислоты содержат асимметрический атом углерода и могут существовать в виде
ХИМИЯ
Слайд 22нелетучие кристаллические вещества
высокие температуры плавления
нерастворимы в неполярных органических растворителях и
молекулы обладают большими дипольными моментами.
ХИМИЯ
Физические свойства:
Слайд 23В кристаллическом состоянии существуют в виде внутренних солей, т.е. биполярных ионов:
Значение
ХИМИЯ
Слайд 27Пептиды :
- продукты поликонденсации, построенные из α-аминокислот.
По числу аминокислотных остатков
ХИМИЯ
Слайд 29Белки - сложные высокомолекулярные
природные соединения,
построенные из остатков
α-аминокислот.
Аминокислоты в
20 видов аминокислот входят в состав белков.
ХИМИЯ
Слайд 30 Свойства живого, связанные с белками:
Способность к воспроизведению себе подобных.
Сократимость и
Обмен веществ.
ХИМИЯ
Слайд 31Задание к видеофрагменту:
Сколько белков должен употреблять ежедневно человек?
Какая пища является источником
Почему белки разные?
ХИМИЯ
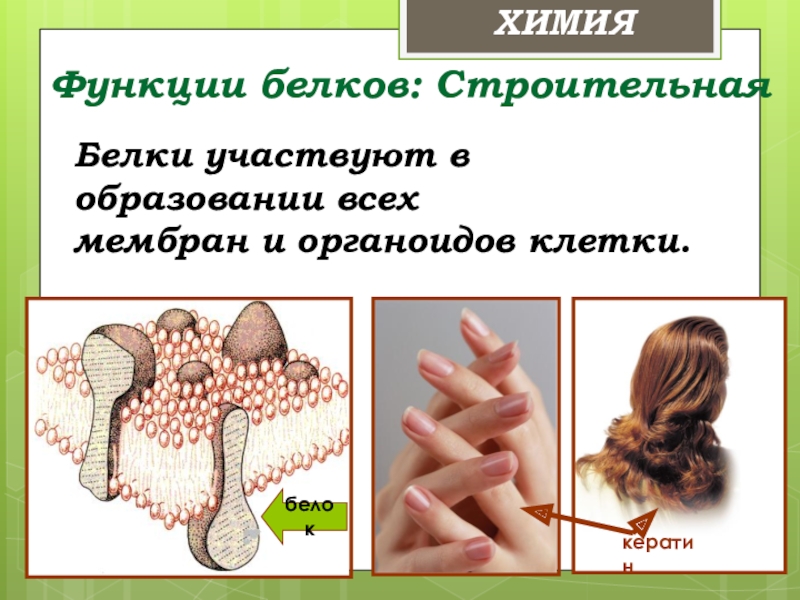
Слайд 32Функции белков: Строительная
Белки участвуют в образовании всех
мембран и органоидов клетки.
белок
кератин
ХИМИЯ
Слайд 33Каталитическая
В каждой клетке имеются сотни ферментов.
Они помогают осуществлять биохимические
реакции,
Ускоряют реакции в 108
раз. Могут контроли-
ровать до 1000 реакций
в секунду.
ХИМИЯ
Слайд 34Транспортная
Белки связывают и переносят
различные вещества
клетки, и по всему организму.
Например, г е м о г л о б и н
крови переносит кислород.
ХИМИЯ
Слайд 35Регуляторная
Белки - гормоны регулируют
различные физиологические
процессы.
Например, инсулин
уровень углеводов в крови.
ХИМИЯ
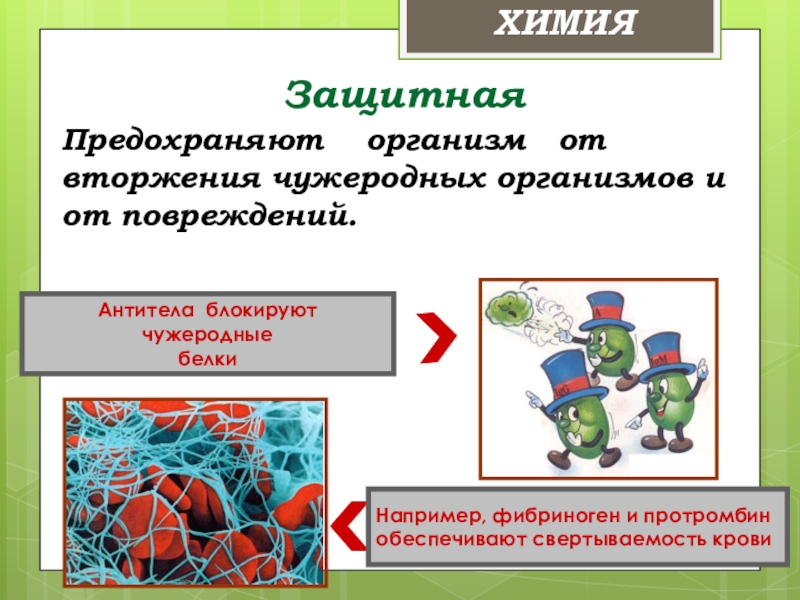
Слайд 36Защитная
Например, фибриноген и протромбин
обеспечивают свертываемость крови
Антитела блокируют чужеродные
белки
Предохраняют организм
ХИМИЯ
Слайд 37Сократительная
Белки - участвуют в сокращении
мышечных волокон
Актин и миозин – белки
ХИМИЯ
Слайд 38Энергетическая
1г белка - 17.6 кДж
При недостатке углеводов или жиров окисляются молекулы
При полном расщеплении белка до конечных продуктов выделяется энергия
!!! Но в качестве источника энергии белки используются крайне редко.
ХИМИЯ
Слайд 39Физико-химические свойства белков
Белки имеют высокий молекулярный вес 16 000-1 000 000.
Заряд
Белковые растворы - коллоидные растворы с разными свойствами.
Осаждение белков. У белков есть гидратная оболочка, заряд, препятствующий склеиванию. Для осаждения необходимо снять гидратную оболочку и заряд. Реакции осаждения делят на два вида. 1. Высаливание белков:
2. Осаждения с потерей нативных свойств белка .
ХИМИЯ
Слайд 40Химические свойства :
Поддаются гидролизу с образованием аминокислот.
Денатурируются: разрушается структура
Горят - появляется
Для белков характерны цветные реакции.
ХИМИЯ
Слайд 41Для обнаружения белков в растворе применяются цветные реакции:
Видеоопыт: «Цветные реакции на
Задание:
Записать название реакции, необходимые реактивы и наблюдения.
Как по-другому можно назвать цветные реакции?
ХИМИЯ
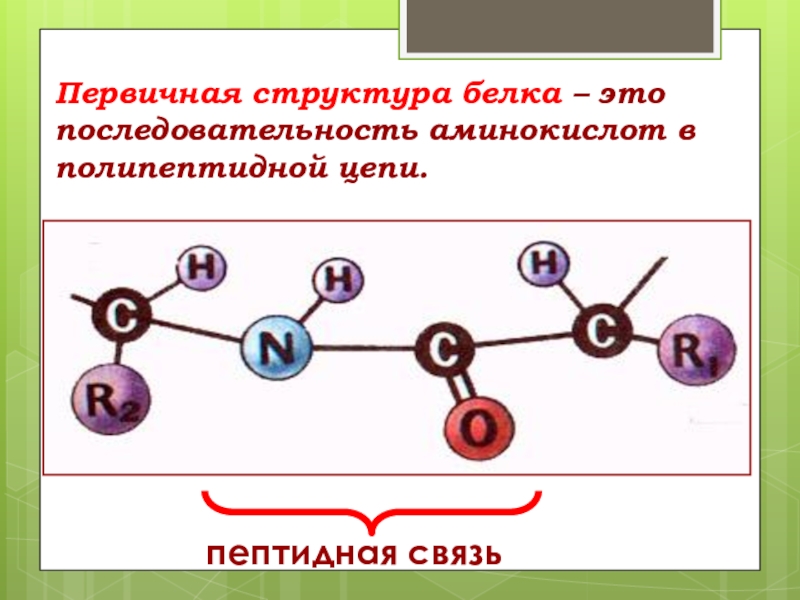
Слайд 43Первичная структура белка – это последовательность аминокислот в полипептидной цепи.
пептидная связь
Слайд 47 Третичная структура – имеет вид клубка, удерживаемого взаимодействием различных остатков
(дисульфидные связи)
Слайд 48 Четвертичная структура
агрегаты нескольких белковых макромолекул (белковые
Слайд 49Денатурация – нарушение природной структуры белка.
Денатурация
необратимая
обратимая
Ренатурация
Слайд 51Проблемный вопрос:
Можно ли утверждать что: «Нет белка – нет органической жизни
ХИМИЯ
Слайд 52Ситуационные задачи
Почему яйца или молоко применяют в качестве противоядия при
Слайд 53Токсическое воздействие алкоголя на головной мозг воспринимается человеком как опьянение; это
Слайд 55Домашнее задание:
1. Изучить тему: «Аминокислоты, пептиды, белки»
2. Выполнить задания 17.13 –
Зубарян С.Э., Лузин А. П. Органическая химия: учебник / Под ред.проф Н.А. Тюкавкиной. – М.: ГЕОТАР – Медиа, 2015. - с.313-326