- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку в 8 классе
Содержание
- 1. Презентация к уроку в 8 классе
- 2. Урок по теме: « Кислоты, свойства кислот.
- 3. Эпиграф урока:О вы, которых ожидает Отечество от
- 4. - Много славных имен оставил наш народ
- 5. «Ломоносов был великий человек… Он создал первый
- 6. Трудно назвать какую-либо отрасль науки из существовавших
- 7. Повторим изученное.1. какой класс веществ вы изучили?(оксиды)2.
- 8. Лабораторный опыт. «Действие растворов кислот на индикаторы».1.
- 9. Заполнить таблицу.
- 10. "Индикаторы"Краснеют от кислот , как от
- 11. Путешествие в «Царство Кислот».
- 12. Путешествие в «Царство кислот». О каком
- 13. « Портретная Галерея».Выполнить задания.Прочитать о физических свойствах
- 14. ТАБЛИЦА С ПОМЕТКАМИ.
- 15. СЕРНАЯ КИСЛОТАОткрытый урок 9 классСЕРНАЯ и СОЛЯНАЯ КИСЛОТЫ.
- 16. ВОПРОСЫ КЛАССУКакие правила Т/Б необходимо соблюдать при
- 17. Интересный опыт:Что произойдет, если к сахару добавить концентрированную серную кислоту?
- 18. «Портретная галерея».Задание 2.Прочитать текст о химических свойствах
- 19. Правила обращения с серной кислотой ОБРАЩАТЬСЯ
- 20. Оригинальность Плавиковая кислота обладает оригинальными свойствами: она
- 21. SO2+H2O=H2SO3 ОБРАЗОВАНИЕ КИСЛОТНЫХ ДОЖДЕЙ В ПРИРОДЕ.
- 22. «Металлический мост».Мы исследуем взаимодействие кислот с металлами.Лабораторный
- 23. Вытеснительный ряд металлов.Где располагаются цинк и
- 24. Николай Николаевич Бекетов.
- 25. «Пропуск на выезд из царства кислот».Выполнить тестовые
- 26. Серная кислотаC серной кислотой люди познакомились значительно
- 27. « Путевые заметки».Зачитайте свои «путевые» заметки по
- 28. Приём «Синквейн»Учитель
- 29. Кластер по теме: «Кислоты, взаимодействие кислот с металлами».
Слайд 1Кислоты
Неорганическая химия
8 класс
Учитель химии высшей категории МКОУ «Товарковская средняя общеобразовательная
Слайд 2Урок по теме: « Кислоты, свойства кислот. Взаимодействие кислот с металлами». Химия, 8 класс.
Слайд 3Эпиграф урока:
О вы, которых ожидает Отечество от недр своих
И видеть
Каких зовет из стран чужих,
О, ваши дни благословенны!
Дерзайте ныне ободренны
Раченьем вашим показать,
Что может собственных Платонов
И быстрых разумом Невтонов
Российская земля рождать”.
Слайд 4- Много славных имен оставил наш народ мировой науке.
Образ М.В.
« Жить – значит узнавать! Жить – это, значит, мечтать широко и привольно!
Жить – это, значит, творить, трудясь без устали, с неисчерпаемым вдохновением».
Д.И. Менделеев.
Слайд 5«Ломоносов был великий человек… Он создал первый университет. Он, лучше сказать, сам был первым
Я знак бессмертия себе воздвигнул
Превыше пирамид и крепче меди,
Что бурный аквилон сотреть не может,
Ни множество веков, ни едка древность.
Не вовсе я умру; но смерть оставит
Велику часть мою, как жизнь скончаю.
Я буду возрастать повсюду славой,
Пока великий Рим владеет светом.
Где быстрыми шумит струями Авфид,
Где Давнус царствовал в простом народе,
Отечество мое молчать не будет,
Что мне беззнатный род препятством не был,
Чтоб внесть в Италию стихи эольски
И первому звенеть Алцейской лирой.
Взгордися праведной заслугой, муза,
И увенчай главу дельфийским лавром.
1747
Слайд 6Трудно назвать какую-либо отрасль науки из существовавших в XVIII в.,
в
В физике, астрономии, метеорологии, химии, геологии, горном деле,
металлургии, географии, истории, теории словесности и литературе
он либо создал капитальные труды, совершил выдающиеся научные открытия,
либо выдвинул новые идеи, высказал гениальные прогнозы.
Многие идеи Ломоносова на десятки лет и столетия опередили свое время.
Академик М.В.Келдыш
Слайд 7Повторим изученное.
1. какой класс веществ вы изучили?
(оксиды)
2. Что такое оксиды? Какие
3.Какие вещества получаются при взаимодействии оксидов неметаллов с водой? Привести примеры. Подтвердить записью уравнений реакций.
4. Как определить наличие кислоты?
(индикатором).
Слайд 8Лабораторный опыт.
«Действие растворов кислот на индикаторы».
1. В одну из трёх
2. Во вторую ячейку прилейте
метилового – оранжевого. Что произошло?
3. В третью ячейку опустите фенолфталеиновую бумажку.
Наблюдения оформите в таблицу.
Слайд 10 "Индикаторы"
Краснеют от кислот , как от стыда
С и н и
Индикаторы были открыты Р.Бойлем в ХVII веке
Индикатор - указатель
Слайд 12Путешествие в «Царство кислот».
О каком веществе говорится в рассказе?
S → SO2 → SO3 → H2SO4
Слайд 13« Портретная Галерея».
Выполнить задания.
Прочитать о физических свойствах серной соляной кислот и
V - это я знаю
+ - новая информация;
- - информация,противоречащая моим знаниям;
? - информация требует пояснения;
!-это интересно.
Слайд 16ВОПРОСЫ КЛАССУ
Какие правила Т/Б необходимо соблюдать при работе с серной кислотой
Что произойдет, если концентрированная кислота попадет на кожу рук или лица? Какую медицинскую помощь необходимо оказать?
Какой газ в опыте с сахарной пудрой поднимает массу, а какой вызывает запах?
Прав Дмитрий Иванович Менделеев:
«Опыт – единственно верный путь спрашивать природу и слышать ответ в ее лаборатории»
Слайд 18«Портретная галерея».
Задание 2.
Прочитать текст о химических свойствах кислот. Сделать пометки на
Концентрированная серная кислота обугливает органические вещества.
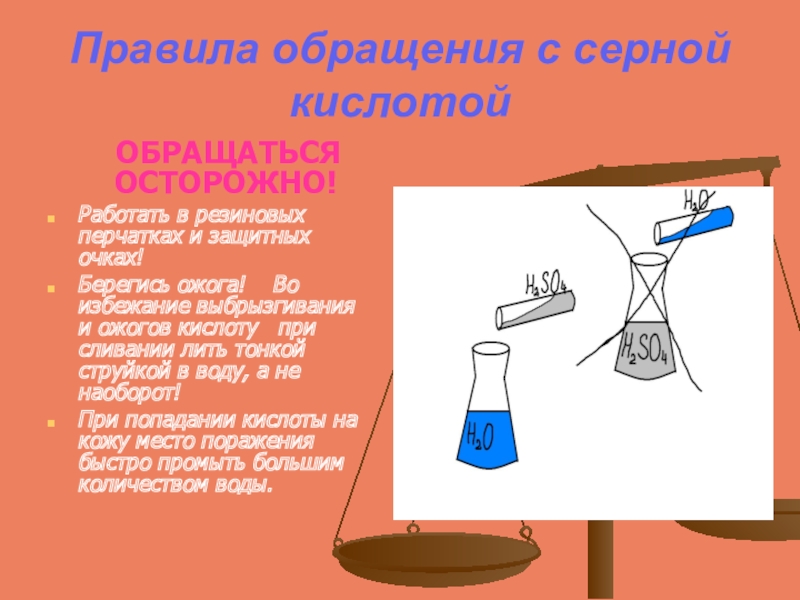
Слайд 19Правила обращения с серной кислотой
ОБРАЩАТЬСЯ ОСТОРОЖНО!
Работать в резиновых перчатках
Берегись ожога! Во избежание выбрызгивания и ожогов кислоту при сливании лить тонкой струйкой в воду, а не наоборот!
При попадании кислоты на кожу место поражения быстро промыть большим количеством воды.
Слайд 20Оригинальность
Плавиковая кислота обладает оригинальными свойствами: она легко реагирует с оксидом
Поскольку стекло содержит изрядное количество этого оксида, то хранить кислоту приходится не в стеклянной посуде, а в полиэтиленовой.
Легко представить, что получится, если какой-то химик перельет эту кислоту в стеклянную колбу.
Слайд 22«Металлический мост».
Мы исследуем взаимодействие кислот с
металлами.
Лабораторный опыт №3.
Лабораторный опыт №4.
Какой
Слайд 23 Вытеснительный ряд металлов.
Где располагаются цинк и медь в этом ряду?
Почему
Слайд 24Николай Николаевич Бекетов.
Русский физико -химик, с 1886 г академик Петербургской АН. Родился в Алферьевке (ныне Новая Бекетовка Пензенской области).
В 1848 г окончил Казанский университет. В 1849-1853 гг. работал в Медико - хирургической академии в лаборатории Н.Н.Зинина, в 1854-1855 гг. - в Петербургском университете, с 1855 г. - в Харьковском университете (в 1859 г. стал профессором), с 1886 г. - в Химической лаборатории Петербургской АН и преподавал на Высших женских курсах в Петербурге.
Один из основоположников физической химии. алюминотермии. Прочитал первый курс лекций по физической химии и организовал практикум в 1865 г. По его предложению в 1864 г в Харьковском университете было учреждено физико - химическое отделение.
Президент Русского физико - химического общества в 1889-1890, 1896-1897, 1900, 1902, 1903, 1911 гг.
Слайд 25«Пропуск на выезд из царства кислот».
Выполнить тестовые задания на карточках.
Соединение
1) H2 SO4; 2) Cu S; 3) SO2; 4) Na2 S.
Соединение серы, для которого характерны следующие свойства: обугливает древесину, сахар, растворяется в воде, , имеет формулу:
1) FeS; 2) H2 SO4 3) SO2; 4) H2 S.
При прибавлении лакмуса к раствору серной кислоты раствор окрашивается в:
1) синий цвет; 2) красный цвет; 3) жёлтый цвет; 4) малиновый цвет.
Раствор серной кислоты взаимодействует с металлом:
1)магнием; 2) медью; 3) золотом; 4) серебром.
Слайд 26Серная кислота
C серной кислотой люди познакомились значительно позднее, примерно в 10
маслом». Именно под таким названием серная кислота была известна в России. Серную кислоту называют «матерью всех кислот».
Слайд 27« Путевые заметки».
Зачитайте свои «путевые» заметки по путешествию в «ЦАРСТВО кислот».
Продолжите
1. Сегодня на уроке…
2. Теперь я знаю…
3. Мне на уроке…
Дома: составить кластер о свойствах кислот.
Слайд 28Приём «Синквейн»
Учитель
1 существительное Ломоносов
2 прилагательных Великий Знаменитый
3 глагола Учился Работал Открывал
Фраза Делал открытия в разных областях науки
Вывод Учёный