CaO+H2O=Ca(OH)2
4HNO3=2H2O+4NO2+O2
CuSO4+Fe=FeSO4+Cu
AgNO3+KBr=AgBr +К NO3
4Fe(OH)2+2H2O+O2=4Fe(OH)3
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку Типы химических реакций
Содержание
- 1. Презентация к уроку Типы химических реакций
- 2. Химические реакции происходят: при смешении или физическом
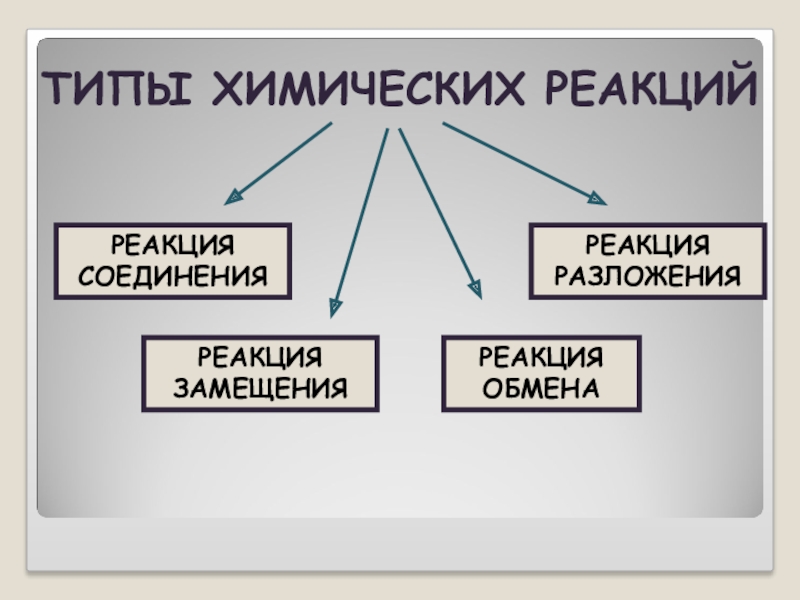
- 3. Типы химических реакций
- 4. План урокаКлассификации химических реакций по различным признакамТипы
- 5. По тепловому эффектуПо числу вступивших в реакцию веществПо обратимостиПо изменению степени окисленияПо агрегатному состоянию веществПо механизму
- 6. По тепловому эффектуРеакции, протекающие с выделением теплоты,
- 7. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙРЕАКЦИЯ СОЕДИНЕНИЯРЕАКЦИЯ РАЗЛОЖЕНИЯРЕАКЦИЯ ЗАМЕЩЕНИЯРЕАКЦИЯ ОБМЕНА
- 8. Реакции соединения Несколько простых или сложных
- 9. – это реакции, в которых из нескольких
- 10. 1) 2HgO = 2Hg + O22) CaCO3
- 11. Реакция разложения одного сложного вещества с образованием несколько новых веществ, называется реакцией разложения.
- 12. Реакции разложенияИз одного сложного вещества получаются несколько
- 13. – это реакции, в результате которых сложное
- 14. 1) CaO + CO2 = CaCO32) CO2
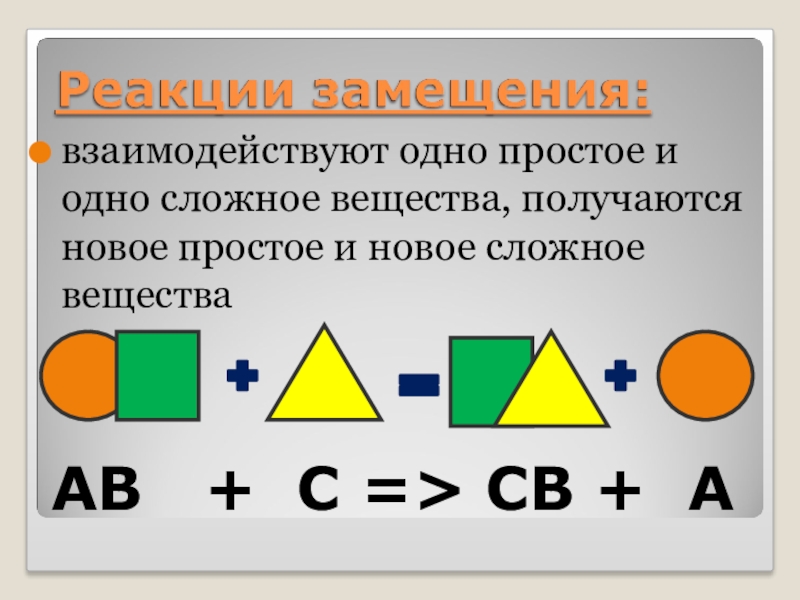
- 15. Реакции замещенияЭто реакции между простым и сложным
- 16. АВ + С => СВ + А взаимодействуют одно
- 17. 1) CaO + CO2 = CaCO32) CO2
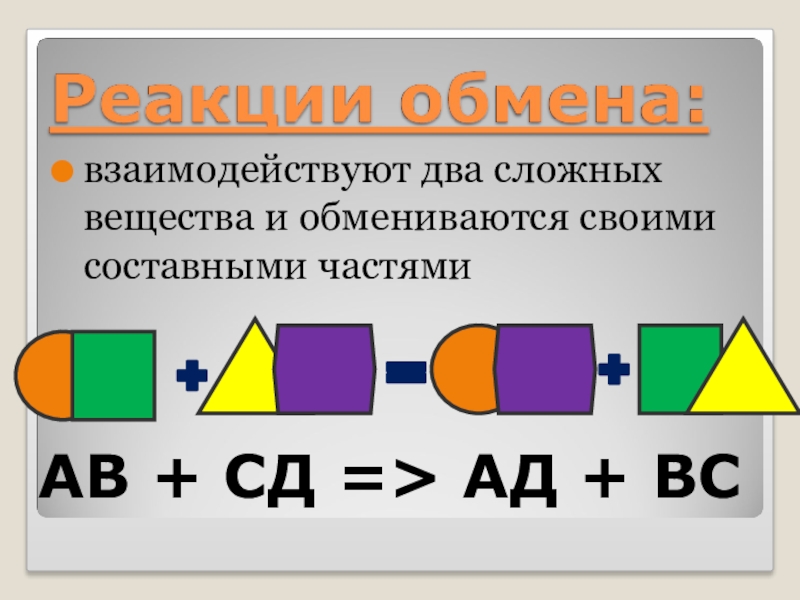
- 18. Реакции обменаЭто реакции, при которых два сложных
- 19. АВ + СД => АД + ВС взаимодействуют два сложных вещества и обмениваются своими составными частями
- 20. Игра «ТРЕТИЙ ЛИШНИЙ-1»1. 2NaCl = 2Na +
- 21. Задание1. Выберите на ваш взгляд, правильный ответ.
- 22. Лабораторный опыт 2Типы химических реакцийЦель:ВЫВОД
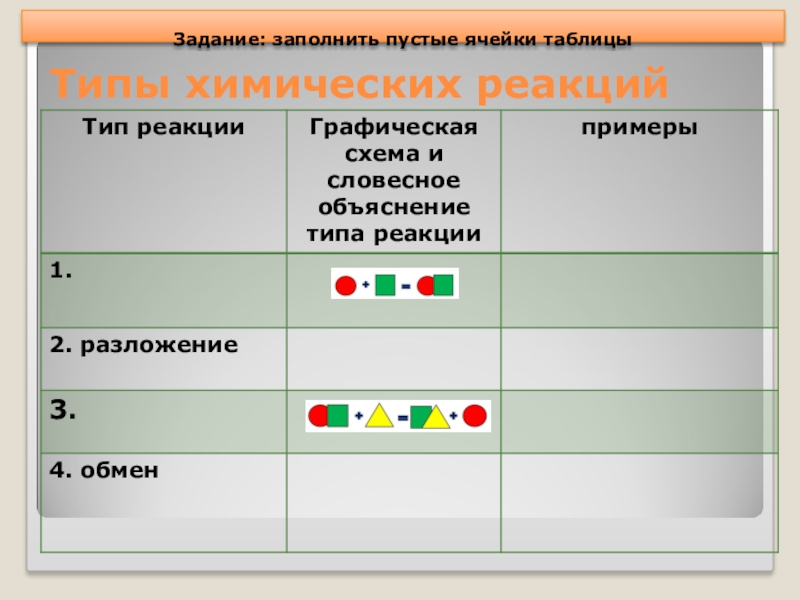
- 23. Типы химических реакцийЗадание: заполнить пустые ячейки таблицы
- 24. Слайд 24
- 25. Домашнее задание§16 читать, зад. 3,6,7 на стр. 56В тетради для домашних работ
Слайд 1
Химическая реакция — превращение одного или нескольких исходных веществ в отличающиеся
Слайд 2Химические реакции происходят:
при смешении или физическом контакте реагентов самопроизвольно
при нагревании
при
действии света
электрического тока
механического воздействия и т. п.
Слайд 4План урока
Классификации химических реакций по различным признакам
Типы химических реакций по числу
Реакции разложения, соединения
Реакции замещения, обмена
Слайд 5По тепловому эффекту
По числу вступивших в реакцию веществ
По обратимости
По изменению степени
По агрегатному состоянию веществ
По механизму
Слайд 6
По тепловому эффекту
Реакции, протекающие с выделением теплоты, называются –
ЭКЗОТЕРМИЧЕСКИМИ
4P+5O2=2P2O5+Q
Протекающие с поглощением теплоты –
ЭНДОТЕРМИЧЕСКИМИ (-Q)
N2+O2 = 2NO-Q
Реакции, протекающие с выделением теплоты и света называются - РЕАКЦИЯМИ ГОРЕНИЯ
Слайд 8Реакции соединения
Несколько простых или сложных веществ соединяются в
Zn + S = ZnS
CaO + CO2 = CaCO3
Na2O + H2O = NaOH
Al + 3O2 = Al2O3
Левая часть уравнения – несколько веществ,
правая часть – только одно сложное!
Слайд 9– это реакции, в которых из нескольких простых или сложных веществ
Реакции соединения -
Подавляющее большинство реакций соединения экзотермичны.
Слайд 101) 2HgO = 2Hg + O2
2) CaCO3 = CaO + CO2
3)
4) CuO + H2 = Cu + H2O
5) 2H2 + O2 = 2H2O
6) H2SO4 + 2KOH = K2SO4 + 2H2O
7) BaO + SO2 = BaSO3
Слайд 11Реакция разложения одного сложного вещества с образованием несколько новых веществ, называется
Слайд 12Реакции разложения
Из одного сложного вещества получаются несколько других веществ
CaCO3 = CaO + CO2
KMnO4 = K2MnO4 + MnO2 + O2
Fe(OH)3 = Fe2O3 + 3 H2O
В левой части уравнения – одно сложное вещество, в правой – несколько различных (менее сложных по составу).
Слайд 13– это реакции, в результате которых сложное вещество разлагается на несколько
Реакции разложения -
Слайд 141) CaO + CO2 = CaCO3
2) CO2 + 2NaOH = Na2CO3
3) Fe + S = FeS
4) 2H2O = 2H2 + O2↑
5) CuO + H2 = Cu + H2O
6) Zn + 2HCl = ZnCl2 + H2↑
7) ZnO + H2SO4 = ZnSO4 + H2O
8) Cu(OH)2 = CuO + H2O
Слайд 15Реакции замещения
Это реакции между простым и сложным веществами, в которых атомы
Mg + 2 HCl = MgCl2 + H2
3 CuSO4 + 2 Al = Al2(SO4)3 +3 Cu
Левая часть уравнения – простое и сложное вещества, правая – новое простое и новое сложное
Слайд 16АВ + С => СВ + А
взаимодействуют одно простое и одно сложное
Слайд 171) CaO + CO2 = CaCO3
2) CO2 + 2NaOH = Na2CO3
3) Fe + S = FeS
4) 2H2O = 2H2 + O2↑
5) CuO + H2 = Cu + H2O
6) Zn + 2HCl = ZnCl2 + H2↑
7) ZnO + H2SO4 = ZnSO4 + H2O
8) Cu(OH)2 = CuO + H2O
Слайд 18Реакции обмена
Это реакции, при которых два сложных вещества обмениваются своими составными
CuO + 2 H2SO4 = CuSO4 + H2O
AgNO3 + HCl = HNO3 + AgCl
Слайд 19АВ + СД => АД + ВС
взаимодействуют два сложных вещества и
Слайд 20Игра «ТРЕТИЙ ЛИШНИЙ-1»
1. 2NaCl = 2Na + Cl2
2. CaO + CO2
3. C + O2 =CO2
Ответ:
2NaCl = 2Na + Cl2