- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку реакции обмена, 8 класс, Габриелян
Содержание
- 1. Презентация к уроку реакции обмена, 8 класс, Габриелян
- 2. С/о – самооценка.О/т – оценка товарища.Оценочная таблица
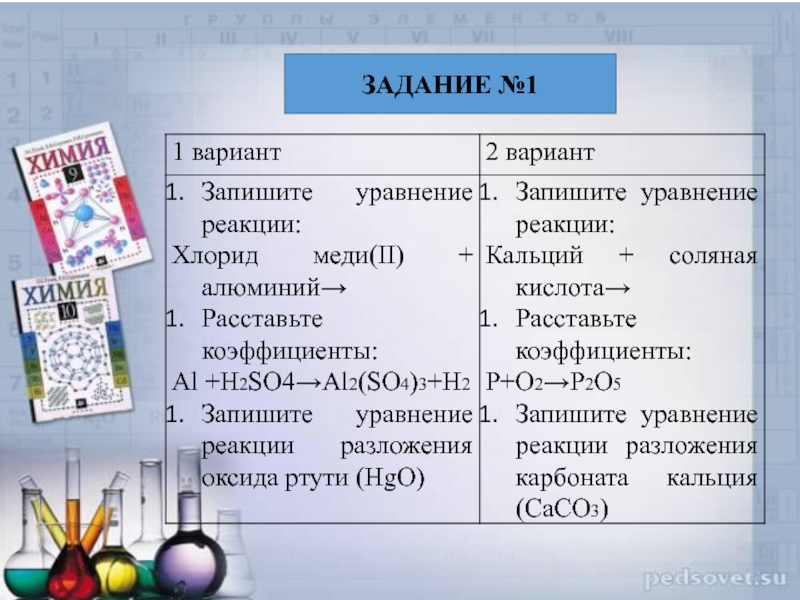
- 3. ЗАДАНИЕ №1
- 4. ОТВЕТЫ
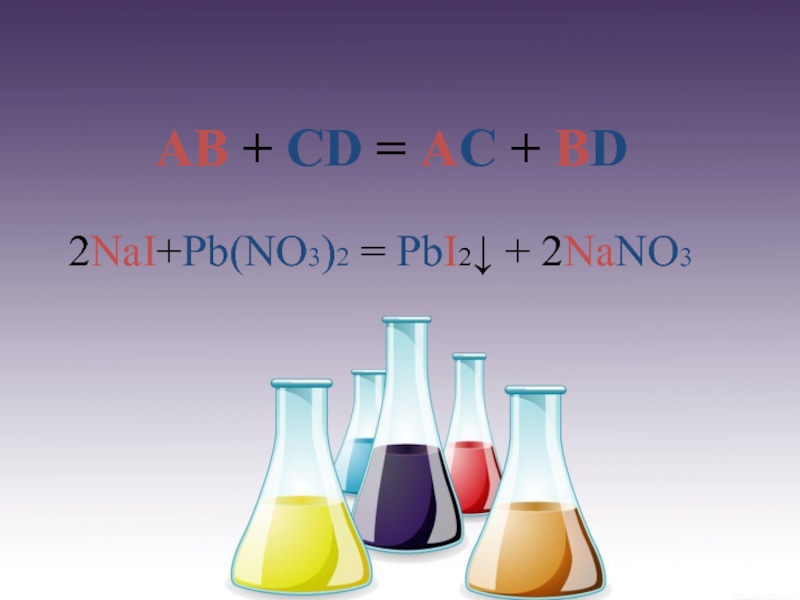
- 5. AB + CD = AC + BD 2NaI+Pb(NO3)2 = PbI2↓ + 2NaNO3
- 6. Реакции обмена
- 7. 1. изучить реакции обмена2. уметь правильно записывать
- 8. Это, друг, химкабинет, Для еды условий нет.Пусть
- 9. Опыт №1. 2NaOH + CuCl2 = Cu(OH)2
- 10. Если выделится газ - Это раз; И
- 11. Клод Луи Бертолле9 декабря 1748 г. – 6 ноября 1822 г.
- 12. BaCl2 + 2AgNO3→Ba(NO3)2+2AgCl↓Cu(NO3)2 + NaCl→CuCl2+NaNO3Pb(NO3)2 + K2S→PbS↓+2KNO3MgCl2 + K2SO4→MgSO4+KClHNO3 + ZnSO4→H2SO4+Zn(NO3)23Ca(NO3)2 +2 H3PO4→Ca3(PO4)2↓+6HNO3Ba(NO3)2 + Na2SO4→BaSO4↓+2NaNO3ЗАДАНИЕ №2
- 13. ОТВЕТЫ1. BaCl2 + 2AgNO3→Ba(NO3)2+2AgCl↓2. Cu(NO3)2 + NaCl→CuCl2+NaNO33.
- 14. Домашнее заданиеобязательное: прочитать §33, упражнение №3;дополнительное: выполнить
- 15. СПАСИБО ЗА УРОК!!!
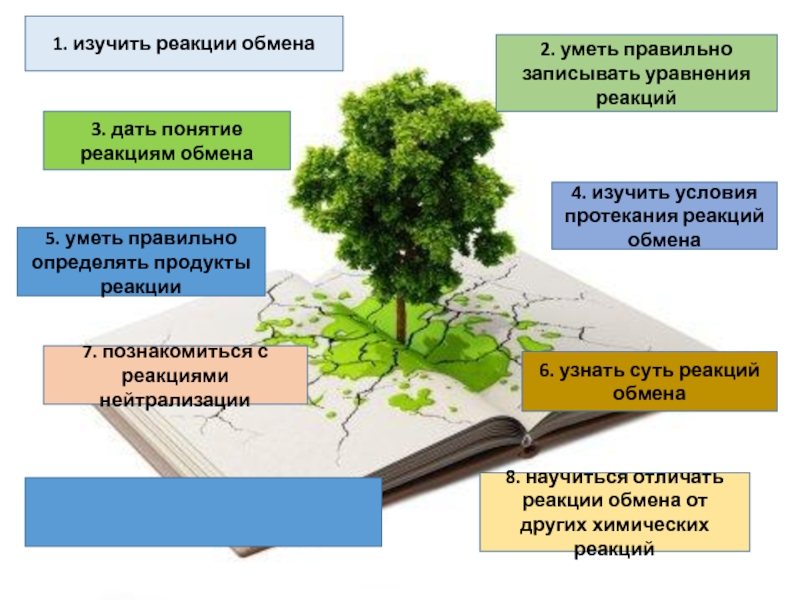
Слайд 71. изучить реакции обмена
2. уметь правильно записывать уравнения реакций
3. дать понятие
4. изучить условия протекания реакций обмена
5. уметь правильно определять продукты реакции
6. узнать суть реакций обмена
7. познакомиться с реакциями нейтрализации
8. научиться отличать реакции обмена от других химических реакций
Слайд 8Это, друг, химкабинет,
Для еды условий нет.
Пусть в пробирке пахнет воблой,
В колбе — будто мармелад.
Вещества на вкус не пробуй!
Сладко пахнет даже яд.
Всякое в опыте может случиться,
Внимательным будь и не оплошай.
Тебе всегда поможет учитель,
Паники только не допускай!
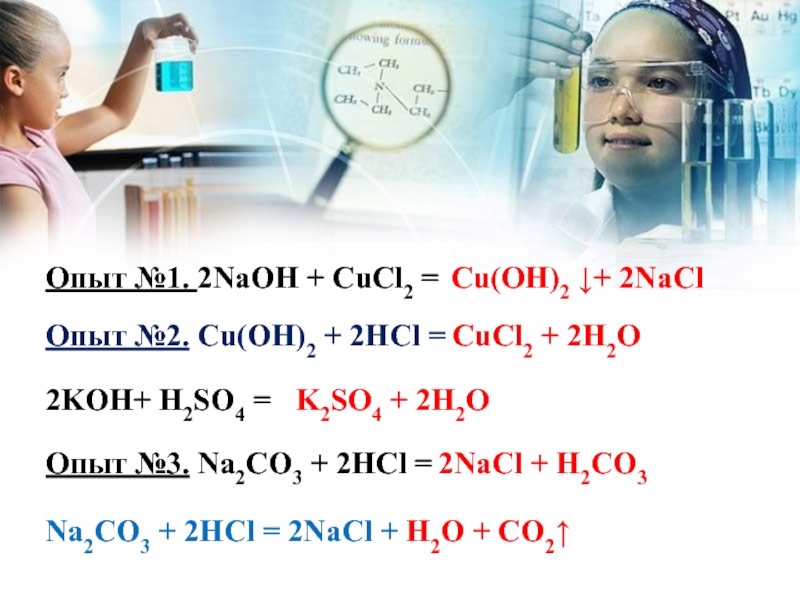
Слайд 9Опыт №1. 2NaOH + CuCl2 =
Cu(OH)2 ↓+ 2NaCl
Опыт №2.
CuCl2 + 2H2O
2KOH+ H2SO4 =
K2SO4 + 2H2O
Опыт №3. Na2CO3 + 2HCl =
2NaCl + H2CO3
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
Слайд 10Если выделится газ - Это раз; И получится вода - Это два; А
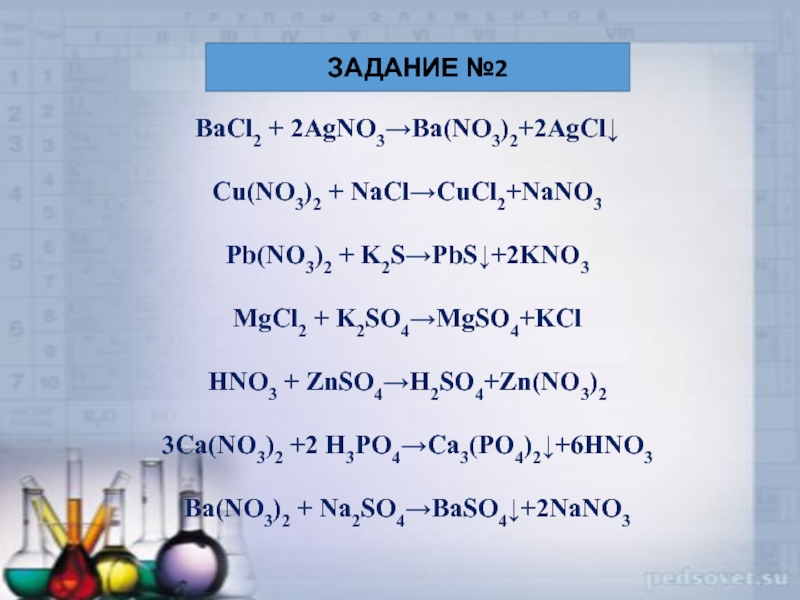
Слайд 12BaCl2 + 2AgNO3→Ba(NO3)2+2AgCl↓
Cu(NO3)2 + NaCl→CuCl2+NaNO3
Pb(NO3)2 + K2S→PbS↓+2KNO3
MgCl2 + K2SO4→MgSO4+KCl
HNO3 + ZnSO4→H2SO4+Zn(NO3)2
3Ca(NO3)2
Ba(NO3)2 + Na2SO4→BaSO4↓+2NaNO3
ЗАДАНИЕ №2
Слайд 13ОТВЕТЫ
1. BaCl2 + 2AgNO3→Ba(NO3)2+2AgCl↓
2. Cu(NO3)2 + NaCl→CuCl2+NaNO3
3. Pb(NO3)2 + K2S→PbS↓+2KNO3
4. MgCl2
5. HNO3 + ZnSO4→H2SO4+Zn(NO3)2
6. 3Ca(NO3)2 +2H3PO4→Ca3(PO4)2↓+6HNO3
7. Ba(NO3)2 + Na2SO4→BaSO4↓+2NaNO3