- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку по теме: Типы химических реакций
Содержание
- 1. Презентация к уроку по теме: Типы химических реакций
- 2. Девиз урока. «Широко распростирает химия руки свои
- 3. Слайд 3
- 4. Слайд 4
- 5. Слайд 5
- 6. Слайд 6
- 7. Условия
- 8. Химические реакции.Как классифицировать ?
- 9. Тема урока: «Типы химических реакций»Запишите тему в рабочую тетрадь
- 10. Классификация
- 11. 2H2 + O2 → 2H2O 4P +
- 12. Cu(OH)2 → CuO + H2O 2HgO →
- 13. CuCl2 + Fe → Cu + FeCl2
- 14. Слайд 14
- 15. A + B → AB AB +
- 16. ФИЗКУЛЬТМИНУТКА«РЕАКЦИИ СОЕДИНЕНИЯ»
- 17. Слайд 17
- 18. Правила техники безопасностиПроводите опыты лишь с теми
- 19. AgNO3 + HCl = AgCl +
- 20. Проверьте свои знанияОпределите тип химической реакции. Распределите
- 21. Сравни и оцени.
- 22. Слайд 22
- 23. ГлоссарийХимическая реакция – процесс
- 24. Список литературыГабриелян О.С. Химия. Неорганическая
Слайд 1
МБОУ СОШ №7
г.Минеральные Воды
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
Учитель высшей квалификационной категории МЕЙБАТЯН
Слайд 2Девиз урока.
«Широко распростирает химия руки свои в дела человеческие…, куда
М.В.Ломоносов
Слайд 3
Все что нас окружает состоит из веществ. Кажется, что они живут своей жизнью, таинственной и непостижимой. Взаимодействуя, они изменяют свои свойства и состав. Без химических реакций невозможна жизнь и все многообразие веществ. И задача человека, изучив этот мир, постараться использовать полученные знания во благо.
Сегодня мы продолжим знакомство с этим удивительным и волшебным миром.
Слайд 4
Она
идет,
она
прошла! Никто
не скажет,
что пришла!
Она - ********** ******* !
Слайд 5
Что такое
химическая реакция?
Химические реакции или химические
Слайд 6
Выделение газа;
Образование осадка;
Выделение (поглощение) тепла и света;
Появление или изменение запаха или вкуса;
Изменение цвета.
Слайд 7Условия
1) Образование хлорида аммония
2) Горение магния
3) Взаимодействие алюминия с иодом
Смешивание веществ;
Нагревание;
Измельчение;
Соприкосновение;
Растворение.
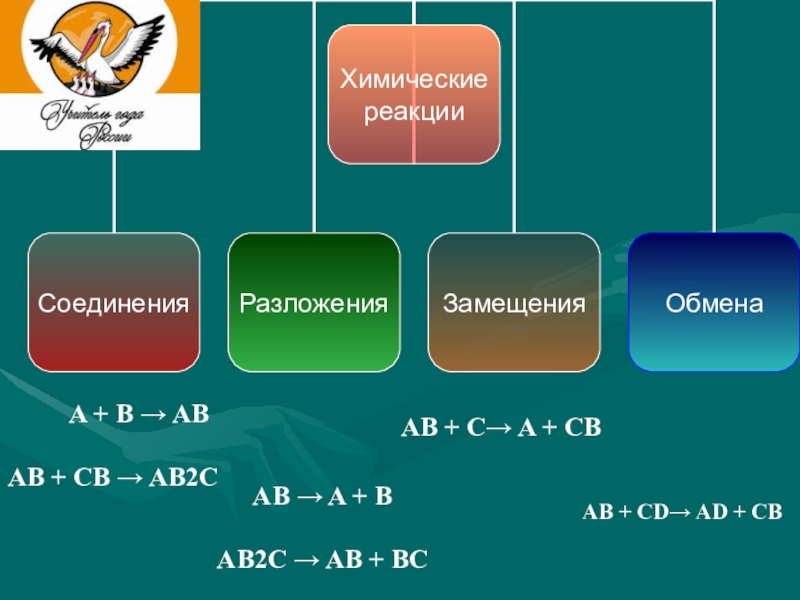
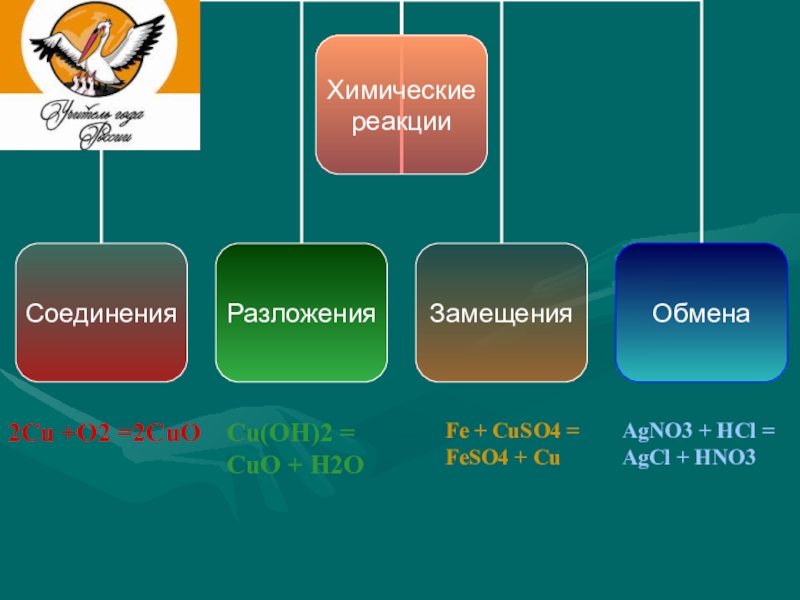
Слайд 10 Классификация
по числу и составу исходных веществ и продуктов реакции
реакция соединения
реакция разложения
реакция замещения
реакция обмена
Слайд 11
2H2 + O2 → 2H2O
4P + 5O2 → 2P2O5
Na2O
CaO + H2O → Ca(OH)2
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать
процесс, который протекает?
Реакции соединения
A + B → AB
AB + CB → AB2C
Слайд 12
Cu(OH)2 → CuO + H2O
2HgO → 2Hg + O2
CaCO3 →
2NO → N2 + O2
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать
процесс, который протекает?
Реакции разложения
AB → A + B
AB2C → AB + BC
Слайд 13
CuCl2 + Fe → Cu + FeCl2
Cr2O3 + 2Al →
Zn + 2HCl → ZnCl2 + H2
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать
процесс, который протекает?
Реакции замещения
AB + C→ A + CB
Слайд 14
BaCl2 + K2SO4 → BaSO4 + 2KCl
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать
процесс, который протекает?
Реакции обмена
AB + CD→ AD + CB
Слайд 17 Типы
Внимательно прочитайте инструктивную карточку по проведению опыта.
Соблюдая технику безопасности, проведите химическую реакцию.
Определите тип реакции, запишите уравнение реакции в соответствующую графу схемы (в тетрадь), укажите признаки прохождения реакции.
Подготовьте отчет своей группы.
Слайд 18Правила техники безопасности
Проводите опыты лишь с теми веществами, которые указаны учителем.
Вещества
Без указания учителя не смешивайте неизвестные вам вещества.
Нагревая пробирку с жидкостью, держите её так, чтобы отверстие было направлено в сторону и от вас и от соседей.
Не приступайте к выполнению опыта, не зная, что и как нужно делать.
При выполнении опытов пользуйтесь небольшими дозами веществ
Остатки веществ не высыпайте и не вливайте обратно в сосуд с чистыми веществами.
Проводите опыты только над столом и, закончив работу, приведите рабочее место в порядок.
Слайд 20Проверьте свои знания
Определите тип химической реакции.
Распределите предложенные вам уравнения.
2H2 +
3NaOH + H3PO4 = Na3PO4 + 3H2O
2Fe(OH)3 = Fe2O3 + 3H2O
P2O5 + 3H2O = 2H3PO4
Mg(OH)2 +2 HNO3 = Mg(NO3)2 + 2H2O
Ca + 2H2O = Ca(OH)2 + H2
CaCO3 = CaO + CO2
Fe +2 HCl = FeCl2 + H2
Слайд 22 Домашнее задание: стр.99-100, задача 4 стр.101,
Уходя с урока, не забудь оценить свое эмоциональное состояние, твои удачи на уроке.
Для этого тебе необходимо выбрать один из 3-х видов смайликов и показать.
Спасибо за урок!
До новых встреч!
Слайд 23 Глоссарий
Химическая реакция – процесс превращения исходных веществ в
Физические явления – явления, приводящие к изменению формы или агрегатного состояния вещества, но не приводящие к образованию новых веществ.
Химические явления – явления, при которых одни вещества превращаются в другие, отличающиеся от исходных составом и свойствами.
Коэффициенты – показывают количество молекул данного вещества.
Индексы – показывают количество атомов элемента в веществе.
Уравнения реакций – условная запись химической реакции
посредством химических формул и математических знаков.
Слайд 24 Список литературы
Габриелян О.С. Химия. Неорганическая химия. 8 класс :
Брейгер, Л. М. Нестандартные уроки. Химия. 8, 10, 11 классы / Л. М. Брейгер. - Волгоград : Учитель, 2004
http://www.nachalka.com/book/export/html/1325
http://www.youtube.com/watch?v=Le3Jxjx7ABs
http://www.himikatus.ru/art/nvideo_neorg/razlojenem.php
http://www.himikatus.ru/art/nvideo_neorg/gorenieamm.php
http://yandex.ru/yandsearch?text=%D1%
http://images.yandex.ru/yandsearch?stype=image&lr=51&noreask=1&source=psearch&text=%D1%84%