СОШ № 188 г. Новосибирска
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку по химии Арены, 10 класс
Содержание
- 1. Презентация к уроку по химии Арены, 10 класс
- 2. Арены – ароматические углеводороды, содержащие в молекуле
- 3. Физические свойства ареновБензол и его ближайшие гомологи
- 4. Гомологи Бензол - C6H6Толуол (метилбензол) - С6Н5СH3Этилбензол
- 5. Номенклатура ареновПервый гомолог бензола — метилбензол, или
- 6. Изомерия ареновСтруктурная изомерия в гомологическом ряду бензола
- 7. ПолучениеВ лаборатории1. Сплавление солей бензойной кислоты с
- 8. Химические свойства1. Присоединение галогенов, водорода
- 9. Применение:Бензол C6H6 – хороший растворитель. Бензол в
- 10. Контроль знаний
Арены – ароматические углеводороды, содержащие в молекуле бензольное кольцо с чередованием одинарных связей и двойных Общая формула: CnH2n-6., где n = 6,7 ….Особенности строения:замкнутая цепь из 6 атомов углеродаособая связь между 6 атомами С
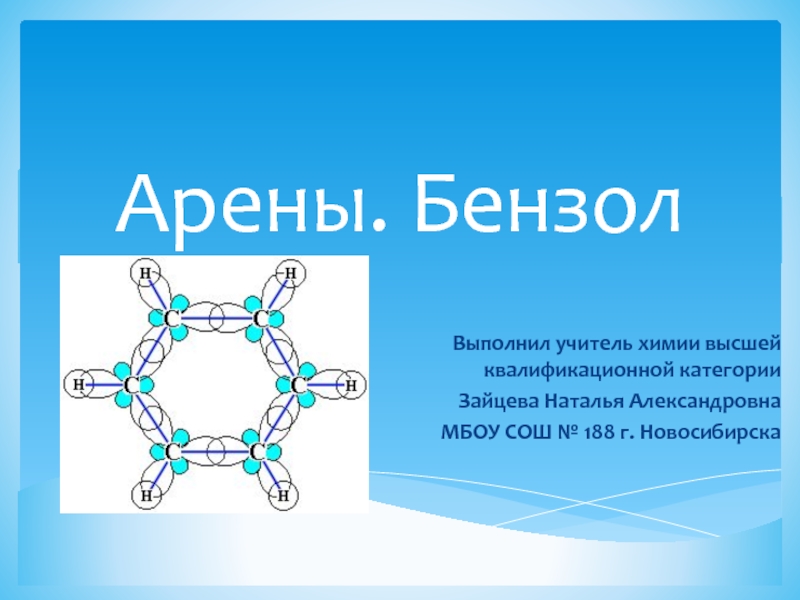
Слайд 1Арены. Бензол
Выполнил учитель химии высшей квалификационной категории
Зайцева Наталья Александровна
МБОУ
Слайд 2Арены – ароматические углеводороды, содержащие в молекуле бензольное кольцо с чередованием
одинарных связей и двойных
Общая формула:
CnH2n-6., где n = 6,7 ….
Особенности строения:
замкнутая цепь из 6 атомов углерода
особая связь между 6 атомами С
Слайд 3Физические свойства аренов
Бензол и его ближайшие гомологи – бесцветные жидкости со
специфическим запахом. Ароматические углеводороды легче воды и в ней не растворяются, однако легко растворяются в органических растворителях – спирте, эфире, ацетоне.
Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все арены горят коптящим пламенем ввиду высокого содержания углерода в их молекулах.
Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все арены горят коптящим пламенем ввиду высокого содержания углерода в их молекулах.
Слайд 4Гомологи
Бензол - C6H6
Толуол (метилбензол) - С6Н5СH3
Этилбензол - С6Н5С2H5
Ксилол (диметилбензол) -
С6Н4(СH3)2
Пропилбензол - С6Н5(CH2)2CH3
Кумол (изопропилбензол) - C6H5CH(CH3)2
Стирол (винилбензол) - С6Н5CH=СН2
Пропилбензол - С6Н5(CH2)2CH3
Кумол (изопропилбензол) - C6H5CH(CH3)2
Стирол (винилбензол) - С6Н5CH=СН2
Слайд 5Номенклатура аренов
Первый гомолог бензола — метилбензол, или толуол, C7H8 не имеет
изомеров положения, как и все однозамещённые производные. Второй гомолог C8H10, может существовать в четырёх формах: этилбензол C6H5-C2H5 и три диметилбензола, или ксилола, C6H4(CH3)2 (орто-, мета-, пара-ксилол, или 1,2-, 1,3-, 1,4-диметилбензол):
Радикал бензола C6H5- носит название фенил (и часто обозначается как Ph); названия радикалов гомологов бензола происходят от названий соответствующих углеводородов, при добавлении к корню суффикса -ил (толил, ксилил) и обозначая буквами (о-, м-, п-) или цифрами положение боковых цепей. Общее название для всех ароматических радикалов — арилы аналогично названию алкилы для радикалов алканов. Радикал C6H5-CH2- называется бензил.
Называя более сложные производные бензола, как и в случае алициклических соединений, из возможных порядков выбирают тот, при котором сумма цифр номеров заместителей в названии соединения будет наименьшей.
Названия высших гомологов часто производят не от названия ароматического ядра, а от названия боковой цепи, то есть рассматривают их как производные алканов.
Радикал бензола C6H5- носит название фенил (и часто обозначается как Ph); названия радикалов гомологов бензола происходят от названий соответствующих углеводородов, при добавлении к корню суффикса -ил (толил, ксилил) и обозначая буквами (о-, м-, п-) или цифрами положение боковых цепей. Общее название для всех ароматических радикалов — арилы аналогично названию алкилы для радикалов алканов. Радикал C6H5-CH2- называется бензил.
Называя более сложные производные бензола, как и в случае алициклических соединений, из возможных порядков выбирают тот, при котором сумма цифр номеров заместителей в названии соединения будет наименьшей.
Названия высших гомологов часто производят не от названия ароматического ядра, а от названия боковой цепи, то есть рассматривают их как производные алканов.
Слайд 6Изомерия аренов
Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей
в ядре. Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров, различающихся взаимным расположением заместителей. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-):
Радикалы ароматических углеводородов называют арильными радикалами. Радикал С6Н5 — называется фенил.
Радикалы ароматических углеводородов называют арильными радикалами. Радикал С6Н5 — называется фенил.
Слайд 7Получение
В лаборатории
1. Сплавление солей бензойной кислоты с твёрдыми щелочами:
t
C6H5-COONa + NaOH → C6H6 + Na2CO3
2. Реакция Вюрца-Фиттинга: (здесь Г – галоген)
С6H5-Г + 2Na + R-Г → C6H5-R + 2NaГ; С6H5-Cl + 2Na + CH3-Cl → C6H5-CH3 + 2NaCl
В промышленности
- выделяют из нефти и угля методом фракционной перегонки, риформингом (процесс образования из углеводородов линейного строения циклических и ароматических веществ) ;
- из каменноугольной смолы и коксового газа
1. Дегидроциклизацией алканов с числом атомов углерода больше 6:
, kat
C6H14 → C6H6 + 4H2
2. Тримеризация ацетилена (только для бензола) – р. Зелинского:
600°C, акт. уголь
3С2H2 → C6H6
3. Дегидрированием циклогексана и его гомологов:
t, kat
C6H12 → C6H6 + 3H2
t, kat
C6H11-CH3 → C6H5-CH3 + 3H2
4. Алкилирование бензола (получение гомологов бензола) – р Фриделя-Крафтса.
t, AlCl3
C6H6 + C2H5-Cl → C6H5-C2H5 + HCl
C6H5-COONa + NaOH → C6H6 + Na2CO3
2. Реакция Вюрца-Фиттинга: (здесь Г – галоген)
С6H5-Г + 2Na + R-Г → C6H5-R + 2NaГ; С6H5-Cl + 2Na + CH3-Cl → C6H5-CH3 + 2NaCl
В промышленности
- выделяют из нефти и угля методом фракционной перегонки, риформингом (процесс образования из углеводородов линейного строения циклических и ароматических веществ) ;
- из каменноугольной смолы и коксового газа
1. Дегидроциклизацией алканов с числом атомов углерода больше 6:
, kat
C6H14 → C6H6 + 4H2
2. Тримеризация ацетилена (только для бензола) – р. Зелинского:
600°C, акт. уголь
3С2H2 → C6H6
3. Дегидрированием циклогексана и его гомологов:
t, kat
C6H12 → C6H6 + 3H2
t, kat
C6H11-CH3 → C6H5-CH3 + 3H2
4. Алкилирование бензола (получение гомологов бензола) – р Фриделя-Крафтса.
t, AlCl3
C6H6 + C2H5-Cl → C6H5-C2H5 + HCl
Слайд 8Химические свойства
1. Присоединение галогенов, водорода
hν t,Pt или Ni
C6H6 +3Cl2 → C6H6Cl6 C6H6 + 3H2 → C6H12 (циклогексан)
2. Горение
2С6Н6+ 15O2 → 12CO2 + 6H2O
3. Полимеризация
t,kat
n CH=CH2 → (-CH-CH2-)n
│ │
C6H5 C6H5
стирол полистирол
4. Замещение:
- Галогенирование -
C6H6 + Cl2 AlCl3→ C6H5-Cl + HCl (хлорбензол)
C6H6 + 6Cl2 t ,AlCl3→ C6Cl6 + 6HCl (гексахлорбензол)
C6H6 + Br2 t,FeCl3→ C6H5-Br + HBr (бромбензол)
- Нитрование (с азотной кислотой)
C6H6 + HO-NO2 t, H2SO4→ C6H5-NO2 + H2O
C6H5-CH3 + 3HO-NO2 t, H2SO4→ СH3-C6H2(NO2)3 + 3H2O
2,4,6-тринитротолуол (тол, тротил)
5. Бензол не обесцвечивает бромную воду и водный раствор марганцовки, гомологи бензола окисляются перманганатом калия (обесцвечивают марганцовку)
C6H6 +3Cl2 → C6H6Cl6 C6H6 + 3H2 → C6H12 (циклогексан)
2. Горение
2С6Н6+ 15O2 → 12CO2 + 6H2O
3. Полимеризация
t,kat
n CH=CH2 → (-CH-CH2-)n
│ │
C6H5 C6H5
стирол полистирол
4. Замещение:
- Галогенирование -
C6H6 + Cl2 AlCl3→ C6H5-Cl + HCl (хлорбензол)
C6H6 + 6Cl2 t ,AlCl3→ C6Cl6 + 6HCl (гексахлорбензол)
C6H6 + Br2 t,FeCl3→ C6H5-Br + HBr (бромбензол)
- Нитрование (с азотной кислотой)
C6H6 + HO-NO2 t, H2SO4→ C6H5-NO2 + H2O
C6H5-CH3 + 3HO-NO2 t, H2SO4→ СH3-C6H2(NO2)3 + 3H2O
2,4,6-тринитротолуол (тол, тротил)
5. Бензол не обесцвечивает бромную воду и водный раствор марганцовки, гомологи бензола окисляются перманганатом калия (обесцвечивают марганцовку)
Слайд 9Применение:
Бензол C6H6 – хороший растворитель. Бензол в качестве добавки улучшает качество
моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C6H5NO2 (растворитель, из него получают анилин), хлорбензола C6H5Cl, фенола C6H5OH, стирола и т.д.
Толуол C6H5–CH3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Ксилолы C6H4(CH3)2. Технический ксилол – смесь трех изомеров (орто-, мета- и пара-ксилолов) – применяется в качестве растворителя и исходного продукта для синтеза многих органических соединений.
Изопропилбензол C6H5–CH(CH3)2 служит для получения фенола и ацетона.
Хлорпроизводные бензола используют для защиты растений. Так, продукт замещения в бензоле атомов Н атомами хлора – гексахлорбензол С6Сl6 – фунгицид; его применяют для сухого протравливания семян пшеницы и ржи против твердой головни. Продукт присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С6Н6Сl6 – инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые вещества относятся к пестицидам – химическим средствам борьбы с микроорганизмами, растениями и животными.
Стирол C6H5 – CH = CH2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.
Толуол C6H5–CH3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Ксилолы C6H4(CH3)2. Технический ксилол – смесь трех изомеров (орто-, мета- и пара-ксилолов) – применяется в качестве растворителя и исходного продукта для синтеза многих органических соединений.
Изопропилбензол C6H5–CH(CH3)2 служит для получения фенола и ацетона.
Хлорпроизводные бензола используют для защиты растений. Так, продукт замещения в бензоле атомов Н атомами хлора – гексахлорбензол С6Сl6 – фунгицид; его применяют для сухого протравливания семян пшеницы и ржи против твердой головни. Продукт присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С6Н6Сl6 – инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые вещества относятся к пестицидам – химическим средствам борьбы с микроорганизмами, растениями и животными.
Стирол C6H5 – CH = CH2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.