- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку ОВР 11 класс
Содержание
- 1. Презентация к уроку ОВР 11 класс
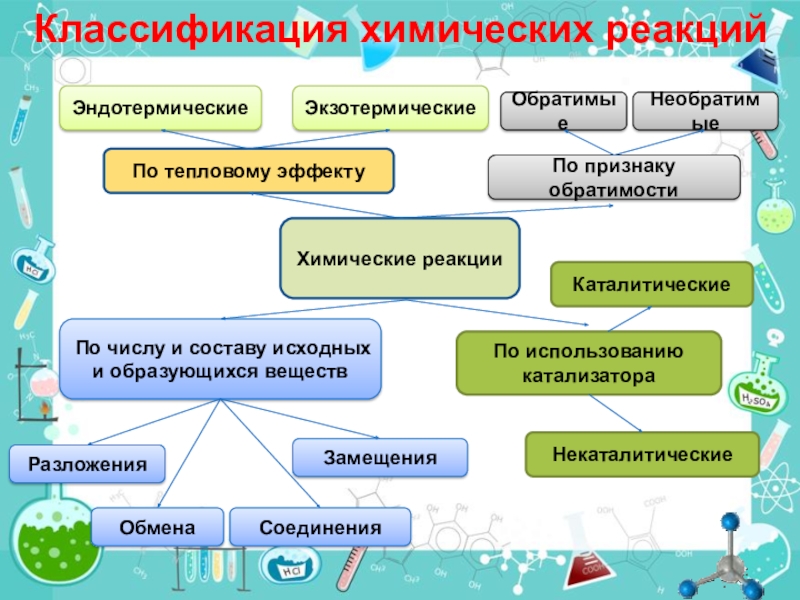
- 2. Химические реакцииПо тепловому эффектуЭкзотермическиеЭндотермическиеПо числу и составу
- 3. Слайд 3
- 4. Окислительно-восстановительные реакции
- 5. Слайд 5
- 6. ЛАБОРАТОРНЫЙ ОПЫТ №1Взаимодействие этанола с оксидом меди (II)Соблюдай правила техники безопасности!
- 7. Межмолекулярные ОВРЭто реакции, в которых степень окисления
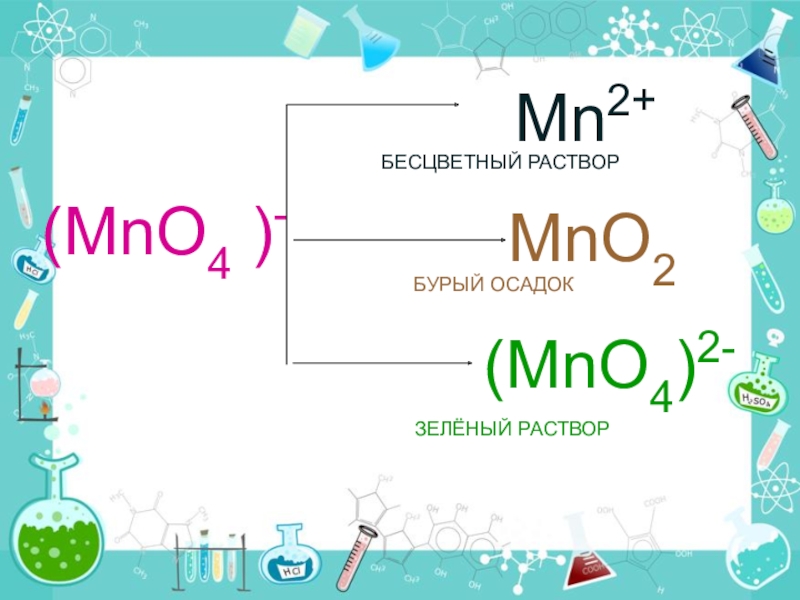
- 8. (MnO4 )-Mn2+MnO2(MnO4)2-БЕСЦВЕТНЫЙ РАСТВОРБУРЫЙ ОСАДОКЗЕЛЁНЫЙ РАСТВОР
- 9. СОСТАВЬТЕ УРАВНЕНИЯ овр МЕТОДОМ ЭЛЕКТРОННОГО БАЛАНСА:I вариантKMnO4
- 10. Внутримолекулярные реакцииЭто реакции в которых атомы, изменяющие степень окисления входят в состав одного соединения
- 11. Слайд 11
- 12. Классификация химических реакцийОпределите тип ОВР
- 13. Химические реакции в заданиях ЕГЭ4. Электроотрицательность.
- 14. Свойства серы
- 15. Установите соответствие между схемой реакции и изменением
- 16. Взаимодействие водорода с кислородом относится к реакциям
- 17. Внимание!!!Самостоятельная работа...
- 18. Слайд 18
- 19. Слайд 19
- 20. Окислительно-восстановительные реакции в природе и жизни человека:1.
- 21. выводы:4)Среда оказывает влияние на процесс. 1)ОВР чрезвычайно
- 22. Завершите фразы:Сегодня я узнал …Я понял, что …Теперь я могу …Меня удивило …Мне захотелось …
- 23. Задание на дом Составить уравнение ОВР обесцвечивания
- 24. « Знание только тогда знание, когда оно приобретено усилиями своей мысли, а не одной памяти»
Слайд 2Химические реакции
По тепловому эффекту
Экзотермические
Эндотермические
По числу и составу исходных и образующихся веществ
По
Обратимые
Необратимые
По использованию катализатора
Каталитические
Некаталитические
Разложения
Обмена
Замещения
Соединения
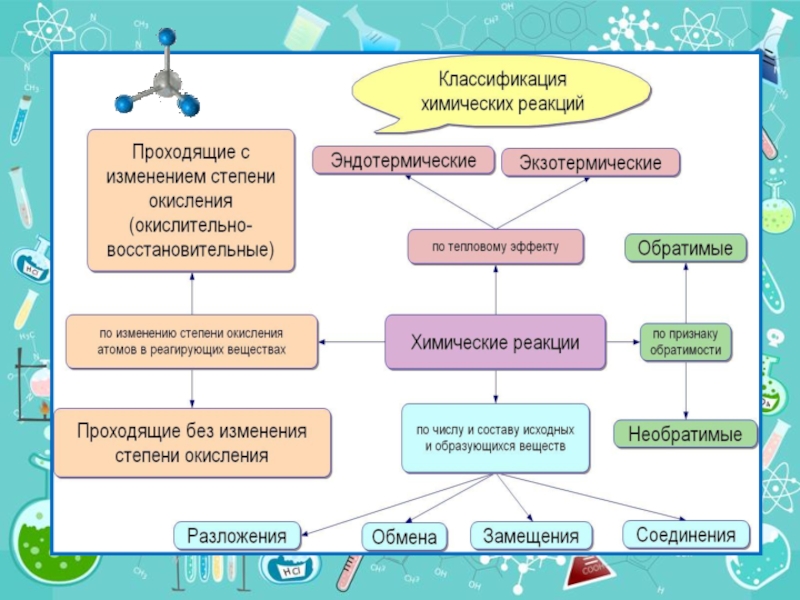
Классификация химических реакций
Слайд 6ЛАБОРАТОРНЫЙ ОПЫТ №1
Взаимодействие этанола с оксидом меди (II)
Соблюдай правила техники безопасности!
Слайд 7Межмолекулярные ОВР
Это реакции, в которых степень окисления изменяют атомы, входящие в
Реакции диспропорционирования
Это реакции, в которых атомы одного и того же элемента являются как окислителями, так и восстановителями
Слайд 9СОСТАВЬТЕ УРАВНЕНИЯ овр МЕТОДОМ ЭЛЕКТРОННОГО БАЛАНСА:
I вариант
KMnO4 + К2SO3 +H2SO4 =
II
KMnO4 + К 2SO 3 +H 2O =
Слайд 10Внутримолекулярные реакции
Это реакции в которых атомы, изменяющие степень окисления входят в
Слайд 12Классификация
химических реакций
Определите тип ОВР
2KClO3 (T) = 3O2 (Г) + 2KCl (т) + Q
2 вариант
Слайд 13Химические реакции
в заданиях ЕГЭ
4. Электроотрицательность. Степень окисления и валентность химических
19. Классификация химических реакций в органической и неорганической химии.
28. Электроотрицательность. Степень окисления и валентность химических элементов.Реакции окислительно-восстановительные
36. Реакции окислительно-восстановительные.
Слайд 14
Свойства серы
А) окислитель 1) 3 S + 2 H2O(пар) = 2H2S + SO2
Б) восстановитель 2) FeS + 2 HCl = FeCl2 + H2S
В) и окислитель, и 3) 2 H2S + 3 O2 = 2 H2O + 2 SO2
восстановитель 4) 2 SO3 = 2 SO2 + O2
Г) ни окислитель,
ни восстановитель
1.Установите соответствие между свойствами серы и уравнением ОВР, в котором она проявляет эти свойства
Слайд 15Установите соответствие между схемой реакции и изменением степени окисления восстановителя в
СХЕМА РЕАКЦИИ
ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ВОССТАНОВИТЕЛЯ
Слайд 16Взаимодействие водорода с кислородом относится к реакциям
2) обмена, экзотермическим
3) соединения, эндотермическим
4) соединения, экзотермическим
Слайд 20Окислительно-восстановительные реакции в природе
и жизни человека:
1. Фотосинтез
2.Реакции круговорота веществ в
3. Дыхание
4. Металлургия
5. Электроника
6. Электротехника
7. Энергетика
Слайд 21выводы:
4)Среда оказывает влияние на процесс.
1)ОВР чрезвычайно распространены;
2)Суть овр-переход электронов от
атомов,молекул или ионов к другим;
3)ОВР-единство двух противоположных
процессов-окисления и восстановления;
Слайд 22Завершите фразы:
Сегодня я узнал …
Я понял, что …
Теперь я могу …
Меня
Мне захотелось …