- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии на тему Кислоты
Содержание
- 1. Презентация к уроку химии на тему Кислоты
- 2. 08/30/2020Готовская СОШ
- 3. 08/30/2020Готовская СОШ
- 4. 08/30/2020Готовская СОШ
- 5. 08/30/2020Готовская СОШ
- 6. 08/30/2020Готовская СОШ
- 7. 08/30/2020Готовская СОШ
- 8. 08/30/2020Готовская СОШ
- 9. 08/30/2020Готовская СОШ
- 10. 08/30/2020Готовская СОШ
- 11. 08/30/2020Готовская СОШ
- 12. 08/30/2020Готовская СОШ
- 13. 08/30/2020Готовская СОШ
- 14. 08/30/2020Готовская СОШ
- 15. Спасибо за урок!
Слайд 208/30/2020
Готовская СОШ
Кислоты- это сложные вещества, имеющие в своем составе водород, способный замещаться на металл.
Слайд 308/30/2020
Готовская СОШ
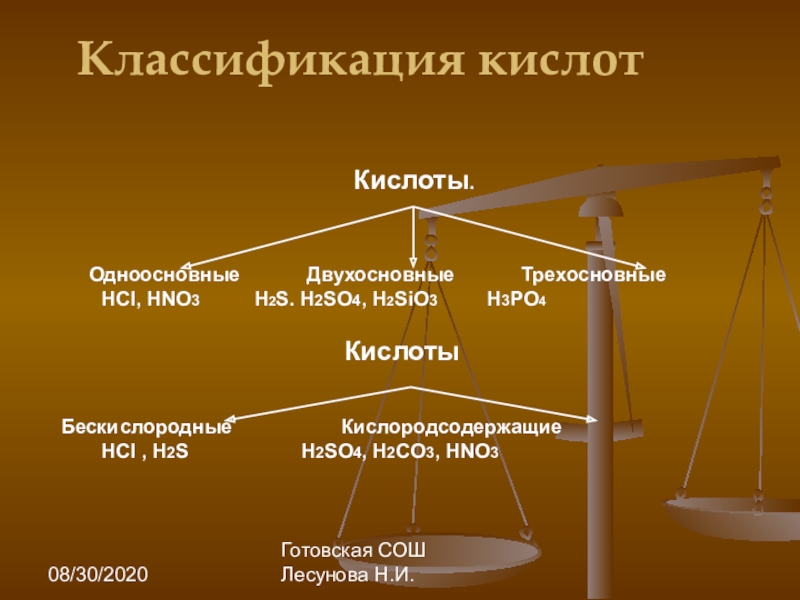
Классификация кислот
Кислоты.
Одноосновные Двухосновные Трехосновные
HCl, HNO3 H2S. H2SO4, H2SiO3 H3РO4
Кислоты
Бескислородные Кислородсодержащие
HCl , H2S H2SO4, H2CO3, HNO3
Слайд 408/30/2020
Готовская СОШ
Состав и названия кислот
I
Н
атом водорода,
который стоит на первом месте
I
Cl
кислотный
остаток
I I
НCl – соляная кислота
I II
Н2SO4 - серная кислота
I III
Н3PO4 – ортофосфорная
кислота
I I
НNO3 – азотная
I II
Н2SO3 – сернистая
I II
Н2CO3 – угольная
I II
Н2SiO3 - кремниевая
Слайд 508/30/2020
Готовская СОШ
Техника безопасности
при работе с кислотами
Проявлять осторожность.
При попадании на кожу смыть большим количеством воды.
При растворении наливать кислоту в воду.
Слайд 708/30/2020
Готовская СОШ
1. Изменение окраски индикаторов в кислой среде
Индикаторы были открыты Р.Бойлем
в ХVII веке
Индикатор - указатель
Слайд 1008/30/2020
Готовская СОШ
3.Взаимодействие с основными оксидами
Видеоролик
CuO+2HCl=CuCl2+H2O
Слайд 1108/30/2020
Готовская СОШ
Взаимодействие кислот с основаниями
(реакция нейтрализации)
видеоролик
NaOH + HCl = NaCl +H2 О
Слайд 1208/30/2020
Готовская СОШ
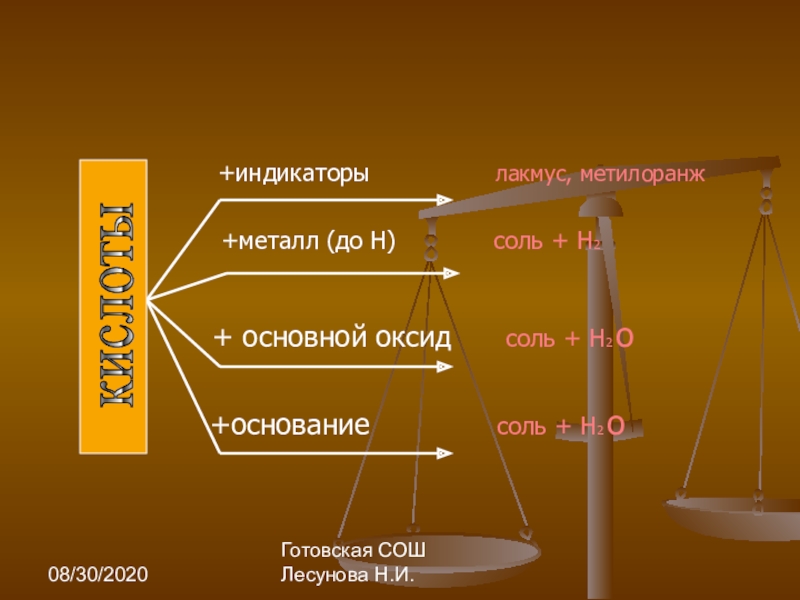
+индикаторы лакмус, метилоранж
+металл (до Н) соль + H2
+ основной оксид соль + H2 о
+основание соль + H2 о
кислоты
Слайд 1308/30/2020
Готовская СОШ
Проверь свои знания!
Na2O + 2HCl →2NaCl+H2O
NaOH + HCl →NaCl+H2O
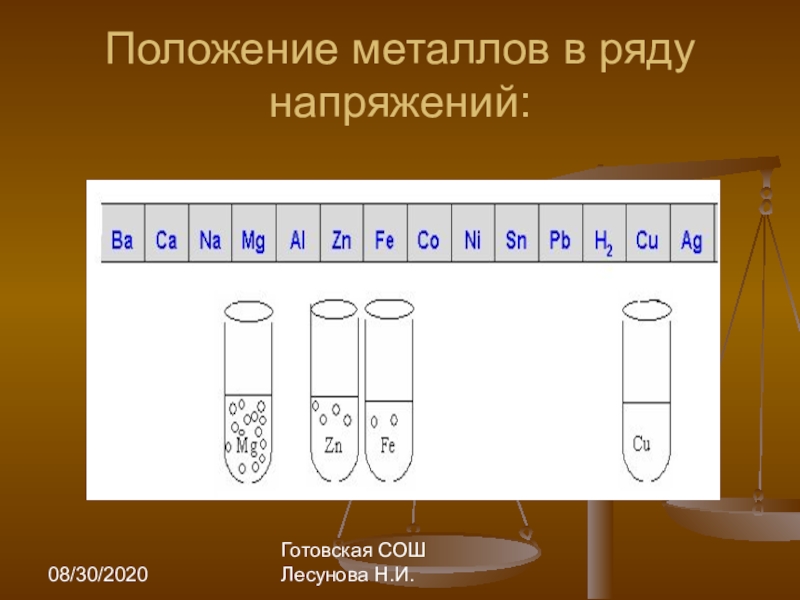
Zn + H2SO4 → ZnSO4+H2
Cu + HCl—/ →
H2SO4 + HCl —/ →
MgO+H2SO4→MgSO4+H2O
Ag + H3PO4—/→
2HBr + Ca →CaBr2+H2
Слайд 1408/30/2020
Готовская СОШ
Третий лишний!
CaO, Al2O3, H2SO4;
HNO3, Na2O, H2SO4;
NaOH, SO2, Ba(OH)2;
H3PO4, H2, H2SiO3.