- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии 8 класса Реакции замещения
Содержание
- 1. Презентация к уроку химии 8 класса Реакции замещения
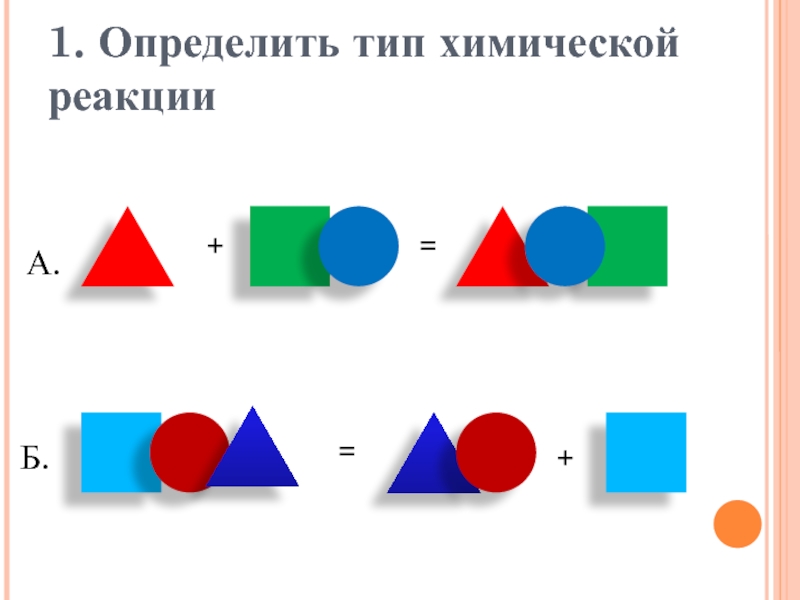
- 2. 1. Определить тип химической реакции +==+А.Б.
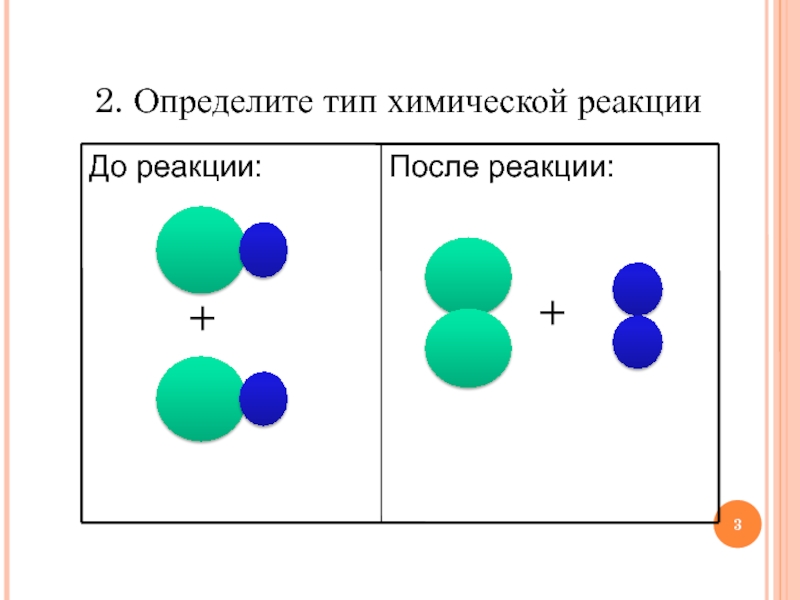
- 3. ++2. Определите тип химической реакции
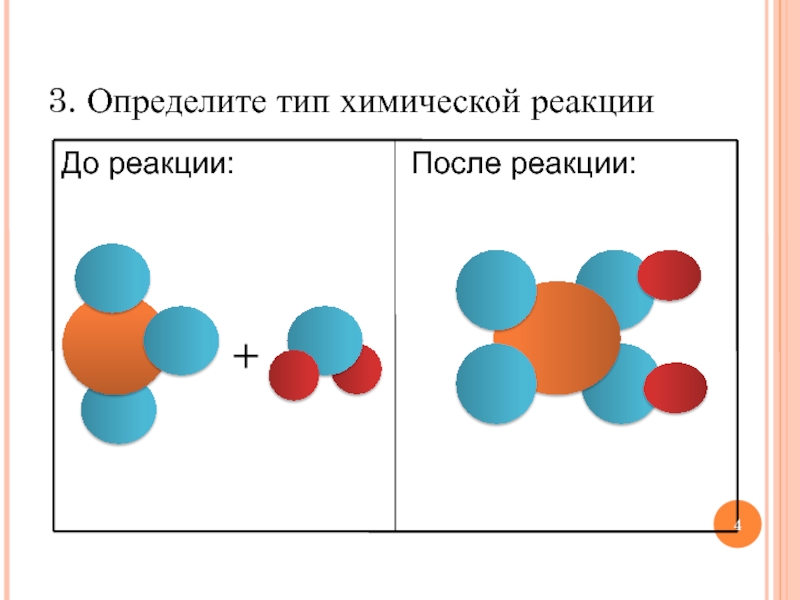
- 4. +3. Определите тип химической реакции
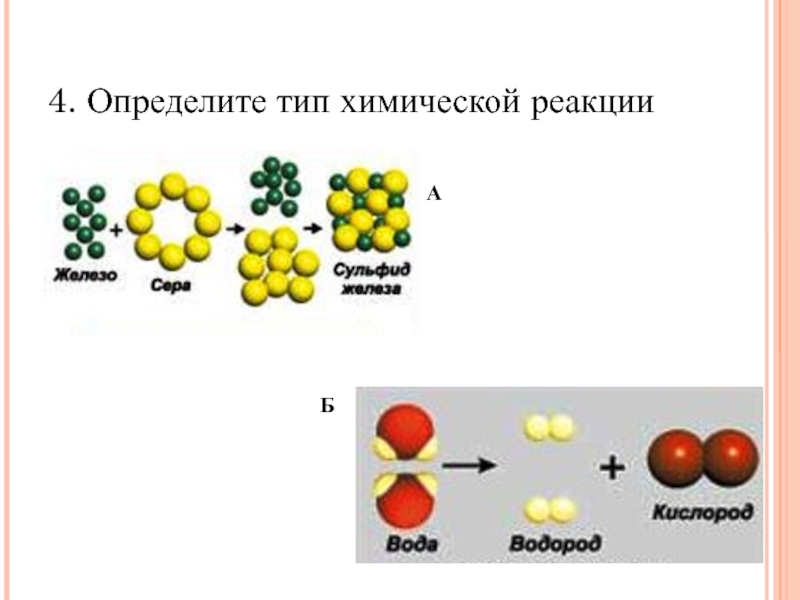
- 5. 4. Определите тип химической реакцииАБ
- 6. 5. Расставить коэффициенты в уравнениях реакций, указать
- 7. Проверка 1. А – соединения, Б –
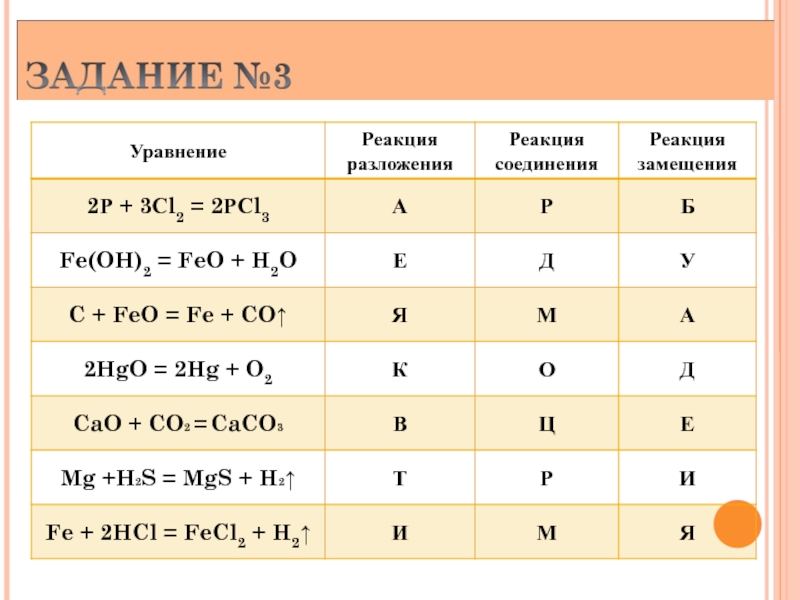
- 8. ЗАДАНИЕ 5.
- 9. Оценки «5» – 19-21«4» – 15-18«3» – 10 - 1410.12.11
- 10. Реакции замещения
- 11. Цель урока Определить понятие «Реакция замещения»;Выявить сущность
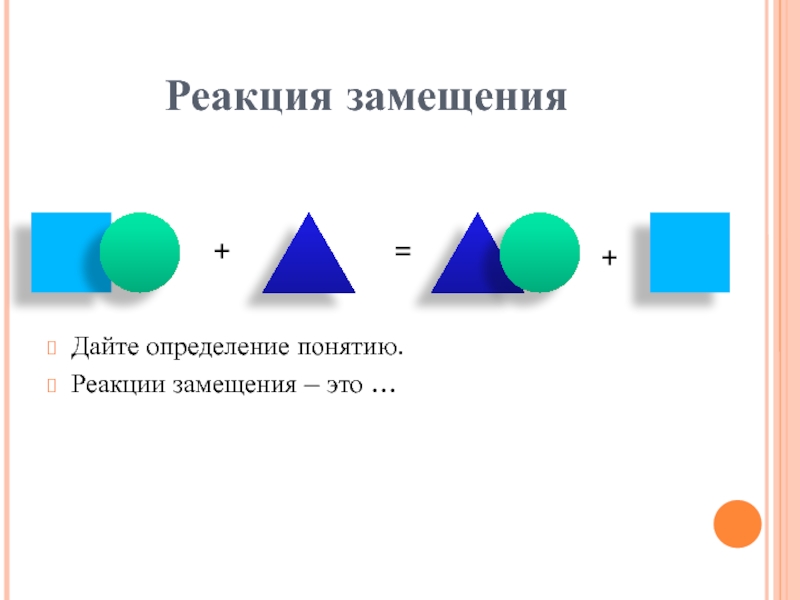
- 12. Реакция замещенияДайте определение понятию.Реакции замещения – это …+=+
- 13. Ряд активности металловСформулируйте умозаключение:Если ………… ……………….
- 14. Сформулируйте умозаключениеЕсли металл стоит ……… в ряду
- 15. Слайд 15
- 16. «Третий лишний» 12Na + Cl2 = 2NaClMg
- 17. «Третий лишний» 2CuSO4 + Fe = FeSO4
- 18. «Третий лишний» 3H2CO3 = H2O + CO22AgBr
- 19. ЗАДАНИЕ 5. Продолжить схемы реакцийAl +
- 20. Итог урокаВспомним цели урока:Определить понятие «Реакция замещения»;Выявить
1. Определить тип химической реакции +==+А.Б.
Слайд 65. Расставить коэффициенты в уравнениях реакций, указать тип реакции
10.12.11
HgO = Hg
+ O2 -
РСl3 + Сl2 = РСl5 -
Ag2O = Ag + O2 -
Fe(OH)2 = FeO + H2O -
Fе + FеСl3 = FеСl2 -
Р + Сl2 = РСl3 –
РСl3 + Сl2 = РСl5 -
Ag2O = Ag + O2 -
Fe(OH)2 = FeO + H2O -
Fе + FеСl3 = FеСl2 -
Р + Сl2 = РСl3 –
Слайд 7Проверка
1. А – соединения, Б – разложения
2. – разложения
3. –
соединения,
4. А. – соединения, Б – разложения
4. А. – соединения, Б – разложения
10.12.11
Ответы
Слайд 8ЗАДАНИЕ 5.
2HgO = 2Hg +
O2 - разложения
РСl3 + Сl2 = РСl5 - соединения
2Ag2O = 4Ag + O2 - разложения
Fe(OH)2 = FeO + H2O - разложения
Fе + 2FеСl3 = 3FеСl2 - соединения
2Р + 3Сl2 = 2РСl3 – соединения
РСl3 + Сl2 = РСl5 - соединения
2Ag2O = 4Ag + O2 - разложения
Fe(OH)2 = FeO + H2O - разложения
Fе + 2FеСl3 = 3FеСl2 - соединения
2Р + 3Сl2 = 2РСl3 – соединения
Слайд 11Цель урока
Определить понятие «Реакция замещения»;
Выявить сущность реакций замещения и условия
их протекания;
Научиться распознавать реакции замещения по уравнению среди других реакций;
Развивать умение писать уравнения реакций.
Научиться распознавать реакции замещения по уравнению среди других реакций;
Развивать умение писать уравнения реакций.
Слайд 13Ряд активности металлов
Сформулируйте умозаключение:
Если ………… ………………. до водорода в ряду
активности металлов, то ……… ………………. ……………… .. …………..
Li, К, Ва, Са, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Sn, Pb, H2 Cu, Hg, Ag, Au
Слайд 14Сформулируйте умозаключение
Если металл стоит ……… в ряду напряжения металлов, то он
способен вытеснять металлы, стоящие ……… из растворов их солей, и сам может быть вытеснен из растворов солей металлами, расположенными ……….. его
Li, К, Ва, Са, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Sn, Pb, H2 Cu, Hg, Ag, Au
Слайд 19ЗАДАНИЕ 5.
Продолжить схемы реакций
Al + CuCl2 →
Zn + H2SO4 →
CuSO4
+ Zn →
AgNO3 + Fe →
Fe2O3 + C →
AgNO3 + Fe →
Fe2O3 + C →
10.12.11
Слайд 20Итог урока
Вспомним цели урока:
Определить понятие «Реакция замещения»;
Выявить сущность реакций замещения и
условия их протекания;
Научиться распознавать реакции замещения по уравнению среди других реакций;
Развивать умение писать уравнения реакций.
Заявка на оценку:
«5» - 21 и более баллов
«4» - 17-20 баллов
«3» - 13 – 16 баллов
Научиться распознавать реакции замещения по уравнению среди других реакций;
Развивать умение писать уравнения реакций.
Заявка на оценку:
«5» - 21 и более баллов
«4» - 17-20 баллов
«3» - 13 – 16 баллов
Домашнее задание § 31 упр. 2