двуокись углерода.
В нормальных условиях это бесцветный не имеющий запаха газ с кисловатым вкусом, почти в 1,5 раза тяжелее воздуха, хорошо растворим в воде.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к сценарию научного спектакля Углекислый газ
Содержание
- 1. Презентация к сценарию научного спектакля Углекислый газ
- 2. Физические свойстваCO2 — углекислый газ, оксид углерода
- 3. Твёрдый углекислый газПри сильном охлаждении углекислый газ
- 4. Открытие углекислого газаУГ впервые описан известным алхимиком
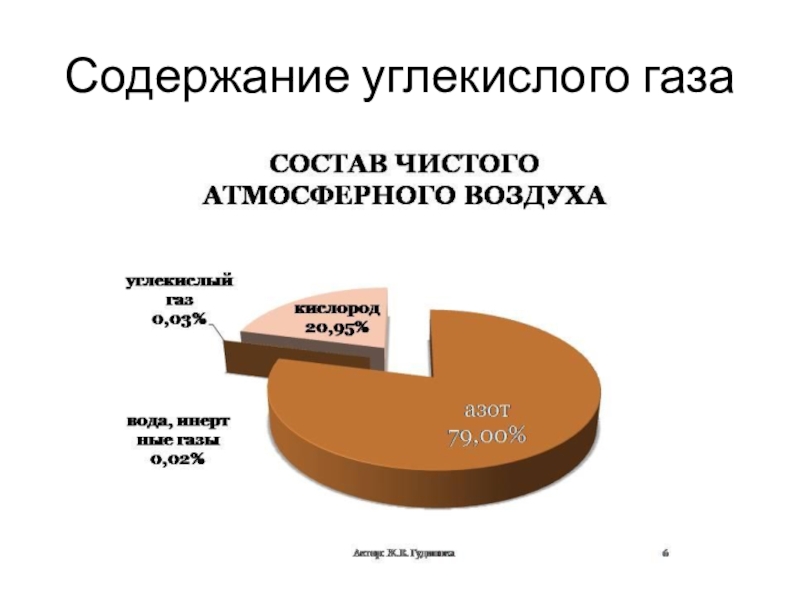
- 5. Содержание углекислого газа
- 6. Роль УГ на планетеФотосинтез кормит растения, которые,
- 7. Обнаружение углекислого газа Са(ОН)2 + СО2 = СаСО3 + Н2О
- 8. Источники углекислого газа
- 9. Получение углекислого газа
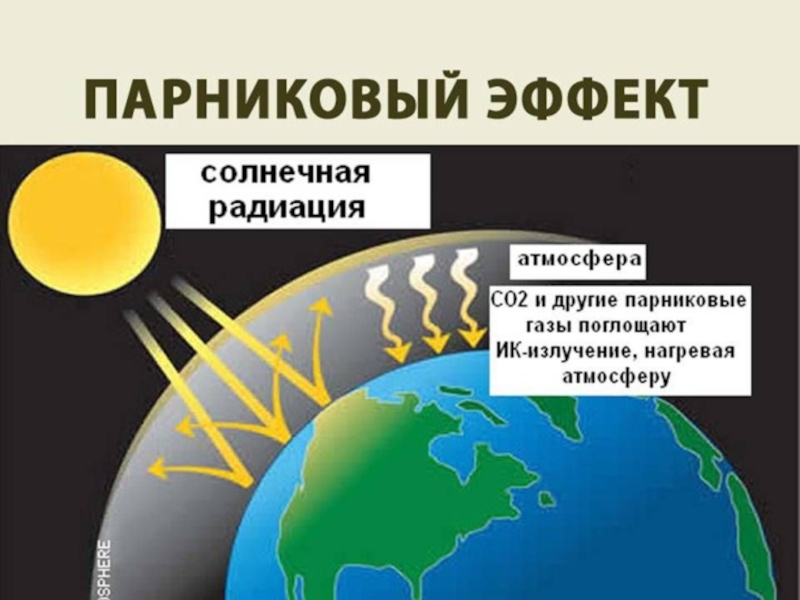
- 10. Парниковый эффект
- 11. Слайд 11
- 12. Применение углекислого газа
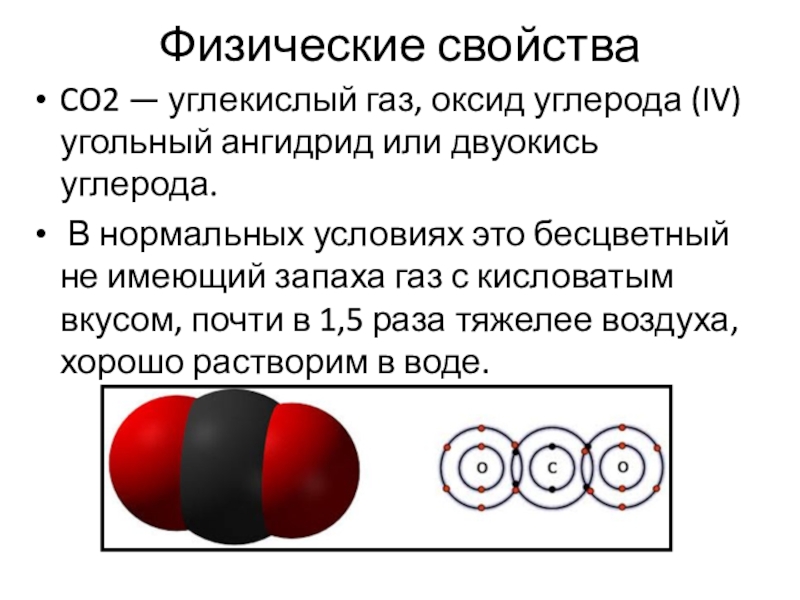
Физические свойстваCO2 — углекислый газ, оксид углерода (IV) угольный ангидрид или двуокись углерода. В нормальных условиях это бесцветный не имеющий запаха газ с кисловатым вкусом, почти в 1,5 раза тяжелее воздуха, хорошо растворим в воде.
Слайд 3Твёрдый углекислый газ
При сильном охлаждении углекислый газ кристаллизуется в виде белой
снегообразной массы — «сухого льда». При атмосферном давлении он не плавится, а испаряется наподобие густого белого тумана.
Слайд 4Открытие углекислого газа
УГ впервые описан известным алхимиком Яном Баптистом
Ван
Гельмонтом в 17 в.
Более подробно изучил это
вещество и выделил его в
чистом виде Джозеф
Пристли в 1771 году.
Более подробно изучил это
вещество и выделил его в
чистом виде Джозеф
Пристли в 1771 году.
Слайд 6Роль УГ на планете
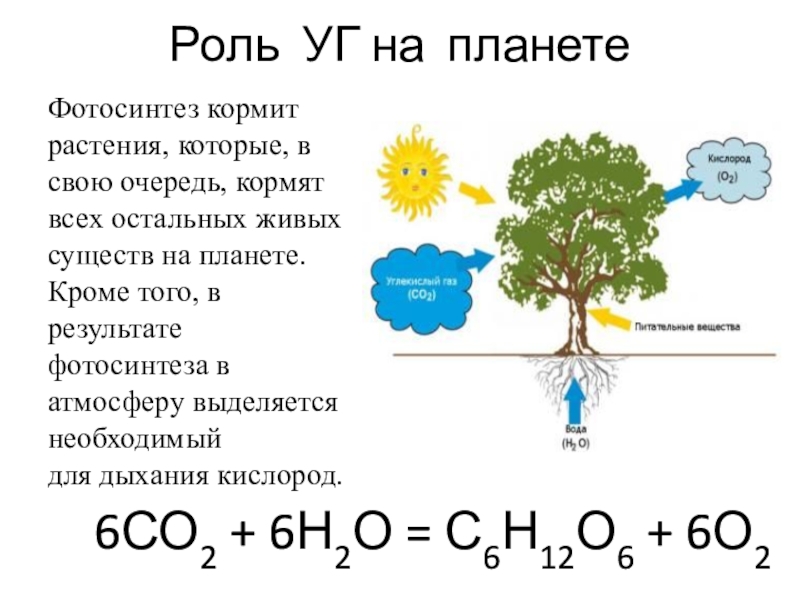
Фотосинтез кормит растения, которые, в свою очередь, кормят
всех остальных живых существ на планете. Кроме того, в результате фотосинтеза в атмосферу выделяется необходимый
для дыхания кислород.
для дыхания кислород.
6СО2 + 6Н2О = С6Н12О6 + 6О2
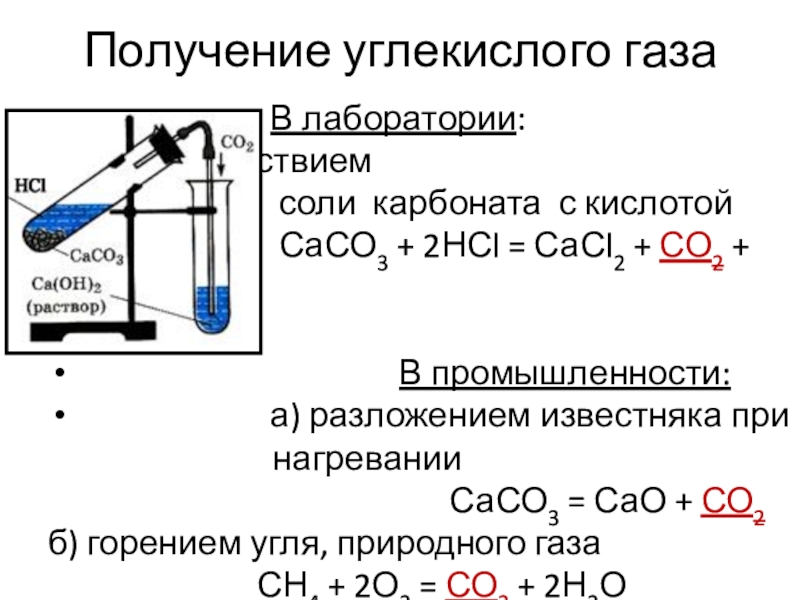
Слайд 9Получение углекислого газа
В лаборатории: взаимодействием
соли карбоната с кислотой
СаСО3 + 2НСl = СаСl2 + СО2 + Н2О
В промышленности:
а) разложением известняка при
нагревании
СаСО3 = СаО + СО2
б) горением угля, природного газа
СН4 + 2О2 = СО2 + 2Н2О
соли карбоната с кислотой
СаСО3 + 2НСl = СаСl2 + СО2 + Н2О
В промышленности:
а) разложением известняка при
нагревании
СаСО3 = СаО + СО2
б) горением угля, природного газа
СН4 + 2О2 = СО2 + 2Н2О